乳酸对肿瘤浸润调节性 T 细胞的代谢支持
调节性T(Treg)细胞,也称为抑制性T细胞,是控制体内自身免疫反应性的一类细胞,虽然对免疫稳态至关重要,但也是抗癌免疫的主要障碍,是近年来免疫学领域研究的热点。来自美国匹兹堡大学和约翰霍普金斯大学医学院的研究人员在Nature期刊上,发表题为“Metabolic support of tumour-infiltrating regulatory T cells by lactic acid”的研究成果,展示了称为肿瘤微环境(tumor microenvironment)的肿瘤周围区域中的代谢物改变、肿瘤内Treg细胞活性以及效应T细胞的关系,为肿瘤免疫治疗提供更为有效的方法。

1.Treg 细胞在肿瘤中不受葡萄糖代谢限制
之前已有肿瘤细胞代谢升高与效应 T 细胞功能降低的相关研究成果,为了确定肿瘤代谢升高与 Treg 细胞功能的关系,研究人员通过分析Foxp3报告小鼠的肿瘤细胞及瘤内Treg细胞,发现Treg 细胞在肿瘤内富集并且没有被抑制而是增殖活跃,可以推测Treg可能以一种不依赖于葡萄糖的方式完成代谢。与常规T细胞相比,基于荧光葡萄糖示踪剂 2NBDG 的 Treg 细胞的葡萄糖摄取显着降低进一步印证了上述猜想。
2.嗜糖使Treg细胞抑制能力(抑制杀伤性T细胞的免疫作用)降低
研究人员纯化了葡萄糖亲和能力低 (2NBDGlow) 和高嗜糖 (2NBDGhigh) 的Treg细胞亚群来观测它们的功能。结果显示,无论是何组织,与2NBDGlow-Treg细胞相比,2NBDGhigh-Treg细胞(高嗜糖)的抑制能力显著降低。研究人员进一步研究了两种细胞类型的转录组,以确定可能支持其功能的代谢途经。两种细胞亚群都表达糖酵解途径的上游酶,但是,2NBDGlow-Treg亚群参与糖酵解的末端步骤的酶,特别是乳酸脱氢酶(由Ldha编码)和单羧酸转运蛋白 MCT1(由 Slc16a1 编码)都有丰富的表达。虽然乳酸是糖酵解的最终产物,但它是许多细胞的重要能量来源。乳酸摄取是通过 MCT1 介导的,并被 LDH 转化为丙酮酸。葡萄糖缺乏的培养基中的Treg 细胞 Ldha 和 Slc16a1 的表达增加了。因此,Treg 细胞上调参与乳酸代谢的基因。
3. Treg细胞的乳酸代谢特性
乳酸在肿瘤微环境中高度富集,且能抑制常规T细胞的功能,但是根据上述研究结果发现Treg对乳酸具有抗性且在Treg中乳酸代谢途径能够得到激活。为了验证Treg是否可以消耗乳酸,来自Foxp3YFP-cre报告小鼠的淋巴细胞通过装载细胞内 pH 染料并与乳酸孵育,结果表明Treg可以摄取乳酸且在不同组织中具有异质性。
4.Treg细胞代谢乳酸以支持自身增殖和抑制功能
研究人员对用 [U13C]-L-乳酸(pH 6.9)脉冲处理的活化 Treg 和 Tconv 细胞进行了高分辨率质谱分析,证实 Treg 细胞吸收的乳酸明显多于 Tconv 细胞。Treg 细胞将 13C-乳酸转化为丙酮酸,随后转化为柠檬酸和苹果酸。当苹果酸离开线粒体并转化为草酰乙酸时,Treg细胞还将乳酸衍生的碳掺入磷酸烯醇丙酮酸(PEPCK)形成的磷酸烯醇丙酮酸(PEP)中。PEP 可以促进细胞增殖所必需的上游糖酵解中间产物,这表明乳酸可以作为糖异生燃料来源,减少 Treg 细胞对葡萄糖的需求。为了确定体内 Treg 细胞利用乳酸的情况,研究人员构建了一个组成性的Treg特异性的MCT1缺失(Slc16a1f/f Foxp3cre)小鼠,Slc16a1的缺失导致乳酸摄取丧失。结果显示MCT1 缺乏对于 Treg 细胞的存活和功能似乎是不必要的。用 B16 黑色素瘤接种 Slc16a1 f/fFoxp3 Cre 小鼠导致肿瘤生长减慢和存活时间延长。因此,Treg 细胞在代谢上是灵活的,它们可以利用 TME 中的“替代”代谢物来维持抑制特性。总而言之,肿瘤吞噬了其周围所有重要的营养物,而这些营养物是杀伤性T细胞进行攻击所需要的。此外,它们还排出乳酸,为Treg细胞提供食物,使它们能够守卫自己。
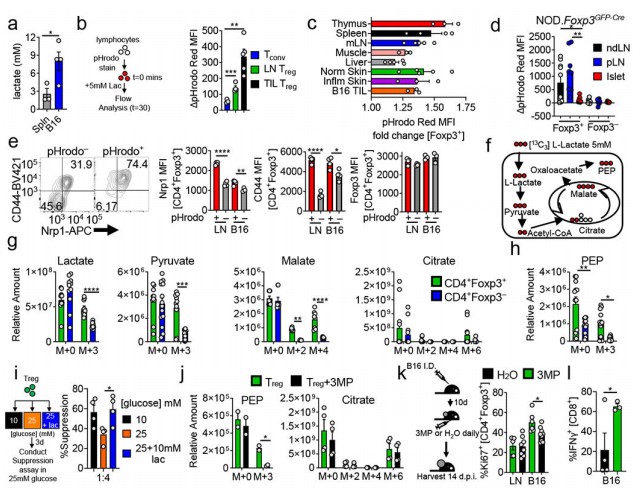
图 Treg细胞代谢乳酸以支持其增殖和抑制功能
Treg细胞特异性乳酸转运蛋白的缺失不仅导致肿瘤生长减少,而且可与检查点阻断免疫治疗协同作用。直接针对乳酸代谢或抑制肿瘤酸性的MCT1抑制可能打破肿瘤细胞和Treg细胞之间的代谢共生关系,降低肿瘤免疫的调节性T细胞屏障。
云克隆相关产品指标如下:
指标 | 指标号 |
Lactate Dehydrogenase (LDH) | B864 |
Lactic Acid (LA) | V643 |
Interferon Gamma (IFNg) | A049 |
Differentiation 4 (CD4) | B16 |
Homing Associated Cell Adhesion Molecule (HCAM/CD44) | A670 |