免疫疗法抗癌效果不理想?或许这篇文章能揭秘一二
肿瘤细胞或组织会通过各种方式逃避机体的免疫监视,目前针对肿瘤免疫逃逸的抗肿瘤免疫疗法主要是依赖免疫检查点阻断剂。虽然免疫疗法用于抗癌治疗的研究在近几年十分火热,但其抗癌效果并不如想象中理想。2021年10月,《Nature》杂志上发表了一篇题为“KDM5B promotes immune evasion by recruiting SETDB1 to silence retroelements”的文章,该文章揭示了KDM5B酶通过招募SETDB1使逆转录元件沉默来促进癌细胞的免疫逃逸。

KDM5B是一种对黑色素瘤维持和耐药性至关重要的H3K4去甲基化酶,参与表观遗传调控过程,与肿瘤等疾病有密切关系。该研究通过GO分析发现KDM5B的表达与免疫系统过程呈负相关,包括与关键的效应细胞因子IFNg和T细胞趋化因子CXCL9、CXCL10等的表达呈负相关。后研究者构建了黑色素瘤小鼠模型,发现KDM5B敲除组的肿瘤细胞被小鼠排斥,对照组则顺利形成肿瘤。且KDM5B敲除的肿瘤中T细胞,尤其是CD8+T细胞明显增加,肿瘤细胞死亡增加。对KDM5B敲除和对照组细胞进行转录组GSEA发现敲除组细胞中I型干扰素通路明显激活。I型干扰素是MHC I分子的正向调节分子,而研究者也发现KDM5B的敲除确实增加了MHC I分子表达,MHC I分子位于普通细胞表面,能被CD8+T细胞识别,向CD8+T细胞提呈内源性抗原。而且进一步研究发现KDM5B敲除的小鼠接受PD1治疗后效果更好(见图1)。
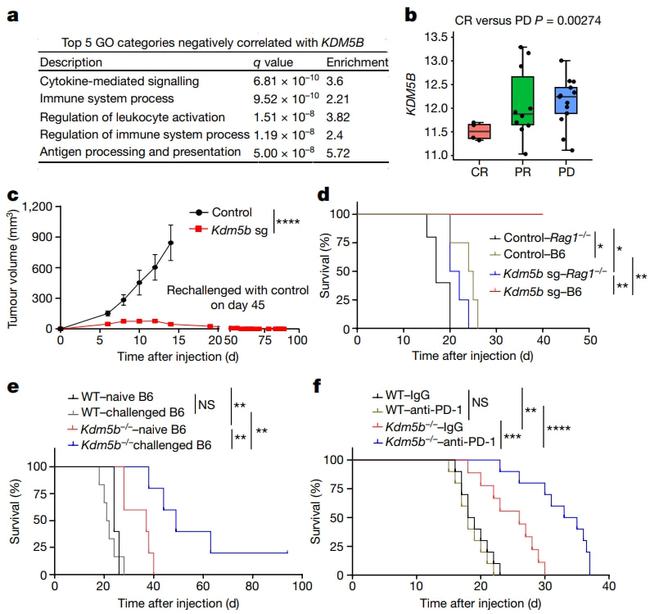
图1.敲除 KDM5B可提升小鼠抗肿瘤能力(图片来源于《Nature》杂志)
随后,研究者利用链特异性RNA-seq分析得出KDM5B敲除后来自于逆转录元件的转录本明显增加,敲除KDM5B后表达增加最明显的内源性逆转录因子是MMVL30,敲除MMVL30后,对干扰素刺激基因的诱导作用明显受到了抑制。利用CHIP-qPCR分析发现KDM5B能结合到逆转录元件位点,而这些位点的H3K4me3水平无明显变化,这表明KDM5B的作用与其去甲基化活性无关。在KDM5B敲除细胞中,H3K9甲基转移酶SETDB1在逆转录元件位点的结合降低。进一步研究表明这些逆转录因子的去抑制可以激活胞质RNA传感和DNA传感通路以及随后的I型干扰素反应,导致肿瘤抑制和诱导免疫记忆(见图2)。
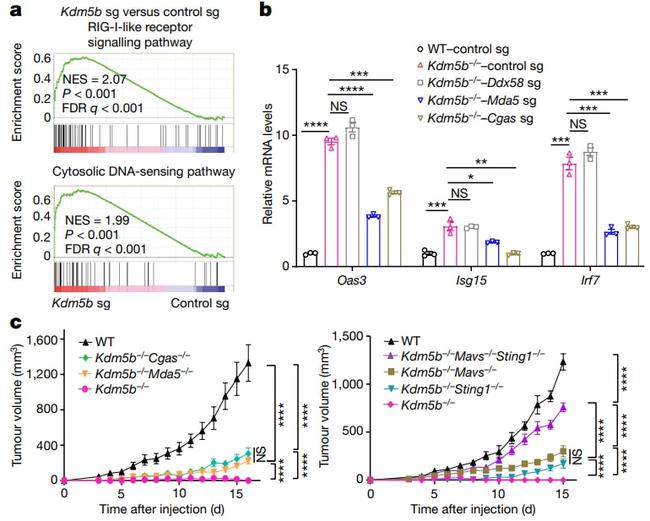
图2. 敲除KDM5B后,逆转录因子通过胞质RNA传感和DNA传感通路激活I型干扰素应答(图片来源于《Nature》杂志)
综上,KDM5B酶在肿瘤免疫逃逸及肿瘤细胞耐药性中发挥了重要作用,为开发KDM5B靶向和SETDB1靶向疗法以增强肿瘤免疫原性和克服免疫疗法耐药性提供了参考。
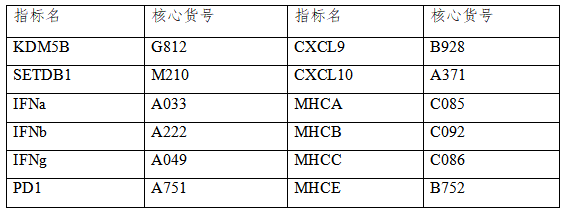
云克隆开发了上述研究中涉及的相关指标的蛋白、抗体、ELISA试剂盒等产品以助力肿瘤治疗相关研究,部分指标节选如下,供参考。
更多信息,欢迎访问http://www.cloud-clone.com/。