只知胰岛素?新的降糖分子FGF1了解一下
糖尿病是一种困扰全球数亿人的慢性代谢性疾病,如果未得到及时和正确的治疗,该病会在不知不觉中危害到心、肺、肾、神经、眼睛等脏器和器官。目前,胰岛素是控制血糖的主要手段。2021年12月,由美国索尔克生物研究所、荷兰的格罗宁根大学等研究机构的专家在“Cell Metabolism”杂志上发表题为“FGF1 and insulin control lipolysis by convergent pathways”文章,该研究发现了纤维细胞生长因子1(fibroblast growth factor 1, FGF1)与胰岛素一样,能快速有效地降低血糖,其作用方式与胰岛素存在差异,使FGF1有可能成为胰岛素抵抗或2型糖尿病患者新的降糖药物。

慢性高血糖和脂质异常是2型糖尿病的主要特征,其原因是胰岛素不能有效抑制肝脏葡萄糖生成和脂肪分解。此外,脂解增多导致游离脂肪酸(FFAs)在外周脂代谢场所(包括肝脏、肌肉和胰岛)的异常积累,可促进葡萄糖生成加重疾病。FGF1是FGF家族成员之一,在研究者已发表研究显示,外源给予FGF1可通过FGFR1依赖途径,迅速降低糖尿病模型小鼠的血糖水平。然而,其作用机理尚不清楚。文中研究者深入探讨了该现象背后的机制。
1.FGF1作用脂肪细胞FGFR1抑制脂肪分解
研究者对饮食诱导肥胖(diet-induced obese, DIO)的adR1 WT小鼠皮下注射FGF1,其血糖会迅速降低。然而,FGF1注射不影响adR1KO小鼠(成熟脂肪细胞中FGFR1选择性敲除)血糖的水平。该研究显示,FGF1通过作用脂肪细胞上相应受体FGFR1最终降低血糖。由于脂解有助于血糖增高,研究者进一步设计体内外实验明确FGF1与脂肪分解的关系。喂食6h后,FGF1 KO小鼠的性腺脂肪组织(gWAT)的脂解(FFA含量)较WT显著增加(图1A);对小鼠基质血管成分(SVF)来源的脂肪细胞和3T3-L1脂肪细胞系外源性给予FGF1后减少了FFA的产生(图1B和C)。为进一步明确FGF1在体内也可抑制脂解,DIO adR1WT和 KO小鼠禁食一夜(最大限度降低胰岛素水平,降低其干扰)后给予FGF1,WT小鼠血清FFA水平降低约30 %(相对于未给药组),但adR1KO小鼠无明显变化(图1D)。性腺脂肪组织(gWAT)的脂解检测亦有相似效应(图1E)。研究者还观察了FGF1处理对小鼠体内油酸(放射性标记)脂解的影响。相较于未处理组,FGF1预处理的adR1WT小鼠油酸的放射性增高(脂解率降低),而adR1KO小鼠脂解率没有明显变化(图1F)。上述实验证实,FGF1通过脂肪细胞FGFR1抑制脂肪分解。
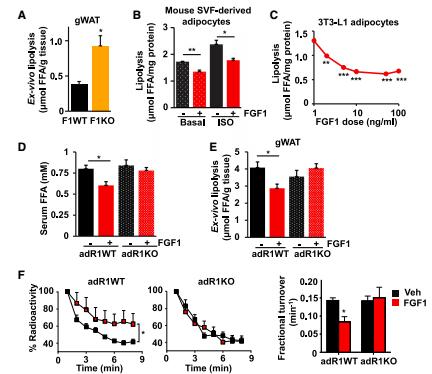
图1.FGF1抑制脂肪分解
(图片来源于《Cell Metabolism》杂志)
2. FGF1 通过脂肪细胞FGFR1抑制肝葡萄糖生成
胰岛素可通过抑制脂解从而抑制肝葡萄糖生成(hepatic glucose production, HGP)来调节血糖水平,而胰岛素抵抗会造成HGP的异常调节导致高血糖。FGF1是否也可以通过抑制脂解进而抑制HGP呢?研究者通过测量FGF1对糖异生底物(丙酮酸,pyruvate)的转化能力,探究其是否抑制脂解进而显著降低HGP。在丙酮酸耐受性测试(PTT)和甘油耐受性测试(甘油TT)中,发现FGF1预处理的ob / ob小鼠(肥胖症鼠)丙酮酸转化为葡萄糖的能力显著降低,而甘油转化为葡萄糖的能力没有差异(图2A)。脂肪细胞FGFR1敲除后,FGF1不影响丙酮酸转化为葡萄糖(图2B)。上述结果提示,FGF1抑制丙酮酸利用的能力依赖于脂肪细胞FGFR1的表达,且FGF1对糖异生的影响局限在丙酮酸的下游(甘油在丙酮酸上游,FGF1对甘油不敏感)。研究人员通过质谱法测量丙酮酸下游的中间体,发现ob / ob小鼠注射FGF1 2h后,在肝脏中的葡萄糖 6-磷酸(G6P)、果糖 6-磷酸 (F6P)、磷酸甘油酸 (PG)、磷酸烯醇丙酮酸(PEP)和草酰乙酸(OAA)减少,但参与三羧酸循环(TCA)的代谢物不受影响(图2C)。而adR1KO小鼠FGF1处理后上述代谢产物没有明显改变(图2D和E)。在对ob/ob小鼠进行短期连续给予FGF1 的高胰岛素钳夹实验,结果显示:基础内源性葡萄糖产生 (EGP) 减少了约 25%;在钳夹条件下,FGF1处理的小鼠需要更高的外源性葡萄糖输注率( GIR )来维持葡萄糖设定点(图2F)。上述实验显示,FGF1以脂肪FGFR1依赖性方式抑制HGP。
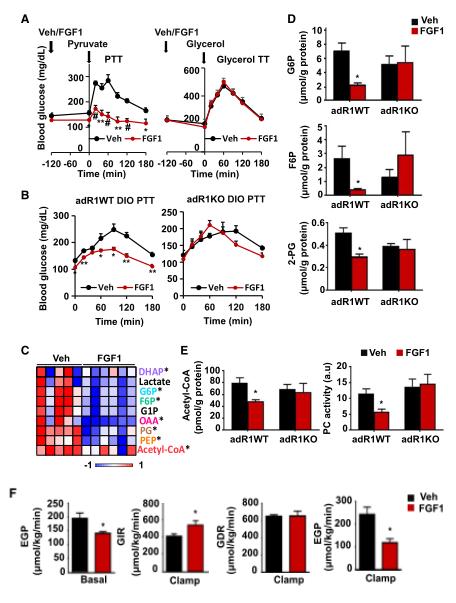
图2.FGF1以脂肪FGFR1依赖性方式抑制HGP
(图片来源于《Cell Metabolism》杂志)
3. FGF1依赖PDE4D抗脂解和抗HGP
胰岛素通过磷脂酰肌醇3-激酶(PI3K)信号激活磷酸二酯酶3B(PDE3B)进而抑制脂解。FGF1是否有相同的作用机制呢?研究人员使用PI3K抑制剂wortmannin消除了FGF1诱导的 3T3-L1 脂肪细胞脂解抑制(释放的FFA减少)。该结果提示PI3K的确是FGF1下游通路的靶点。然而,抑制PDE3B 并未减弱 FGF1 抗脂解作用,PDE4D抑制却显著减弱 3T3-L1 脂肪细胞以及SVF 来源的脂肪细胞中FGF1 的抗脂解活性。提示,FGF1的靶点蛋白是PDE4D而非PDE3B。研究者还在体内对DIO小鼠灌胃给予PDE4D抑制剂并注射FGF1,发现PDE4D抑制剂逆转FGF1的介导的抑制脂肪分解能力。 FGF1可减弱异丙肾上腺素(ISO)诱导的荷尔蒙脂肪酶(hormone-sensitive lipas,HSL)和围脂滴蛋白(perilipin)共定位(反映脂解),PDE4D抑制可消除体内FGF1的上述效应。上述结果均表明,PDE4D是FGF1的下游靶点。此外,研究人员还设计了一系列的实验证实FGF1/PDE4D通路的抗解脂活性需要PDE4D在S44处磷酸化,且该过程受生理性的饱食-空腹循环的调节。总之,该研究为FGF1依赖PDE4D抗脂解和抗HGP揭示了一条与胰岛素- PDE3B轴平行的通路(图3)。
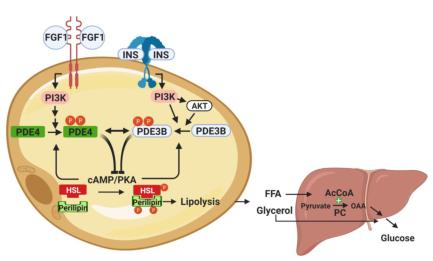
图3.FGF1诱导的抑制脂解和HGP模型
该研究显示FGF1与胰岛素一样,是通过抑制脂肪分解而快速降低肝脏葡萄糖生成。但二者作用方式不同,胰岛素是通过PDE3B抑制脂解,但FGF1依赖PDE4D,因而FGF1 / PDE4D通路在胰岛素抵抗下保持功能。FGF1的独特能力可能为胰岛素抵抗或2型糖尿病患者提供新的治疗方式。
云克隆为广大科研人员提供相关检测试剂产品:
指标名 | 核心货号 |
Fibroblast Growth Factor 1(FGF1) | A032 |
Insulin(INS) | A448 |
Fibroblast Growth Factor Receptor 1 (FGFR1) | B791 |
Phosphodiesterase 4D(PDE4D) | F644 |
Perilipin 1 (PLIN1) | C745 |
Phosphodiesterase 3B, cGMP Inhibited (PDE3B) | F640 |
Cyclic Adenosine Monophosphate (cAMP) | A003 |
Lipase, Hormone Sensitive (LIPE) | B276 |
Lipolysis Stimulated Lipoprotein Receptor (LSR) | D744 |
Free Fatty Acid Receptor 2 (FFAR2) | C949 |
Free Fatty Acid Receptor 1 (FFAR1) | C971 |
Glucose Transporter 1 (GLUT1) | B185 |