继钟南山院士团队后,云克隆再次助力广州医科大学发表《CELL》
2020 年 11 月 27 日,来自广州医科大学张玉霞教授团队和北京大学生物医学前沿创新中心白凡教授团队关于胆道闭锁(biliary atresia, BA)发病机制和治疗方法的联合研究成果“Liver Immune Profifiling Reveals Pathogenesis and Therapeutics for Biliary Atresia”发表于国际顶级期刊《Cell》。该文章中核心指标 C1Q 的检测试剂盒来自于云克隆,SEA747Mu(补体 1q(C1q) 检测试剂盒)。
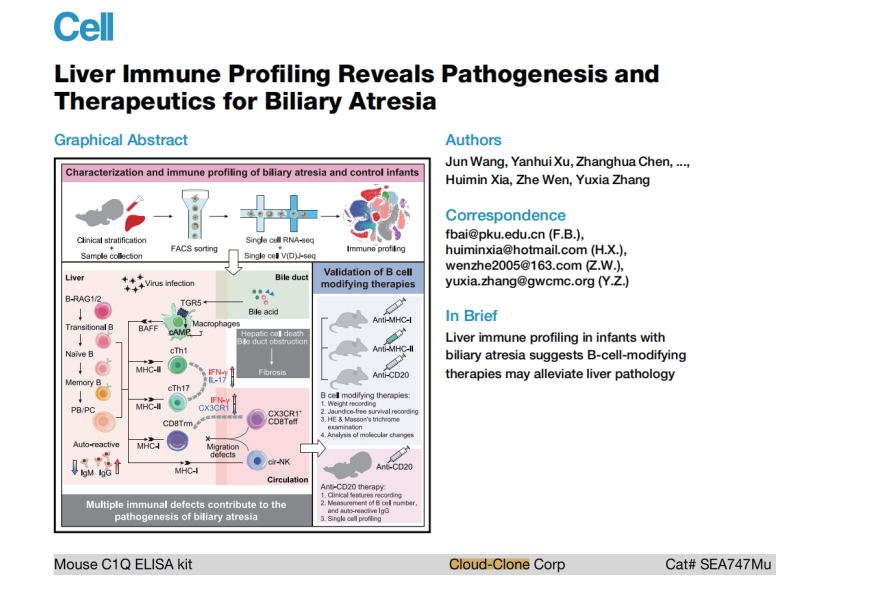
该工作以临床队列为研究对象,借助单细胞转录组学、动物及临床试验,系统描绘了BA患儿肝脏免疫图谱,提出B细胞耐受缺陷、杀伤性T细胞扩增、巨噬细胞低炎反应性、Kupffffer细胞清道夫功能障碍、组织修复性CX3CR1+T/NK细胞的缺乏共同促进了BA患儿的肝硬化和肝衰竭进展。团队首次报道了新生儿肝脏存在完整的B细胞造血功能,(病毒感染后)因B细胞耐受缺陷产生大量自身反应性IgG抗体。在一项探索性临床试验中,用利妥昔单抗(Rituximab)对4例BA患儿的B细胞进行了清除性治疗,发现治疗后BA患儿肝脏紊乱的免疫系统恢复到了健康状态。
该研究较为全面地揭示了导致 BA 患儿肝脏快速衰竭的免疫致病机制,同时提出 B 细胞修饰疗法可以改善 BA 患儿的肝脏病理,对重大新生儿肝脏疾病胆道闭锁的肝免疫微环境进行全面阐述,对人类肠 - 肝轴区域免疫领域的研究具有重要推动作用。