NSC12或将成为瓦尔登斯特伦巨球蛋白血症的新疗法

2020年11月16日,来自意大利瑞士工程科学院Aldo M. Roccaro教授及其团队在优秀国际期刊《Blood》上发表了 题 为“Halting the FGF/FGFR axis leads to anti-tumor activity in Waldenström's Macroglobulinemia by silencing MYD88”的文章。该文章发现使用NSC12可能成为瓦尔登斯特伦巨球蛋白血症的新疗法。
在这篇文章中,云克隆 ELISA试剂盒(白介素 6(IL6),SEA079Hu)获得了科研工作者的认可,荣登优秀国际期刊,助力科学研究。


研究介绍
瓦尔登斯特伦巨球蛋白血症(WM)是恶性 B淋巴细胞增殖性疾病。其特征是骨骼中存在 B淋巴细胞浸润,MYD88和 CXCR4体细胞突变。WM是一种无法治疗的疾病,因此探究新的负调控信号通路对于治疗 WM是必不可少的步骤。前人研究发现,NSC12可以沉默 FGF/FGFR信号级联,有抗肿瘤活性。因此,作者想将 NSC12运用到 WM的治疗之中。
FGFR3的超量表达会促使 WM病人的肿瘤细胞分化,而 FGF/FGFR通路在疾病中起着重要作用。因此,作者首先对病人的 CD19阳性细胞和正常细胞进行了转录组分析,发现 P13K-AKT,MAPK以及 STAT3相关基因簇有明显富集。并且,FGFs(FGF2,FGF7,FGF12,FGF18)基因在 WM细胞中显著高表达。在此基础上,作者将 WM细胞在有 /无 NSC12的两种条件下进行培养。结果发现,NSC12可以阻断 WM细胞存活。为了探究 NSC12依赖的抗 WM活性的潜在分子机制,作者比较了 NSC12处理和没处理的 WM细胞系。两者在细胞周期,DNA复制,细胞分裂中的都显著不同。而在 WM细胞中,NSC12还可以诱导细胞凋亡。NSC12诱导细胞凋亡会提升 caspase8和 PARP-cleavage。并且,NSC12处理的 WM细胞中 mtROS增加以及氧化胁迫发生。这些都是 NSC12影响 WM细胞存活的原因。
在 NSC12处理的 WM细胞中,NSC12诱导 FGFR相关基因沉默,P13K-AKT、STAT3和 MAPK信号通路相关基因受到抑制。在此过程中,作者发现 MYD88 相关基因显著下调,MYD88 蛋白也被沉默。于是作者想探究 NSC12 是否能够调控野生型 MYD88 和L265P-MYD88突变基因的表达。已有研究报道,突变型 MYD88可以引发造血细胞激酶(HCK)的转录并且作为 WM存活因子在 WM细胞中异常上调。作者发现,NSC12可以调控 HCK的表达并且在 WM细胞中显著沉默 HCK转录本。在 WM细胞中超量表达 MYD88基因,然后检测 NSC12对超量表达 MYD88基因的 WM细胞的靶向能力。结果发现,在 WM细胞中表达 MYD88能够显著削弱 NSC12诱导的细胞死亡,从而进一步证实了 NSC12通过 MYD88靶向作用 WM细胞的能力。之后,作者证实了 NSC12能抑制与 MYD88相关的 NF-κB信号通路基因簇。这些结果均说明 NSC12抑制 WM细胞中 FGFR信号靶点 .是通过沉默 MYD88以及 MYD88相关通路进行的。
在证实了 NSC12可以抑制 WM肿瘤细胞活性后,作者进一步探究 NSC12与其他试剂结合使用共同抗击 WM肿瘤细胞活性的能力。作者将视线放到了调控内质网(ER)应激和未折叠蛋白反应(UPR)上。通过在 WM细胞中添加蛋白酶体抑制剂(硼替佐米和卡非佐米),ER应激和未折叠蛋白反应提升,提高了 NSC12抗肿瘤活性。最后,作者证明了 NSC12依赖 FGF/FGFR通路的阻断作用是在 BM微环境下影响 WM细胞,导致体内抗肿瘤的活性。
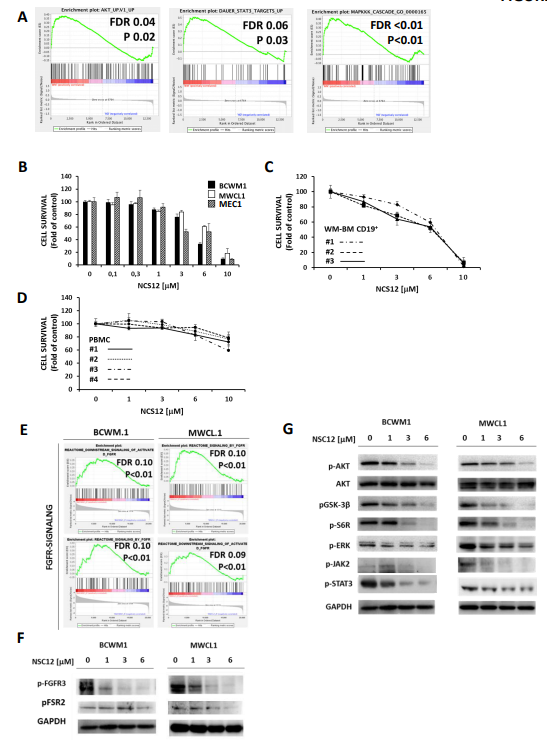
图 1 NSC12在 WM中具有抗肿瘤活性