云克隆多款ELISA试剂盒助力肥胖研究成果发表于《Cell Metabolism》
2021年6月8日,武汉大学李红良团队在国际代谢领域顶尖杂志《Cell Metabolism》(IF=21.567)在线发表了题为“TMBIM1 is an inhibitor of adipogenesis and its depletion promotes adipocyte hyperplasia and improves obesity-related metabolic disease”的论文。在这项研究中,云克隆ELISA试剂盒【胰岛素(INS)检测试剂盒(酶联免疫吸附试验法),CEA448Mu;瘦素(LEP)检测试剂盒(酶联免疫吸附试验法),SEA084Mu;脂联素(ADPN)检测试剂盒(酶联免疫吸附试验法),SEA605Mu】作为实验核心产品,受到科研工作者的认可,荣登优秀国际期刊。
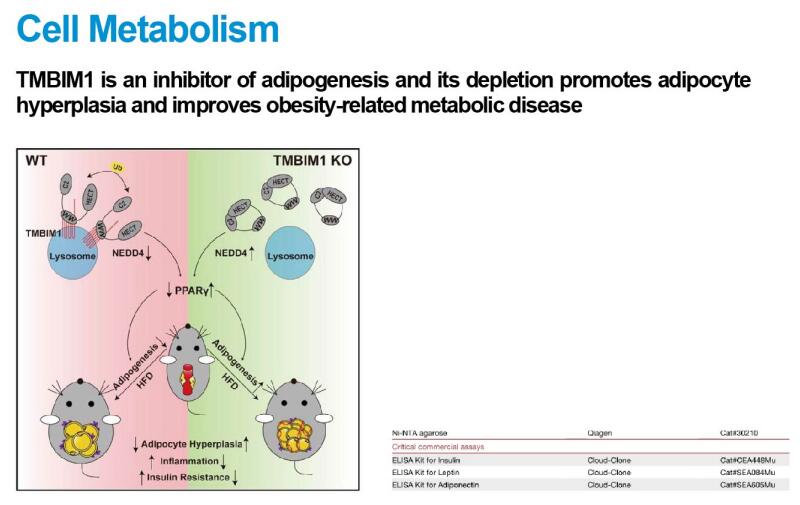
肥胖目前已成为全球的一个主要公共卫生挑战。此前已有研究指出,肥胖和心脏代谢疾病密切相关,如2型糖尿病、血脂异常和非酒精性脂肪肝疾病(NAFLD)等。如何治疗肥胖及其相关的代谢疾病成为和全球健康息息相关的重要课题。在这项研究中,研究团队通过转录组学方法,发现跨膜BAX抑制剂motif-containing 1 (TMBIM1)在脂肪前体细胞中差异表达。同时在小鼠动物实验研究中发现,脂肪细胞前体特异性TMBIM1敲除(KO)小鼠表现出白色脂肪组织增生,并能改善肥胖引起的系统代谢紊乱;而TMBIM1过表达的小鼠则有着相反的作用,脂肪细胞肥大且代谢紊乱进一步恶化。此外,成熟脂肪细胞特异性Tmbim1敲除不影响白色脂肪组织细胞数量或营养稳态。进一步的分子机制研究得出,TMBIM1结合并促进E3泛素连接酶NEDD4的自泛素化从而加速其降解,而NEDD4发挥稳定脂肪生成关键促进因子PPARγ的作用。因此,TMBIM1是通过降低PPARγ的稳定性而抑制脂肪生成。该研究首次证明TMBIM1是一种有效抑制脂肪生成的全新因子,提示TMBIM1是治疗肥胖相关代谢疾病的潜在治疗靶点。白色脂肪组织通过脂肪细胞增生的健康扩张可以抵消肥胖的负面代谢影响。因此,识别促进增生的新型脂肪生成调节因子可能会有助于肥胖诱导的代谢紊乱的有效治疗。