文献解读 | 可应用于靶向自传递和癌症治疗的多功能类套索自组装抗癌肽

2022年9月27日,北京化工大学生命科学与技术学院生物加工过程重点实验室Shi-Zhong Luo团队在《ACS Nano》上发表题为“Computer-Aided Design of Lasso-like SelfAssembling Anticancer Peptides with Multiple Functions for Targeted Self-Delivery and Cancer Treatments”的文章,利用计算机辅助方法设计了几种具有多种功能的类套索自组装抗癌肽。

在这篇文章中,云克隆试剂盒【激肽释放酶2(KLK2)检测试剂盒(酶联免疫吸附试验法),SED108Hu】受到科研工作者的认可,荣登优秀国际期刊。
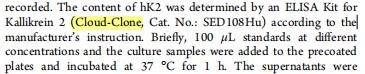

研究简介
生物制品作为一种恶性肿瘤的替代治疗方案,因其特异性和安全性而受到广泛关注,其中多肽因其结构多样性和抗肿瘤能力而成为有前景的候选药物之一。近年来,随着细胞识别和肿瘤表面蛋白研究的进展,研究人员发现了多种具有主动靶向能力的肽,三肽RGD就是其中之一,它可以特异性结合癌细胞上过度表达的αVβ3整合素。此外,药物传递系统已被开发用于肽药物的靶向传递,以提高其特异性和稳定性。
在本研究中,作者利用计算机辅助的方式设计了几种用于靶向癌症治疗的类套索自组装抗癌肽(LASAPs),其与各种靶向策略相结合,包括肿瘤生物标记物αVβ3整合素的靶向性;实体瘤酸性微环境的敏感性;以及对肿瘤过度表达酶人类激肽释放酶2(hK2)的反应性。引入二硫键环化和自组装策略以提高体内稳定性。在这些LASAP中,LASAP1被确定为优于其他药物,在血清中表现出更好的稳定性。因此,作者选择LASAP1来证明其设计理念。LASAP1由于其两亲性结构,可以自组装成纳米粒子,在表面显示iRGD,并且由于EPR效应和iRGD靶向αVβ3整合素,注射后可以积聚到肿瘤部位。纳米粒子可以在实体瘤的酸性微环境中分解,并被前列腺癌细胞分泌的过度表达的hK2裂解,以释放效应肽PTP-7b(FLGALFKALSHLL),该肽被酸性pH进一步激活。因此,LASAP1腹腔注射后可靶向模型小鼠的原位前列腺肿瘤,特异性抑制肿瘤生长,系统毒性低。
综上所述,作者以计算机辅助的方式设计出抗癌LASAP,其中,LASAP1表现优于其他。LASAP1纳米粒子能够响应酸性肿瘤微环境和肿瘤细胞分泌的hK2,因此具有精确的抗肿瘤活性和低系统毒性。这些功能使LASAP1成为一种潜在的自递送抗癌肽药物,这种设计思路将有助于靶向肽药物的开发。