细胞凋亡:传染性疾病的隐形战场与治疗新靶点
在多细胞生物中,细胞凋亡对于生物的发育和体内平衡是必不可少的。在感染过程中,细胞凋亡在清除感染细胞中起主要作用。传染性疾病控制细胞凋亡,并参与疾病的发病机制。细胞凋亡的增加可能以两种不同的方式参与:它可以帮助细胞内病原体的传播或诱导免疫抑制以促进病原体的传播;另一方面,细胞凋亡有利于从宿主中消灭感染因子。因此,细菌、病毒、真菌和寄生虫已经发展出通过细胞凋亡抑制宿主细胞死亡的策略,以允许病原体在细胞内存活和持续存在。阐明细胞内信号通路、参与的受体和干扰细胞凋亡的病原体因子,可以为阻断微生物作用于细胞凋亡通路提供新的治疗靶点。
1. 细胞凋亡与寄生虫感染
不同谱系的细胞经历凋亡可能向周围环境传递不同的信号。目前尚不清楚来自不同细胞谱系的凋亡细胞是否会对巨噬细胞活化产生不同的影响。德国汉堡-埃彭多夫大学医学中心Lidia Bosurgi团队发现在白细胞介素-4(IL-4)富集的环境中,巨噬细胞对凋亡中性粒细胞的感知触发了它们的组织重塑特征[1]。凋亡性中性粒细胞的摄取诱导巨噬细胞中的组织重塑谱,而凋亡肝细胞的感应促进免疫抑制或耐受性表型(图1)。这些明显的特征也在从感染曼氏血吸虫的小鼠中分离的肝髓细胞中被鉴定出来。通过暴露于凋亡的中性粒细胞,巨噬细胞的过继性转移可以改善曼氏血吸虫感染的结果。巨噬细胞吞噬凋亡细胞的能力依赖于吞噬受体的参与。他们发现吞噬受体AXL和MERTK是摄取凋亡中性粒细胞和T细胞所必需的。因此,依赖AXL和MERTK的吞噬作用控制了宿主对曼氏血吸虫感染的反应,总体上有助于寄生虫卵的清除。
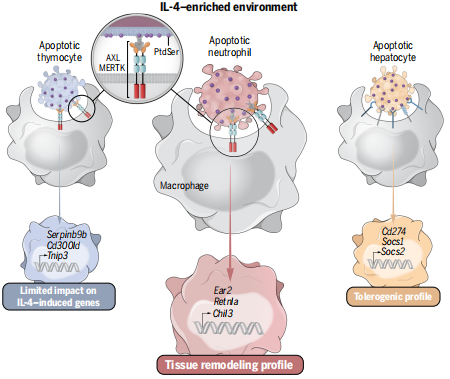
图1 不同凋亡细胞诱导外泌巨噬细胞对IL-4的不同功能反应
2. 细胞凋亡与细菌感染
细胞凋亡将细胞转化为凋亡细胞外囊泡(apoEV),然而,在细菌感染过程中释放的apoEV是否能产生抗菌反应仍然未知。第四军医大学口腔医学院组织工程中心Shiyu Liu团队开发了一种源自巨噬细胞的工程化凋亡细胞外囊泡(apoEV),并研究了它们作为脓毒症治疗多功能药物的潜力[2]。在金黄色葡萄球菌诱导的脓毒症模型中发现了广泛的巨噬细胞凋亡,揭示了对宿主的保护作用。从机制上讲,保护作用是由凋亡的巨噬细胞释放的apoEV介导的,apoEV结合含铁蛋白质,并通过与膜受体的相互作用中和α-毒素。为了进一步提高治疗效率,在apoEV中掺入预载抗炎剂(microRNA-146a)的介孔二氧化硅纳米颗粒。这些工程化的apoEV可以捕获铁并用其天然膜中和α-毒素,同时通过在吞噬细胞中释放微小RNA-146a来调节炎症(图2)。进一步地,红细胞被用来驱动工程apoev以扩展微观运动和旋转能力。红细胞驱动的工程化apoEV显示出高的毒素和铁捕获能力,最终提供了与高铁负荷条件相关的败血症的保护。

图2 负载miR-146a的工程化apoEV减轻了细菌诱导的炎症
3. 细胞凋亡与病毒感染
线粒体对感染的反应是凋亡途径中的亚致死信号。线粒体信号可能是炎症性的,但其机制仅部分了解。德国弗莱堡大学医学院Georg Häcker团队发现,胱天蛋白酶激活的DNase(CAD)介导线粒体促炎功能,并对宿主防御病毒感染做出了重大贡献[3]。在缺乏CAD的细胞中,亚致死信号的促炎活性降低。CAD的实验性激活导致短暂的DNA损伤和明显的DNA损伤反应,涉及主要的激酶信号通路NF-κB和cGAS/STING,驱动干扰素、细胞因子/趋化因子的产生并吸引中性粒细胞。CAD缺陷细胞对病毒感染的反应减弱。流感病毒感染的CAD缺陷小鼠表现出肺组织炎症减少、病毒滴度升高和体重减轻加剧(图3)。因此,CAD将线粒体凋亡系统和细胞死亡半胱天冬酶与宿主防御联系起来,其驱动的DNA损伤是感染炎症反应的生理因素。
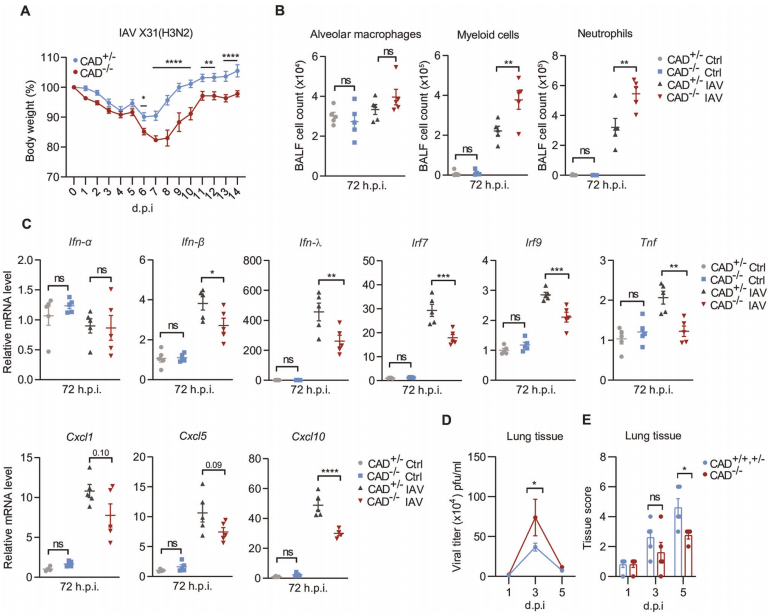
图3 CAD有助于小鼠感染甲型流感病毒期间的炎症和免疫防御
云克隆不仅可提供脓毒症、牙周炎等感染性疾病动物模型,还具有多个物种淋巴内皮细胞、淋巴单核细胞等原代细胞产品和各类感染免疫、细胞凋亡相关指标检测产品,以及上述IL-4、NF-κB、STING等相关产品,可助力广大科研工作者进行细胞凋亡与病原微生物感染疾病相关研究。
相关原代细胞产品
小鼠真皮淋巴内皮细胞(DLEC)原代细胞·CSI078Mu01
小鼠淋巴单核细胞(LMC)原代细胞·CSI166Mu01

相关动物模型
牙周炎大鼠模型
建模方法:
1. 大鼠经腹腔注射麻醉。
2. 用牙科探针分离第一、二磨牙牙间间隙,采用直径为0.2mm的正畸不锈钢丝结扎大鼠双侧上颌第一磨牙牙颈部,用持针器夹持结扎丝从大鼠上颌双侧第一磨牙远中腭侧进入,环绕上颌第一磨牙一周后,在腭侧偏近中处结扎固定,结扎丝末端保留3mm回弯置于龈下,防止结扎丝划伤口腔内软组织,且不损伤牙龈的结合上皮。
3. 术后严密观察大鼠的状态,从实验当天起喂食糖水,12小时后进食,每天高糖饮食喂养( 饮用水为 10% 葡萄糖水,饲料为 10%葡萄糖水浸泡变软的常规饲料) 。术后每周检查牙周结扎情况,并观察牙周组织的状况。
脓毒血症大鼠模型
建模方法:
1. 称量大鼠,麻醉,腹部正中剃毛后用碘酒及酒精擦拭手术区域。
2. 沿腹白线切开腹腔约2cm,找出盲肠,用5-0缝线结扎约1/3盲肠,以21G针头贯通穿刺结扎的盲肠2次。轻轻挤压使少量肠内容物从穿刺孔溢出确保通畅;将处理好的盲肠回纳入腹腔,用5-0缝线缝合内层,3-0缝线缝合外层,将大鼠置于加热垫维持肛温在37±0.5℃。
3. 待大鼠苏醒后自由饮水,正常饲养。
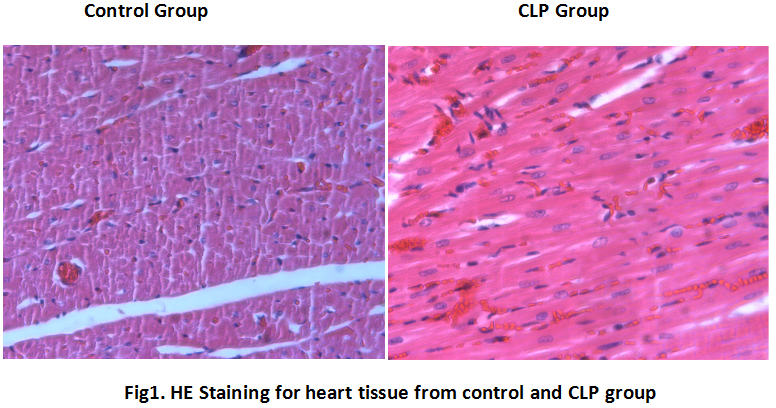
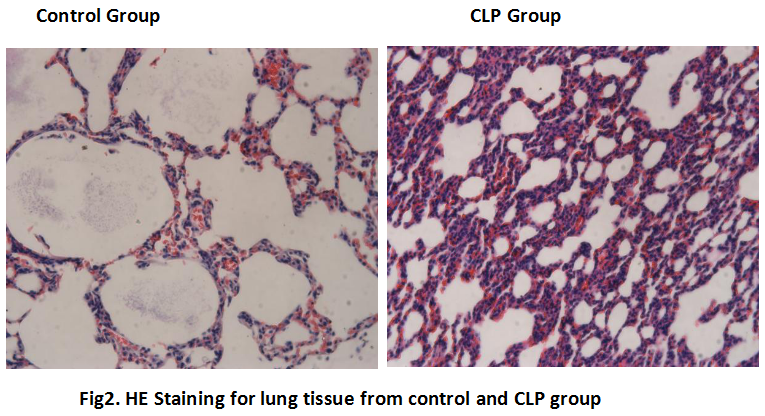
4. 2d后,麻醉大鼠,于腹主动脉取血5ml,室温静止2h, 4℃离心机3000r/min离心10min,分离出上层血清,置-80℃冰箱保存备用。处死大鼠,取出心脏、肝脏、肾脏、肺、小肠,4%多聚甲醛固定,石蜡包埋切片(厚4um),HE染色,观察病理改变,其余组织置于-80℃冰箱备用。
参考文献
[1]Liebold I, Al Jawazneh A, Casar C, et al. Apoptotic cell identity induces distinct functional responses to IL-4 in efferocytic macrophages. Science. 2024;384(6691):eabo7027. (IF=44.7)
[2]Li Y, Qu G, Dou G, et al. Engineered Extracellular Vesicles Driven by Erythrocytes Ameliorate Bacterial Sepsis by Iron Recycling, Toxin Clearing and Inflammation Regulation. Adv Sci (Weinh). 2024;11(13):e2306884. (IF=14.3)
[3]Moeed A, Thilmany N, Beck F, et al. The Caspase-Activated DNase drives inflammation and contributes to defense against viral infection. Cell Death Differ. 2024;31(7):924-937. (IF=13.7)