细胞死亡的双刃剑:坏死性凋亡在癌症治疗中的新希望
细胞凋亡历来被认为是程序性细胞死亡的唯一形式,而坏死被认为是一种不受分子事件调节的“意外”死亡类型,被认为是与凋亡完全相反的细胞死亡方式。直到坏死性凋亡的发现,作为一种新的程序性坏死细胞死亡形式,其机制与细胞凋亡相似,形态与坏死相似。坏死性凋亡在癌症生物学的调节中发挥着关键作用,包括癌症发生、癌症转移、癌症免疫和癌症亚型。作为细胞凋亡和坏死的结合,坏死性凋亡对癌症具有以下双重作用:一方面,坏死性凋亡途径的关键介质单独或联合被认为可以促进癌症转移和癌症进展;然而,另一方面,坏死性凋亡也是一种“故障安全”机制,在细胞凋亡受损时防止肿瘤发展。考虑到坏死性凋亡在癌症生物学中的关键作用,它成为癌症治疗的新靶点。
1. 坏死性凋亡与乳腺癌
癌基因诱导的复制应激会产生内源性DNA损伤,激活cGAS-STING介导的信号传导和肿瘤抑制。然而,内源性DNA损伤激活cGAS的确切机制仍然是个谜。美国北卡罗来纳大学教堂山分校Lineberger综合癌症中心Gaorav P. Gupta团队报道DNA双链断裂传感器MRE11通过调节cGAS激活的关键作用抑制乳腺肿瘤的发生[1]。他们发现,MRE11-RAD50-NBN复合物与核小体片段的结合对于从酸性斑块介导的隔离中置换cGAS是必要的,这使得它能够被dsDNA动员和激活。因此,MRE11对于cGAS在致癌应激、细胞质dsDNA和电离辐射下的激活至关重要。此外,MRE11依赖性cGAS激活促进ZBP1-RIPK3-MLKL介导的坏死性凋亡(图1),这对抑制致癌增殖和乳腺肿瘤发生至关重要。人类癌症三阴性乳腺癌中ZBP1的下调与基因组不稳定性增加、免疫抑制和患者预后不良有关。这些发现证实MRE11是连接DNA损伤和cGAS激活的关键介质,通过ZBP1依赖性坏死性凋亡导致肿瘤抑制。
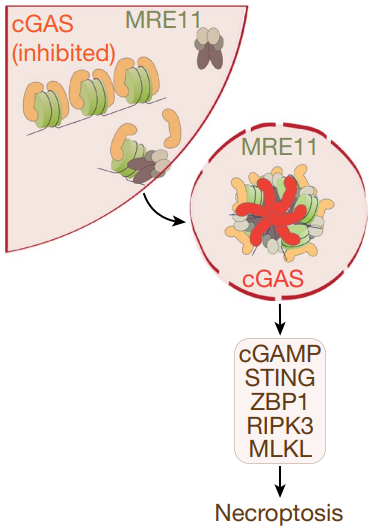
图1 MRE11介导肿瘤发生过程中cGAS和ZBP1依赖性坏死性凋亡的激活
2. 坏死性凋亡和胰腺导管腺癌
胰腺导管腺癌(PDAC)是一种毁灭性的癌症,即使在早期,也由于远处转移而预后不佳。福建医科大学胜利临床医学院Shi Chen团队发现与非转移性(T1M0)患者相比,早期肝转移T期(T1M1)患者的PDAC中MLKL的表达升高,坏死性凋亡途径增强[2]。从机制上讲,MLKL驱动的坏死性凋亡会招募巨噬细胞,增强肿瘤CD47的“不吃我”信号,并诱导巨噬细胞细胞外陷阱(MET)形成以激活CXCL8。CXCL8进一步启动上皮间质转化(EMT),上调ICAM-1表达以促进内皮粘附。MET还会降解细胞外基质,最终支持PDAC肝转移。同时,靶向坏死性凋亡和CD47可减少体内肝转移(图2)。这些结果表明坏死性凋亡通过逃避免疫监视促进PDAC转移,并表明CD47阻断联合MLKL抑制剂GW806742X可能是一种有前景的新辅助免疫疗法,可以克服T1M1困境,恢复根治性手术的机会。
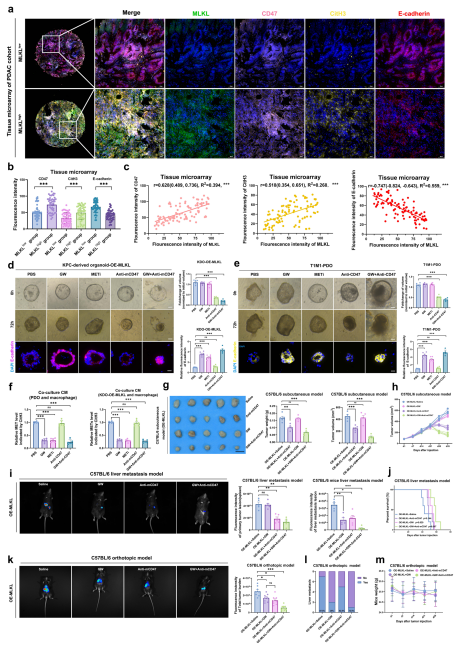
图2 GW联合抗CD47抑制T1M1-PDA的进展和转移
3. 坏死性凋亡和肝癌
坏死性凋亡在驱动代谢性肝病方面起主要作用,例如酒精性和非酒精性脂肪性肝炎,这些都是肝细胞癌发展的主要原因之一。德国杜塞尔多夫大学医院胃肠病、肝病和传染病科Tom Luedde团队发现了一种分子开关,促进肝细胞中两种替代性坏死性凋亡信号模式之间的重编程,从根本上影响免疫反应和肝癌发生[3]。肝细胞中伴随的坏死体和NF-κB激活,在生理上表达低浓度的RIPK3,不会立即导致细胞死亡,而是迫使它们进入长时间的“亚致死”状态,膜渗漏,充当分泌细胞,释放包括CCL20和MCP-1在内的特定趋化因子。这引发了肝细胞增殖以及原癌单核细胞衍生的巨噬细胞簇的激活,从而导致了肝癌的发生。相比之下,NF-κB信号失活的肝细胞中的坏死体激活导致坏死性凋亡的加速执行,从而预防了炎症和肝癌的发生(图3)。一致地,瘤内NF-κB坏死性凋亡特征与人类肝癌发生中的不良预后相关。因此,这些不同形式的坏死性凋亡之间的药理学重编程可能代表一种有前途的对抗肝细胞癌的策略。
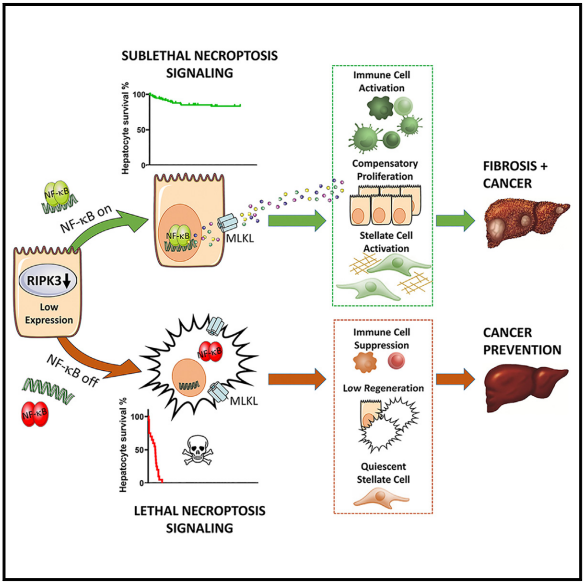
图3 亚致死性坏死凋亡信号促进炎症和肝癌
云克隆不仅可提供多种肿瘤实验动物模型,包括肿瘤移植动物模型、自发性肿瘤动物模型、诱发性肿瘤动物模型、肿瘤转移动物模型等,涵盖常见肿瘤研究。还具有各类癌症细胞系、癌症检测和坏死性凋亡相关指标及上述cGAS、STING、MRE11、RAD50、NBN、ZBP1、RIPK3、MLKL、ICAM-1、CD47、CXCL8、CCL20、MCP-1等相关产品,可助力广大科研工作者进行细胞凋亡与癌症相关研究。
指标 | 核心货号 | 指标 | 核心货号 |
cGAS | U056 | MLKL | R645 |
STING | N011 | ICAM-1 | A548 |
MRE11 | K113 | CD47 | B014 |
RAD50 | K111 | CXCL8 | A080 |
NBN | C679 | CCL20 | A095 |
ZBP1 | B552 | MCP-1 | A087 |
RIPK3 | E639 |
相关动物模型
皮下成瘤动物模型
建模方法:将标准条件下培养的处于对数生长期的HepG2细胞消化、离心,将所得的约5×106个细胞溶于0.1mLDMEM培养液,注射于裸鼠右侧背部皮下。

原位成瘤动物模型
建模方法:将标准条件下培养的处于对数生长期的HepG2-luc细胞消化、离心,将所得的约5×106个细胞溶于0.1mLDMEM培养液待用。麻醉小鼠,开腹暴露肝脏,用1ml胰岛素注射针取准备好的细胞注射于裸鼠肝脏内,用5-0丝线缝合伤口,活力碘消毒伤口,将裸鼠放在加热垫上,待清醒后正常饮食饲养。
参考文献
[1]Cho MG, Kumar RJ, Lin CC, et al. MRE11 liberates cGAS from nucleosome sequestration during tumorigenesis. Nature. 2024;625(7995):585-592. (IF=50.5)
[2]Liao CY, Li G, Kang FP, et al. Necroptosis enhances 'don't eat me' signal and induces macrophage extracellular traps to promote pancreatic cancer liver metastasis. Nat Commun. 2024;15(1):6043. (IF=14.7)
[3]Vucur M, Ghallab A, Schneider AT, et al. Sublethal necroptosis signaling promotes inflammation and liver cancer. Immunity. 2023;56(7):1578-1595.e8. (IF=25.5)