铁死亡:癌症治疗的新星?揭秘铁依赖细胞死亡机制如何成为抗癌新靶点
铁死亡,一种铁依赖性的脂质过氧化导致的细胞死亡方式,近年来在癌症研究中崭露头角。这种细胞死亡模式不同于传统的凋亡、自噬等机制,其核心在于细胞内铁离子和活性氧的积累,导致细胞膜脂质过氧化,最终破坏细胞结构,引发细胞死亡。癌症细胞由于快速增殖和对铁的高需求,往往更容易受到铁死亡的影响。研究表明,肿瘤细胞存在“铁成瘾”现象,即它们对铁离子的摄取和利用远高于正常细胞。这一特性使得铁死亡成为癌症治疗的一个潜在靶点。通过诱导铁死亡,可以有效地消灭癌细胞,而对正常细胞的影响较小。尽管目前大多数研究仍处于实验阶段,但铁死亡在癌症治疗中的应用前景令人期待,未来有望为癌症患者带来更为有效和个性化的治疗方案。
1. SLC13A3通过赋予细胞铁死亡抵抗性来破坏肿瘤免疫
免疫检查点阻断(ICB)触发肿瘤铁死亡。然而,大多数患者对ICB无反应。肿瘤可能在肿瘤微环境中(TME)逃避铁死亡。美国安娜堡密歇根大学医学院外科Weiping Zou团队发现SLC13A3是肿瘤细胞中的itaconate转运体,赋予肿瘤铁死亡抵抗力,降低肿瘤免疫力和ICB的有效性[1]。机制上,肿瘤细胞通过SLC13A3从肿瘤相关巨噬细胞(TAMs)摄取itaconate,从而激活NRF2-SLC7A11途径,逃避免疫介导的铁死亡(图1)。巨噬细胞中ACOD1(itaconate合成的必需酶)的缺失、肿瘤中SLC13A3的基因消融或抑制SLC13A3均使肿瘤对铁死亡敏感,抑制肿瘤进展,并增强ICB的有效性。这项研究揭示了SLC13A3-itaconate-NRF2-SLC7A11轴是肿瘤微环境中以前未被发现的免疫逃避机制,并发现SLC13A3是一个有潜力的抗癌靶点。
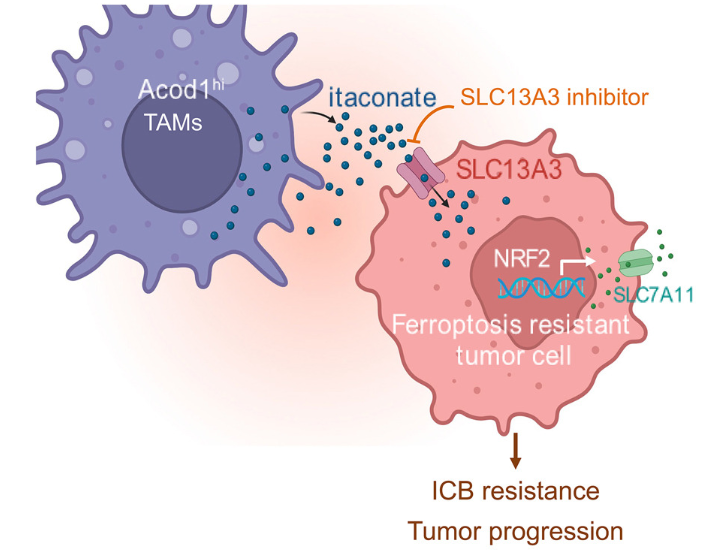
图1 SLC13A3通过赋予细胞铁死亡抵抗性来破坏肿瘤免疫
2. PD-1信号限制磷脂磷酸酶1的表达并促进肿瘤内CD8+ T细胞铁死亡
TME促进免疫细胞的代谢重编程和功能障碍。郑州大学第一附属医院生物治疗中心Yi Zhang团队研究了TME对CD8+ T细胞磷脂代谢的影响[2]。在肺癌中,与外周血CD8+ T细胞相比,肿瘤内CD8+ T细胞的磷脂酰胆碱(PC)和磷脂酰乙醇胺(PE)水平较低。肿瘤内CD8+ T细胞表达磷脂酰磷酸酶1(PLPP1)的量减少,该酶催化PE和PC的合成。T细胞特异性删除Plpp1会损害抗肿瘤免疫功能并通过铁死亡促进T细胞死亡。TME中的不饱和脂肪酸刺激Plpp1-/- CD8+ T细胞发生铁死亡。机制上,程序性死亡受体1(PD-1)信号在CD8+ T细胞中诱导GATA1结合Plpp1的启动子区域,从而抑制Plpp1的表达(图2)。PD-1阻断增加了Plpp1的表达并恢复了CD8+ T细胞的抗肿瘤功能,但未能挽救Plpp1-/- CD8+ T细胞的功能障碍。因此,PD-1信号调节CD8+ T细胞的磷脂代谢,这对免疫治疗具有治疗意义。
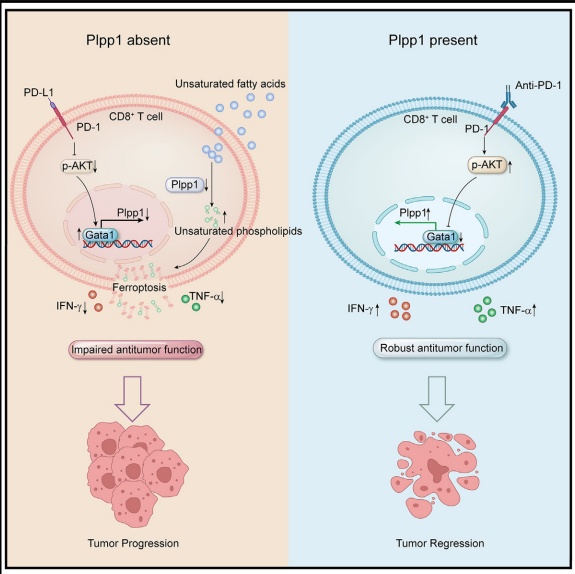
图2 PD-1信号限制磷脂磷酸酶1的表达并促进肿瘤内CD8+T细胞铁死亡
3. Zeb1通过调节脂质酶表达和磷脂组成介导肿瘤细胞EMT/可塑性相关的铁死亡敏感性
治疗抵抗和转移是癌症中最致命的两个步骤,通常是由上皮间质转化(EMT)程序的部分激活引起的。德国埃尔兰根-纽伦堡弗里德里希-亚历山大大学Nikolaus Fiebiger分子医学中心Thomas Brabletz团队发现,包括TGFβ刺激和获得性治疗抵抗在内的各种形式的EMT激活会增加癌细胞的铁死亡易感性,这取决于EMT转录因子Zeb1[3]。Zeb1通过调节关键酶甾醇酰-CoA脱氢酶1(SCD)、脂肪酸合成酶(FASN)、脂肪酸脱氢酶2(FADS2)、极长链脂肪酸5(ELOVL5)和长链酰基辅酶A合成酶4(ACSL4)的差异表达,增加了含有促铁死亡多不饱和脂肪酸(PUFA)的磷脂与具有细胞保护作用的单不饱和脂肪酸(MUFA)磷脂的比例(图3)。这些结果提示可以将铁死亡激活剂与SCD抑制剂联合应用于表达高水平Zeb1的侵袭性癌症的治疗。
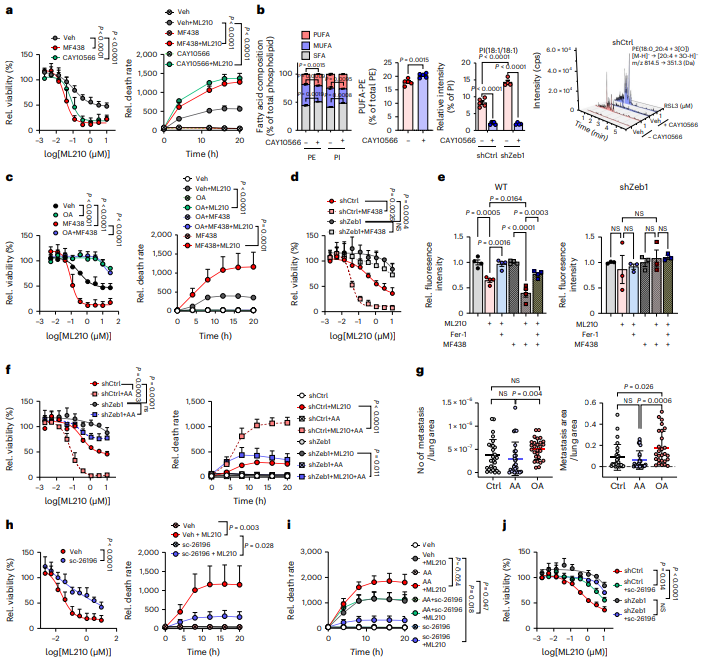
图3 抑制调节PUFA与MUFA比率的关键酶以Zeb1依赖的方式影响铁死亡敏感性
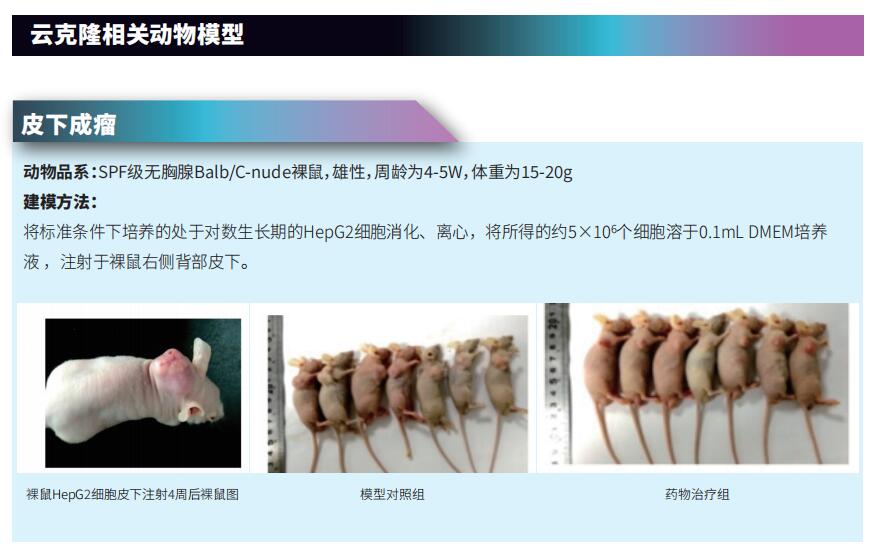
云克隆不仅可提供多种肿瘤实验动物模型,包括肿瘤移植动物模型、自发性肿瘤动物模型、诱发性肿瘤动物模型、肿瘤转移动物模型等,涵盖常见肿瘤研究。还具有各类癌症细胞系、癌症检测和铁死亡相关指标及上述NRF2、SLC7A11、GATA1、Zeb1、SCD、FASN、ACSL4等相关产品,可助力广大科研工作者进行铁死亡与癌症相关研究。
参考文献
[1]Lin H, Tison K, Du Y, et al. Itaconate transporter SLC13A3 impairs tumor immunity via endowing ferroptosis resistance. Cancer Cell. 2024;42(12):2032-2044.e6. (IF=48.8)
[2]Ping Y, Shan J, Qin H, et al. PD-1 signaling limits expression of phospholipid phosphatase 1 and promotes intratumoral CD8+ T cell ferroptosis. Immunity. 2024;57(9):2122-2139.e9. (IF=25.5)
[3]Schwab A, Rao Z, Zhang J, et al. Zeb1 mediates EMT/plasticity-associated ferroptosis sensitivity in cancer cells by regulating lipogenic enzyme expression and phospholipid composition. Nat Cell Biol. 2024;26(9):1470-1481. (IF=17.3)