红细胞程序性死亡机制新发现——NLRP3介导的血影蛋白依赖性细胞死亡
补体介导的成熟红细胞(RBCs)裂解会引发严重的溶血疾病。近期,第四军医大学西京医院的团队在《Cell》上发表了题为“Red blood cells undergo lytic programmed cell death involving NLRP3”的文章。本研究结果表明,补体激活可介导成熟红细胞中NLRP3-ASC-caspase-8复合物的组装,导致β-血影蛋白的水解以及细胞骨架完整性的破坏。从而诱导红细胞发生连续的形态变化,并导致溶血。
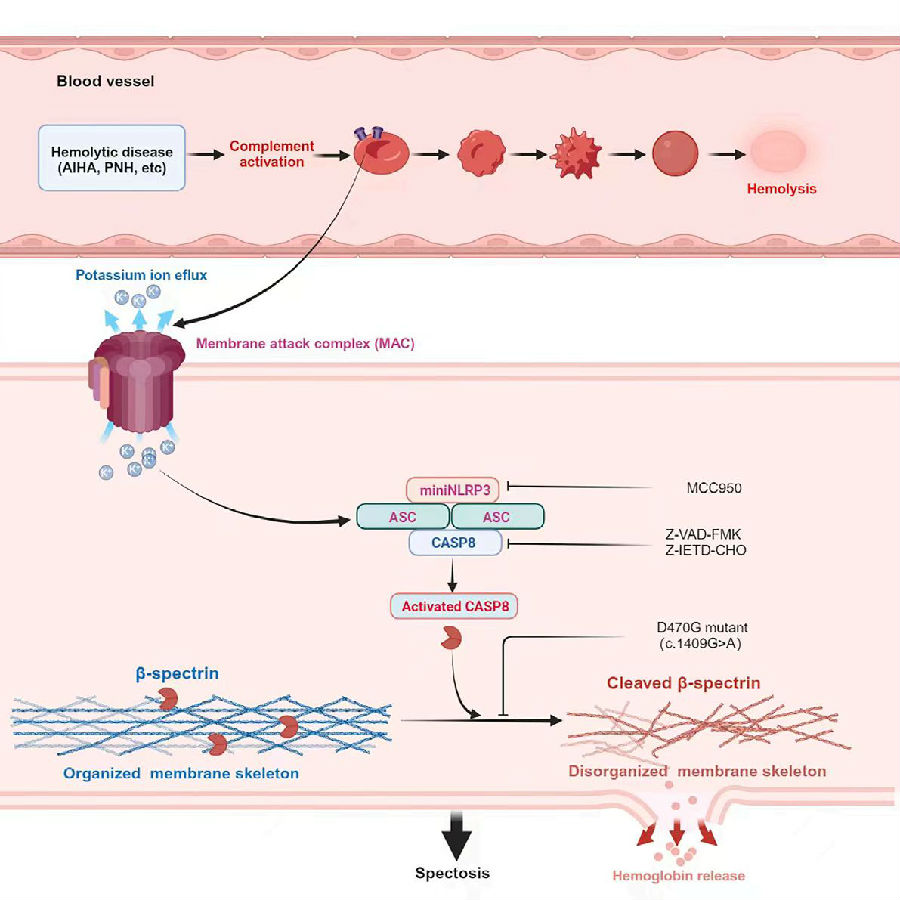
图1. 抑制NLRP3信号传导可减少补体诱导的红细胞程序性死亡
(图片源自《Cell》)
研究者首先收集了纯化的成熟人红细胞,并基于ABO血型激活补体建立了体外模型,以表征补体介导的溶血。与对照组相比,激活补体组上清液中游离血红蛋白(Hb)的浓度显著升高。并且在激活补体组中观察到了异形红细胞和红细胞影。这些发现表明补体激活介导了溶血。进一步通过扫描显微镜观察发现红细胞从圆盘状到影细胞的形态变化并非同步发生。但经补体刺激后,几乎所有的红细胞都会经历这种变形过程。伴随着这些形态变化,上清液中Hb的浓度相应增加。综合来看,这些发现表明,在补体诱导的溶血过程中,成熟红细胞会经历一系列形态变化,表明在溶血过程中人成熟红细胞的损伤可能涉及细胞程序性死亡。
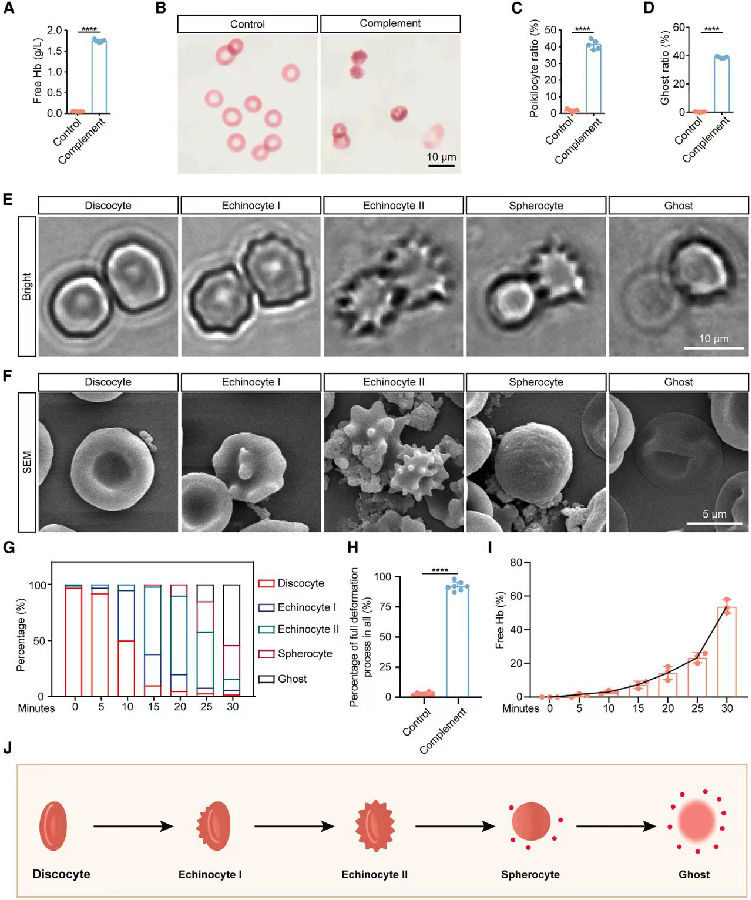
图2. 补体激活可诱导溶血过程中红细胞的一系列形态学变化
(图片源自《Cell》)
随后,研究人员给成熟红细胞施用了细胞焦亡、细胞凋亡、铁死亡和坏死性凋亡的抑制剂,以进一步探究补体诱导的成熟红细胞的程序性细胞死亡。值得注意的是,泛半胱天冬酶抑制剂显著降低了补体诱导的血红蛋白释放以及球形红细胞与影细胞的比例,这表明补体诱导的溶血可能主要依赖于半胱天冬酶的活性。接着,作者又用一系列半胱天冬酶抑制剂来确定是哪一种半胱天冬酶参与了溶血过程。结果表明,caspase-8抑制剂Z-IETD-FMK和caspase-3抑制剂Ac-DEVD-CHO均能有效抑制补体诱导的血红蛋白释放,并降低球形红细胞与影细胞的比例,且caspase-8抑制剂的抑制作用更显著。同时,作者在补体激活组中也检测到了caspase-8的激活。另外,在补体激活组红细胞中裂解的caspase-8信号逐渐增强;在棘形红细胞I型和II型以及球形红细胞中裂解的caspase-8的荧光强度显著高于圆盘形红细胞。这些数据表明,caspase-8活性是补体诱导的红细胞程序性死亡的主导者。
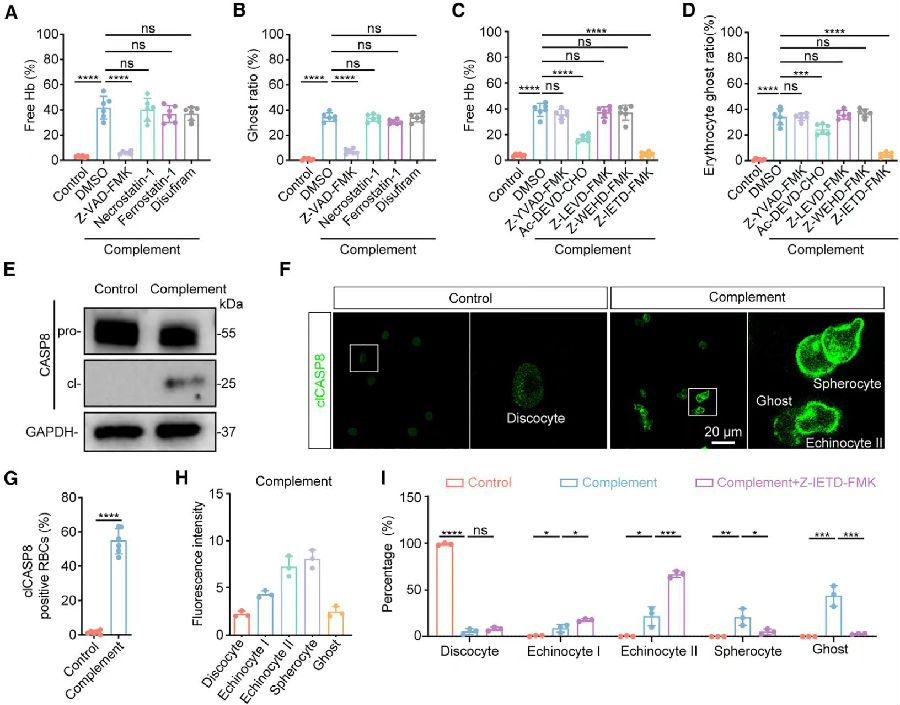
图3. 活化的caspase-8在补体诱导的红细胞死亡中起关键作用
(图片源自《Cell》)
有研究表明补体系统可激活巨噬细胞和T细胞中的NOD样受体热蛋白结构域相关蛋白3(NLPR3)炎性小体,且NLPR3-凋亡相关斑点样蛋白ASC复合物会利用caspase-8形成非经典的NLRP3复合物。基于此,作者假设成熟红细胞中被激活的NLPR3可能会激活caspase-8。观察到NLPR3抑制剂MCC950也降低了补体诱导的Hb的释放,并减少了人红细胞中球形红细胞与影红细胞的比例,这表明红细胞NLRP3参与了补体诱导的溶血。此外,MCC950处理显著减少了裂解的caspase-8阳性红细胞的数量,并减弱了caspase-8的激活。综上所述,这些结果表明激活的补体介导了成熟红细胞中NLRP3-ASC-caspase-8复合物的组装。
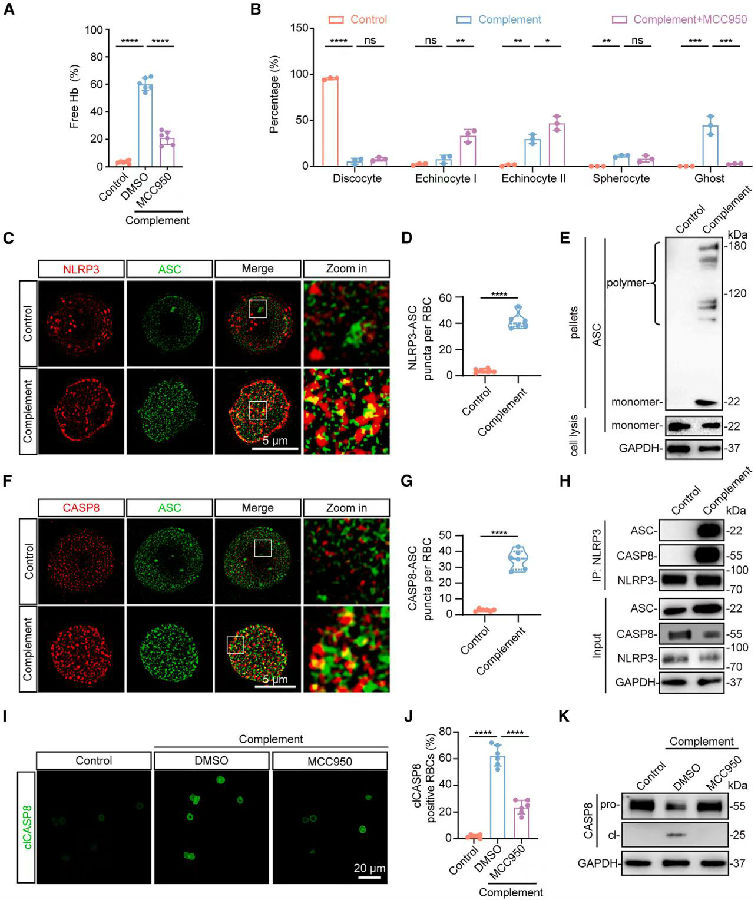
图4. 补体激活介导成熟红细胞中NLRP3-ASC-caspase-8复合物的组装
(图片源自《Cell》)
接下来,作者对补体激活红细胞组和对照组进行了蛋白质组学分析,基因本体论(GO)分析显示,与细胞骨架和肌动蛋白丝组装动力学相关的通路显著富集。鉴于血影蛋白是红细胞骨架的主要成分,作者推测血影蛋白可能是活化caspase-8的关键下游底物。而免疫印迹(WB)显示补体激活红细胞中的β-血影蛋白而非α-血影蛋白被切割。后面作者又通过caspase-8抑制剂预处理红细胞证明了抑制剂可阻止β-血影蛋白的切割。为了证明caspase-8和β-血影蛋白之间的相互作用,用活性caspase-8孵育红细胞影,发现β-血影蛋白被caspase-8有效切割。以上结果表明,NLRP3激活的caspase-8在补体诱导的红细胞死亡过程中介导β-血影蛋白的切割。
由于β-血影蛋白的N端包含一个与丝状肌动蛋白结合的结构域,β-血影蛋白裂解会导致其与丝状肌动蛋白的解离,从而造成红细胞细胞骨架网络的破坏。而作者也证实了补体激活组红细胞中β-血影蛋白与丝状肌动蛋白的共定位率显著低于对照组。用caspase-8抑制剂可显著恢复红细胞中的β-血影蛋白和丝状肌动蛋白的紊乱状态。同时,作者观察到caspase-8孵育的红细胞膜提取物的细胞骨架结构发生了变化,与补体处理后的变化相似。这些发现表明,β-血影蛋白的切割可直接导致红细胞膜完整性的丧失。
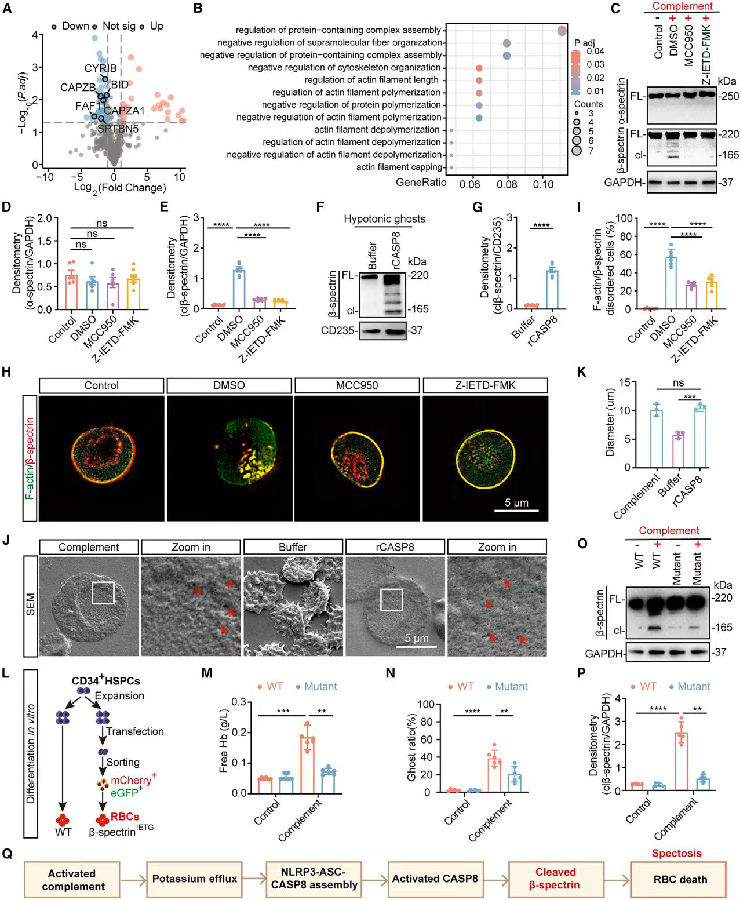
图5. NLRP3激活caspase-8引发红细胞中的β-血影蛋白裂解导致细胞骨架结构破坏
(图片源自《Cell》)
作者进一步在已建立的急性溶血性输血反应(AHTR)小鼠模型中进行了体内抑制剂给药实验。在输注血浆前,小鼠分别接受了PBS、MCC950和Z-IETD-FMK的预处理。结果表明,MCC950和Z-IETD-FMK处理均能显著减少血红蛋白尿的排泄,表明溶血得到了缓解。同时游离HB水平明显降低。此外,抑制剂处理显著提高了小鼠的生命力。与对照组相比,抑制剂处理组的棘形红细胞II、球形红细胞和影红细胞的比例降低,而圆盘形红细胞的比例增加。随后,作者又通过使用能抑制补体系统的合成肽Cp40对小鼠进行治疗。结果发现,Cp40的溶血治疗效果和前面两种抑制剂的效果相当。作者进一步同时用MCC950和Cp40进行治疗,发现联合用药效果比单独Cp40效果更佳。表明联合用药有显著的治疗潜力,阻断补体旁路途径和抑制补体活性有望用于治疗补体介导的溶血。
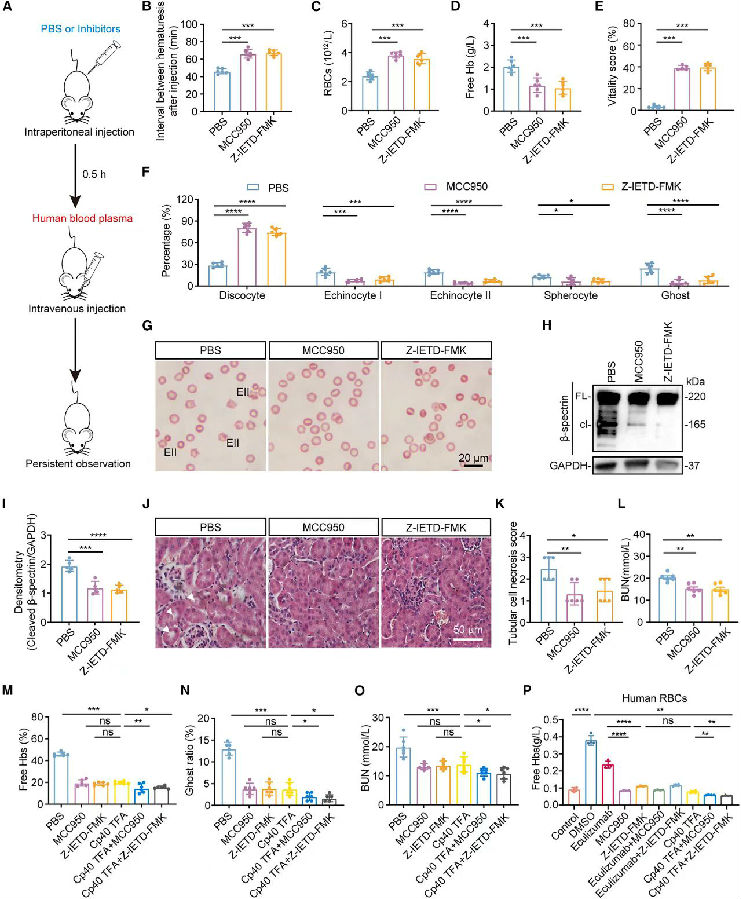
图6. 阻断补体激活信号可以减轻补体诱导的溶血
(图片源自《Cell》)
本研究揭示了成熟红细胞中的一种由β-血影蛋白控制的程序性死亡级联反应,为补体诱导的溶血相关的细胞内信号通路提供了进一步见解,这对溶血性疾病的治疗具有重要意义。
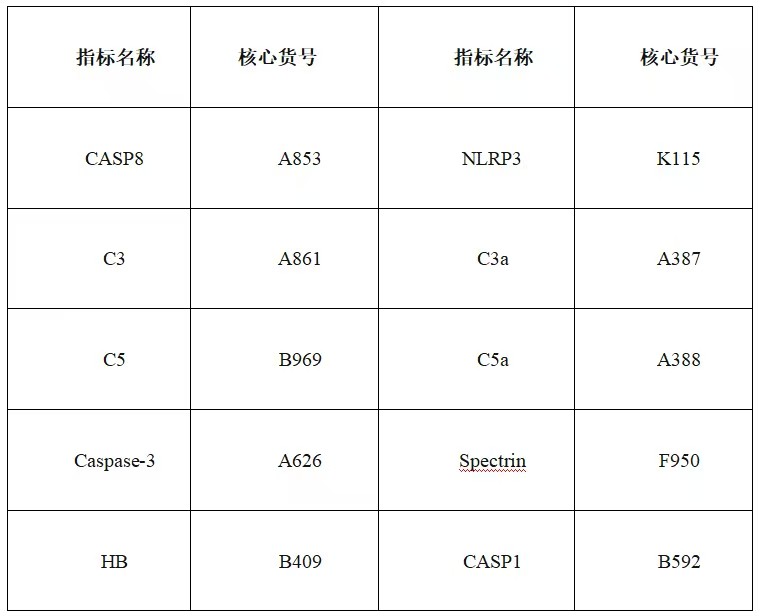
云克隆开发了上述研究中相关指标产品以助力科学研究,部分指标如下,供您参考: