成人海马体中竟然有正在增殖的神经祖细胞?!
神经细胞发育遵循神经干细胞→神经祖细胞→神经母细胞→成熟神经元的级联路径,但成年后仅特定脑区保留此能力。尽管科学家在成年啮齿动物上观察到海马等多个脑区的神经发生过程,但关于成人海马体中是否存在增殖的祖细胞一直存在争议。增殖的神经祖细胞和神经源性细胞的轨迹难以确定,理解成人海马体神经发展的环节缺失。2025年7月3日,有研究团队在《Science》期刊上发表了题为“Identification of proliferating neural progenitors in the adult human hippocampus”的文章,该研究通过单细胞RNA测序技术对人类从出生到成年不同年龄段的海马体进行了分析。确定了在早期的儿童中所有神经祖细胞的阶段。在成年人中,利用抗增殖标志物Ki67的抗体和机器学习算法,发现了增殖的神经祖细胞。此外,转录组数据表明神经祖细胞位于齿状回内。这些结果有助于理解成人的神经发展过程。
该文章研究思路如下:
一、儿童时期海马神经祖细胞的特征分析
为了在人类海马体中识别神经祖细胞,研究者首先将研究重点放在年龄在0 - 5岁的个体上。根据以往的研究数据,预期在这个群体中会发现大量的神经祖细胞。研究者对儿童组的海马核进行了snRNA-seq(Single-nucleus RNA sequencing),根据标志物表达情况手动注释主要细胞类型。得到两大聚类,一个主要由星形胶质细胞组成,另一个由颗粒神经元组成。这些聚类与中间神经祖细胞(intermediate neural progenitor cells,INPs)和神经母细胞有关,通过核表达细胞增殖标志物MKI67和/或EOMES连接起来。分析表明从表达INP标志物的细胞开始,依次表达神经母细胞标记物的细胞群,最终进入颗粒神经元簇,这表明存在神经发生谱系。通过Louvain聚类和标志物表达来描绘神经发生轨迹中的不同细胞阶段。发现INP和神经母细胞形成了独立的细胞簇,而潜在的神经干细胞则分散在星形胶质细胞簇中,并通过NESTIN、PAX6、ASCL1、SOX2 的共表达及S100β的低表达得以识别。潜在的未成熟神经元会表达颗粒神经元标志物PROX1、ST8SIA2、DCX以及低水平的GAD2。扩散图分析证实了从神经干细胞到增殖的INP细胞、神经母细胞和颗粒神经元的轨迹。通过差异基因表达分析,发现了一些在出生后神经发生过程中尚未得到充分研究的基因,但这些基因在人类的神经祖细胞和神经母细胞中含量丰富,如EZH2;或者在神经母细胞和未成熟神经元中含量丰富,如GLRA2、EPHA3、KCNH7和SEMA3C。(见图1)
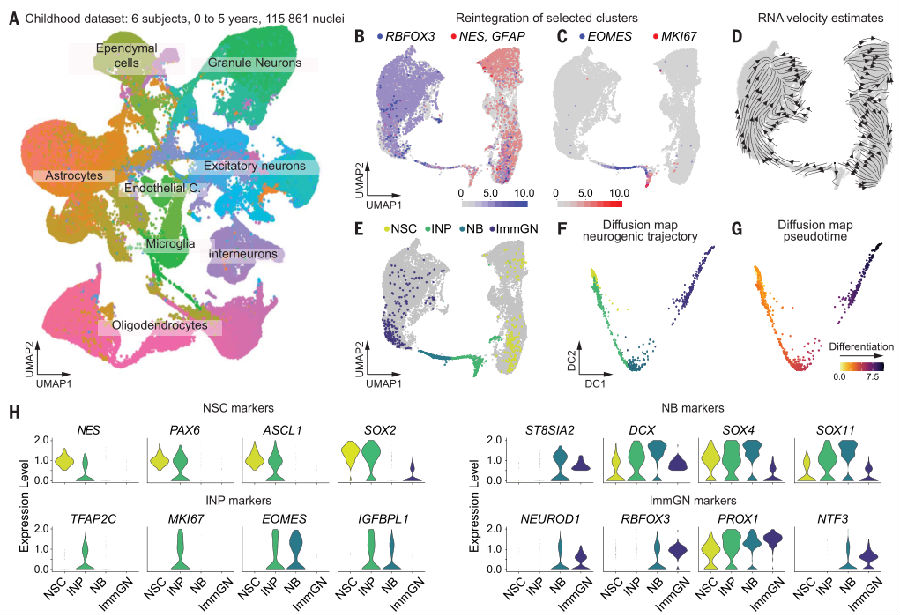
图1. 人类儿童时期海马体中神经生成轨迹的描绘
(图片来源于《Science》杂志)
二、年轻小鼠与人类神经祖细胞之间的相似性与差异性
研究者将人类儿童数据集与幼年小鼠海马体数据集进行了整合。几种细胞类型完全重合(如神经祖细胞和神经母细胞),而其他细胞类型则不同(如推定的神经干细胞和未成熟神经元),这表明物种之间在基因表达方面存在特定的细微差别。层次聚类显示神经祖细胞和神经母细胞与小鼠对应细胞更为相似,而与人类其他细胞类型相似度较低,这表明人类和小鼠神经发生细胞在转录水平上具有相似性。研究者评估了人类和小鼠神经发生轨迹上典型神经发生标志物的分布,并发现这两种物种中均有表达。然而,它们的动态变化在从干细胞发展到未成熟神经元的过程中有所不同。在小鼠中特异表达于神经祖细胞和神经母细胞的HES6在儿童海马体中的干细胞和神经祖细胞中有表达。在小鼠中特异表达于神经祖细胞的EOMES在人类的神经祖细胞和神经母细胞中有表达。(见图2)
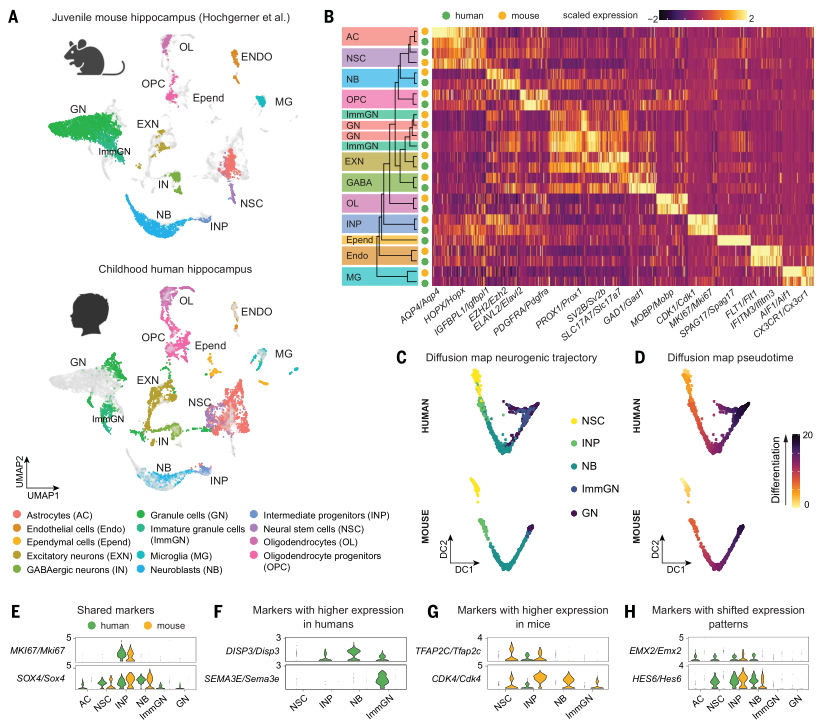
图2. 人类儿童期与幼年期小鼠海马体中神经祖细胞的比较
(图片来源于《Science》杂志)
三、神经祖细胞的富集与鉴定
为了确定青少年及成年人类海马体中的神经祖细胞,对19名年龄在13至78岁之间的个体的整个海马体或齿状回进行了snRNA-seq分析。在其中12名个体(20 至78岁)中,通过流式细胞术分选法富集了神经祖细胞。与儿童组数据整合后,形成了一个涵盖年龄范围从0岁到78岁个体的数据集。在这个数据集中,通过无偏聚类和人工标注的方式,识别出了所有主要的海马细胞类型。并通过对比测试幼年小鼠数据集证明了机器学习算法能够高特异、保守地识别出潜在的神经祖细胞,错误预测率很低,仅有0.37%。
四、青少年及成年人类海马体中的神经祖细胞
对青少年及成年人海马体的 snRNA-seq 数据集应用机器学习技术,共识别出354个祖细胞,根据其表达模式和聚类特征确定这些细胞为神经干细胞、神经祖细胞和神经母细胞。将此数据集与已发表的小鼠、猪和恒河猴海马体snRNA-seq 数据集相结合,以小鼠为参考,发现所有年龄段中被发现的人类神经组细胞,其发育轨迹与来自其他物种的神经组细胞完全一致。此外,还发现人类祖细胞表达的标记物与其他物种的神经祖细胞相似,但也有一些似乎是人类成人细胞特有的基因,如APOLD1和RRM2。在青少年和成年数据集中,大多数神经组细胞核处于细胞周期中(与儿童数据集中的22%相比,占70%)。与儿童期的增殖祖细胞类似,处于细胞周期的青少年/成年祖细胞除了表达MKI67这种增殖标志物外,还表达其他一些标志物,如TOP2A、CENPF、PCNA、MCM2及SMC4、HMGB2(这些属于神经祖细胞中的细胞周期基因),与细胞分裂相关。(见图3)
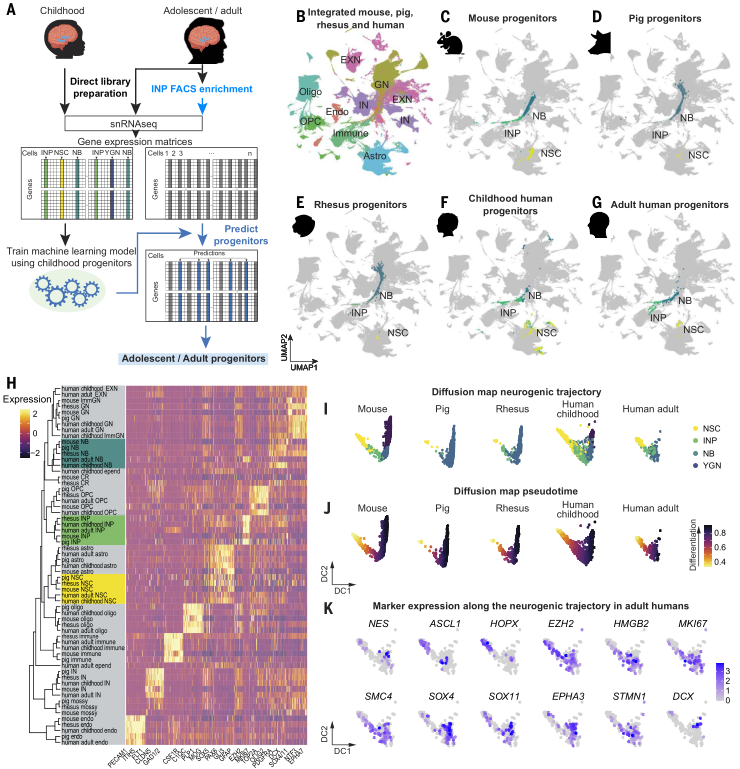
图3. 青少年/成年人大脑海马体中的神经祖细胞
(图片来源于《Science》杂志)
五、成人齿状回中神经祖细胞的空间定位
在齿状回中鉴定出了同时表达NESTIN、SOX2 和ASCL1的神经干细胞,表达 ASCL1、EOMES、SOX2、SOX11、EZH2和DCX 的INPs,及表达EZH2、EOMES、DCX、ST8SIA2、SOX11、IGFBPL1、ELAVL4、CALB2和STMN1的神经母细胞。还定位了表达新标志物的细胞,发现这些细胞在人类神经祖细胞中富集。此外,还发现那些同时表达神经发生相关标志物和增殖标志物(但不表达其他细胞类型标志物)的细胞,大多集中在齿状回和相邻的海马穹窿区域。(见图4)
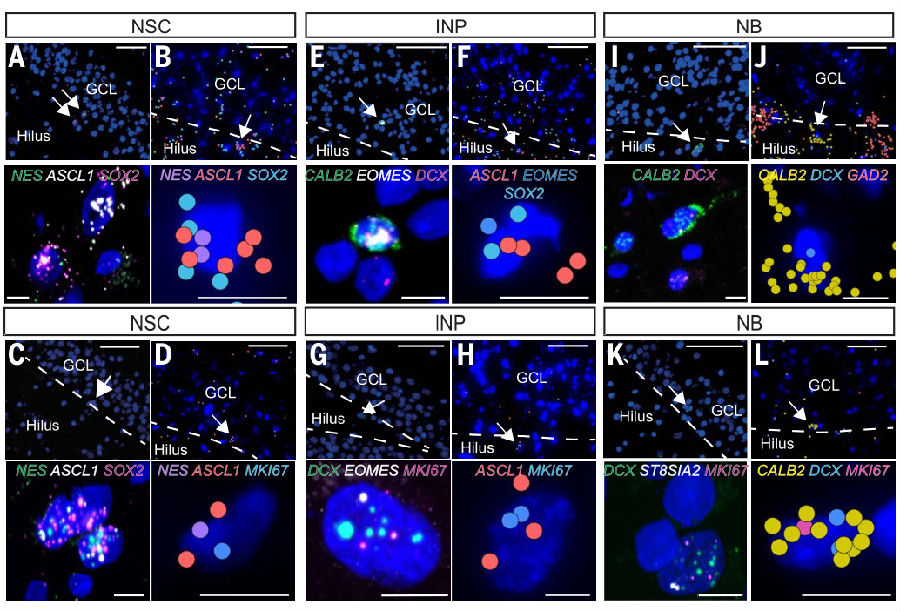
图4. 对具有空间分辨率的成人神经祖细胞及人类神经源性微环境的单细胞转录组学特征分析
(图片来源于《Science》杂志)
这篇研究报告了人类海马体中从出生到成年期间神经祖细胞的鉴定及分子特征。这些细胞在生命早期更为丰富且易于识别,而在青少年和成年人中则变得稀少,且存在显著的个体差异。其次,发现了神经祖细胞位于齿状回内,齿状回是海马体的主要通道,控制着信息从大脑皮层流向海马体本身的方式。使用了snRNA-seq的方法,用于分析单个细胞核中的基因活性,使用流式细胞术来研究细胞特性,并通过结合机器学习,识别神经元发育的不同阶段。通过捕获并描述增殖性神经祖细胞,描绘出了人类成人神经发生的完整细胞轨迹。这项研究揭示了大脑的终身可塑性,为神经退行性疾病和精神疾病的治疗提供了新思路。
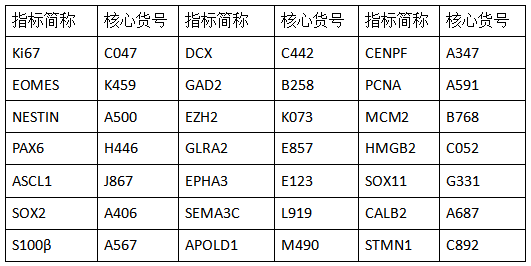
云克隆开发了与该研究相关的靶标产品,部分指标节选如下:
更多信息,欢迎访问:http://www.cloud-clone.cn/