解码细胞死亡“万花筒”
细胞死亡是所有细胞最终的宿命,细胞死亡的方式是生物医学领域的重大研究热点,涉及多种复杂的生物学机制。细胞死亡的主要功能是通过去除无功能、受损和有害的细胞来维持组织稳态。2005年第一届细胞死亡学术命名委员会对细胞死亡做出了较为清晰的定义,将细胞死亡定义为不同于濒死细胞的可逆细胞状态,死亡细胞是指细胞到达生命终点,处于不可逆转的状态。
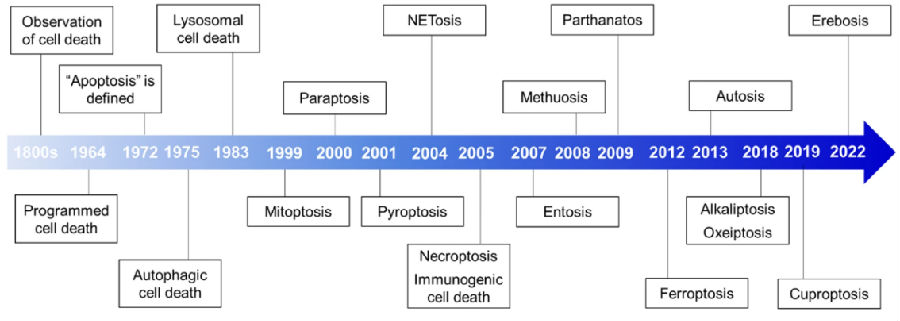
图1. 细胞死亡发现的时间点
一、细胞死亡的分类
细胞死亡主要有两种方式:坏死和程序性细胞死亡(PCD)。坏死是一种非程序性的细胞死亡形式,通常由创伤性损伤引起;PCD是一种受控的细胞死亡形式,由各种生理或发育信号引发的一系列分子事件导致。细胞凋亡是一种已被充分表征的PCD机制,其他类型的PCD,如:自噬性细胞死亡(autophagic cell death),溶酶体细胞死亡(lysosomal cell death),线粒体细胞凋亡(mitoptosis),副凋亡(paraptosis),焦亡(pyroptosis),NETosis,坏死性凋亡(necroptosis),免疫原性细胞死亡(immunogenic cell death),细胞套亡(entosis),代谢性胀亡(methuosis),PARP-1依赖性细胞死亡(parthanatos),铁死亡(ferroptosis),自噬性死亡(autosis)等。

图2. 细胞死亡的分类
二、细胞死亡的机制
1. 细胞凋亡
细胞凋亡的激活有两条主要途径:外源性和内源性途径。外源性途径由细胞外配体(TNF-α和Fas配体(FasL))与死亡受体结合激活,分别对应TNF和Fas受体。细胞外配体与死亡受体结合后,形成死亡诱导信号复合体(DISC),招募并激活启动caspase,如caspase-8和caspase-10。内源性途径由细胞内压力因子激活,如DNA损伤、氧化压力和生存信号的丧失,这导致线粒体外膜的通透性增加。这个途径由Bcl-2家族的抗凋亡蛋白(Bcl-2和Bcl-xL)、促凋亡蛋白(Bax和Bak)和BH3-only蛋白(Bim和Bid)调节。在应对细胞内压力时,促凋亡的BH3-only蛋白的激活抑制了抗凋亡蛋白,使Bax和Bak形成线粒体孔道并释放细胞色素c到细胞质中。释放的细胞色素c与凋亡蛋白酶活化因子-1(Apaf-1)形成凋亡体并激活caspase-9。

图3. 细胞凋亡的机制
2. 坏死性凋亡
坏死性凋亡(Necroptosis)是PCD的一种细胞裂解形式,并可导致炎症。主要通过RIPK1-RIPK3-MLKL信号通路介导,当caspase-8的活性被药物或病毒抑制剂阻断时,TNFR1、TLR等受体的刺激可诱导坏死性凋亡,涉及受体相互作用的丝氨酸/苏氨酸蛋白激酶1(RIPK1)的自磷酸化激活。RIPK1激活RIPK3,之后RIPK3磷酸化并激活下游MLKL(Mixed Lineage Kinase Domain-Like Protein),这是导致细胞膜裂解的坏死性凋亡的末端效应物,表现为细胞膜破裂和炎症因子的释放。尽管它具备凋亡的调控特性,但形态上呈现坏死特征。FASL、肿瘤坏死因子相关凋亡诱导配体(TRAIL)、TNF和Ⅰ型干扰素(IFN-1)分别激活各自的受体,招募MLKL、RIPK1和RIPK3,并通过磷酸化作用组装成坏死体(necrosome)。磷酸化介导的MLKL激活以及随后的MLKL介导的膜孔形成是坏死性凋亡的关键步骤。响应TNF-α诱导的坏死性凋亡,磷酸甘油酸变位酶5(PGAM5)被招募到外线粒体膜上的RIPK1/RIPK3复合物,激活动力蛋白相关蛋白1(Drp1)介导的线粒体断裂,并释放大量ROS,从而进一步激活多聚ADP核糖聚合酶1(PARP-1),导致NAD+水平下降并加剧该过程,这被认为是坏死性凋亡发生的必需步骤。

图4. 坏死性凋亡的机制
3. 自噬性细胞死亡
“自噬”来自希腊语“auto”,意思是吃或吞噬,描述了细胞分解和再利用自身成分以实现多种细胞功能的有序方式。自噬是体内自然发生的生理过程,通过合理分配资源和清除有害或无用物质来维持体内平衡,从而调节细胞生命周期和自然发育。然而,当细胞受到饥饿、氧化应激或任何有毒物质的影响时,自噬过程可能会失调,导致细胞死亡,即自噬性细胞死亡或II型细胞死亡。这种双重功能表明自噬在决定细胞命运中起着关键作用,它既可以作为一种生存机制,也可以在特定条件下驱动细胞死亡,具体取决于细胞环境和外部刺激。自噬的本质其实是细胞内的膜重排,自噬激活的第一步是形成隔离膜,或称自噬体,这是一种双膜结构,将细胞质成分隔离以进行降解。自噬过程的主要驱动因素是UNC-51样激酶1(ULK1)复合物,雷帕霉素靶蛋白(mTOR)通路是调节该复合物形成或抑制的重要途径。在正常情况下,mTOR的激活通过抑制ULK1复合物的形成来抑制自噬;但在应激或营养剥夺条件下,抑制mTOR导致ULK1复合物的形成,该复合物启动一种称为吞噬泡的双膜结构的形成,吞噬泡延伸并包裹细胞内成分,形成自噬体。然后与溶酶体融合形成自噬溶酶体,利用其酶消化细胞内成分。包括自噬相关基因(ATG)家族蛋白和Beclin-1在内的多种蛋白质在自噬过程中起着重要作用,它们参与吞噬泡的形成和自噬蛋白的募集。微管相关蛋白轻链 3(LC3)则参与吞噬泡的延伸、封闭和自噬体的成熟,自噬激活导致吞噬泡的形成,反过来又导致自噬性细胞死亡。

图5. 自噬性细胞死亡的机制
4. 溶酶体细胞死亡
溶酶体细胞死亡,即溶酶体依赖性细胞死亡(LCD),是由于溶酶体膜通透化,导致溶酶体酶释放到细胞质中并激活细胞死亡途径。LCD通常由活性氧(ROS)或其他外部刺激触发。ROS的激增是导致钙离子浓度升高的主要因素之一,这一过程通过瞬时受体电位通道M2型(TRPM2)通道的过度激活和溶酶体中钙离子的外流来实现,进而诱发溶酶体膜破裂(LMP)和溶酶体蛋白酶(如cathespins)释放到细胞质中。溶酶体蛋白酶催化多种底物的降解,包括Bid和凋亡蛋白,进而启动依赖caspase的细胞死亡途径。此外,LCD的发生还涉及Ca2+依赖的腺苷酸环化酶1(ADCY1)激活,随之而来的是环磷腺苷(cAMP)的增加,最终抑制溶酶体酸性鞘磷脂酶(SMase)的活性。同时,内质网应激也能引起细胞质内Ca2+浓度升高。过量的细胞质钙刺激钙蛋白酶(calpain)激活,导致溶酶体膜蛋白(如LAMP1/2)的降解,进而引发溶酶体膜的破裂,最终导致LCD。
 图6. 溶酶体细胞死亡的机制
图6. 溶酶体细胞死亡的机制
5. 免疫原性细胞死亡
免疫原性细胞死亡(ICD)是一种PCD类型,是调节性细胞死亡(RCD)的一种,一种足以在具有免疫能力的宿主中激活适应性免疫的细胞死亡方式。ICD可由一组有限的刺激引起,包括病毒感染、一些FDA批准的药物(蒽环类药物等)、特定形式的放疗和光动力治疗等。当死亡细胞释放损伤相关分子模式(DAMPs)时,会引发免疫反应,这些DAMPs吸引免疫细胞到细胞死亡的部位。在ICD过程中,死亡的肿瘤细胞在其表面表达钙网蛋白(Calreticulin,CALR),这作为“吃我”信号作用于树突状细胞(DCs)和其他吞噬细胞。这种信号促进DCs吞噬死亡细胞,从而激活免疫反应。DAMPs包括细胞表面暴露的CALR和热休克蛋白(Heat Shock Proteins,HSPs)、以及细胞外释放的三磷酸腺苷(ATP)、高迁移率族框1(HMGB1)等。这些DAMPs可以作为危险信号,被先天免疫系统的模式识别受体(Pattern Recognition Receptors,PRRs)所识别,如Toll样受体(TLRs)和NOD样受体(NLRs),从而激活抗肿瘤免疫反应。

图7. 免疫原性细胞死亡的机制
6. 碱死亡
碱死亡(Alkaliptosis)是一种由细胞内pH升高引发的PCD。碱死亡通常由NF-κB激活引发,导致碳酸酐酶9(CA9)的下调或ATP酸性H+转运V0亚基D1(ATP6V0D1)的上调,进而破坏溶酶体pH平衡。CA9作为一种维持pH平衡的酶,通过催化二氧化碳的可逆水合反应,促进碳酸氢盐离子和质子穿过细胞膜。当CA9被过度下调时,受损的H+流出可激活其他转运体或调节器以调高细胞内pH水平作为适应性反应。这种碱化破坏了细胞内稳态并可激活诱导细胞死亡的信号通路。

图8. 碱死亡的机制
7. 氧死亡
氧死亡(Oxeiptosis)一种不依赖caspase的细胞凋亡样死亡途径,于2018年首次提出的一种非典型的氧化应激诱导的细胞死亡,具有非发炎性的特征,且与KEAP1-PGAM5-ASK1信号通路密切相关。在氧化应激条件下,细胞内ROS水平的升高引发KEAP1(Kelch样ECH相关蛋白)的构象变化,从而促使其与NRF2解离。KEAP1随后转运至线粒体,介导AIF(凋亡诱导因子)从PGAM5(磷酸甘油酸变位酶家族成员5)的释放,并促进AIF向细胞核的转运。在细胞核内,AIF的S116位点被去磷酸化,进而引发细胞死亡。

图9. 氧死亡的机制
8. 细胞焦亡
细胞焦亡(Pyroptosis)是一种涉及炎症并由caspase 1介导的PCD,通常由细胞内炎症小体的激活引发,导致细胞膜破裂并释放促炎因子,广泛存在于感染和免疫反应过程中。在响应病原体相关分子模式(PAMPs)或损伤相关分子模式(DAMPs)的作用下,细胞质中的经典炎症小体(如NLRP3、NLRP1、NLRC4、AIM2等)响应微生物感染(如微生物毒素等)或危险信号(如双链DNA和结晶等)激活caspase 1,而非经典炎症小体则直接响应LPS或其他刺激激活caspase 4/5/11。炎症caspase被激活后,pro-IL-1β、pro-IL-18和GSDMD被切割,释放出N端的GSDMD(GSDMD-N),后者在细胞膜上形成孔洞,进而释放炎症介质(如IL-1β、IL-18等)。除此之外,Pyroptosis的其他途径还包括caspase 3、caspase 8和caspase 9的激活,以及gasdermin E、B和C(分别为GSDME、GSDMB和GSDMC)的切割。此外,钠离子进入细胞并带入水分,导致细胞体积膨胀。随着这一过程的持续,细胞膜可能无法承受增大的压力,从而导致膜破裂。膜破裂后,所有剩余的可溶性细胞质内容物会迅速被释放,几乎是瞬时发生的,从而最终导致Pyroptosis。

图10. 细胞焦亡的机制
9. 铁死亡
铁死亡(ferroptosis)是一种铁依赖的涉及脂质过氧化物和氧化应激积累,导致膜损伤的PCD。
铁死亡由脂质过氧化物的积累引发,这些脂质过氧化物是通过脂氧合酶或其他酶氧化多不饱和脂肪酸产生的。脂质过氧化物通过多不饱和脂肪酸的氧化积累,这个过程可以通过铁催化的芬顿反应进一步放大,生成ROS和羟基自由基,这些自由基会攻击和破坏细胞成分,特别是细胞膜,导致细胞死亡。铁死亡的特点是细胞内谷胱甘肽(GSH)的耗竭和谷胱甘肽过氧化物酶4 (GPX4) 活性的降低,导致未代谢的脂质过氧化物的积累和高水平ROS的产生。

图11. 铁死亡的机制
10. NETosis
NETosis是中性粒细胞的一种炎性细胞死亡方式,通过释放网状结构的中性粒细胞外陷阱(NETs)来捕捉并杀死病原体。特征是NETs释放到细胞外空间,NETs是由染色质、组蛋白和颗粒蛋白组成的网状结构。NETosis中的一个关键事件是NADPH氧化酶复合物的激活,这依赖于细胞质中Ca2+浓度的增加和随后的ROS生成。过量的ROS导致细胞质颗粒降解,并促使中性粒细胞弹性蛋白酶(NE)、髓过氧化物酶(MPO)和肽基精氨酸脱亚胺酶4(PAD4)释放到细胞核中,导致染色质去凝聚和核膜解体。另一个重要的因素是PAD4从细胞质转移到细胞核,催化组蛋白的去甲基化,导致染色质去凝缩。在NETosis的最终阶段,质膜上形成孔洞,染色质释放到细胞外环境,形成NETs。

图12. NETosis的机制
11. Parthanatos
Parthanatos是一种由聚ADP-核糖聚合酶(PARP)激活介导的PCD,特征是PAR聚合物积累、AIF释放,最终导致DNA片段化。由多种因子触发,如ROS、过氧化氢、电离辐射和烷基化剂。当DNA损伤较轻时,PARP-1 招募DNA损伤修复蛋白来修复受损的DNA。严重的 DNA损伤导致PARP-1过度激活和PAR聚合物的形成。积累的PAR聚合物与AIF 结合并介导AIF从线粒体的释放。AIF与巨噬细胞迁移抑制因子(MIF)互动形成AIF/MIF复合物,该复合物被转运到细胞核,导致DNA降解并引发Parthanatos。

图13. Parthanatos的机制
12. 铜死亡
铜死亡(cuproptosis)是一种由铜触发的PCD形式,其特征是由于脂酰化线粒体酶聚集和铁硫中心蛋白丧失引起的线粒体应激。过量的铜对细胞和组织有毒性,导致一种称为铜超载或铜毒性的状况。线粒体基质还原酶铁氧还蛋白1(FDX1)催化ES-Cu2+还原为Cu+,将其释放到线粒体中。FDX1还被鉴定为一种新型的脂酰化效应物,促进有毒的脂酰化二氢脂酰胺S-乙酰转移酶(DLAT)的积累,随后引发铜死亡。这种细胞死亡依赖于细胞中的铜含量和三羧酸(TCA)循环酶的脂酰化状态。

图14. 铜死亡的机制
13. 双硫死亡
双硫死亡(disulfidptosis)是一种由双硫键失衡引发的细胞死亡,核心机制始于葡萄糖饥饿导致的NADPH耗竭,由此引发细胞内还原能力崩溃,无法维持蛋白质巯基的还原状态。关键步骤是SLC7A11高表达细胞通过大量摄取胱氨酸,因其无法被还原而在肌动蛋白细胞骨架等富含胱氨酸的蛋白间形成异常二硫键,直接导致肌动蛋白丝交联、收缩和崩解,最终引发细胞失粘附而死亡。这一过程独立于已知的凋亡、坏死性凋亡、焦亡和铁死亡通路,其独特之处在于二硫键应激直接破坏了细胞骨架结构。

图15. 双硫死亡的机制
三、细胞死亡的相关蛋白
1. 细胞凋亡主要相关蛋白
蛋白质 | 作用 | 云克隆检测试剂核心货号 |
Annexin V | 检测细胞凋亡早期脂质双层的变化 | A259 |
Cytochrome C
| 关键调控因子,其释放到细胞质中可以引发一系列的信号级联反应 | A594 |
Caspase 3 | 凋亡的最终执行者 | A626 |
Bax、Bak、Bad、Bid、Bim等 | 促凋亡因子 | B343、C324、C337、A629、Q166 |
Bcl-2、Bcl-xL等 | 抗凋亡因子 | A778、E582 |
2. 坏死性凋亡主要相关蛋白
蛋白质 | 作用 | 云克隆检测试剂核心货号 |
TNFα
| 最主要的上游信号元件
| A133 |
Caspase-8
| 在caspase-8受到抑制时发生 | A853 |
RIPK1、RIPK3和MLKL
| 关键蛋白RIPK1、RIPK3 和 MLKL的磷酸化状态是识别坏死性凋亡的重要步骤 | E640、E639、R645 |
3. 自噬性细胞死亡主要相关蛋白
蛋白质 | 作用 | 云克隆检测试剂核心货号 |
LC3 | LC3-Ⅱ/Ⅰ的比值变化评估自噬的强弱 | L701、L702、P423 |
mTOR | 诱导自噬的重要调节分子 | B806 |
ATG家族,如Atg1/4/5/7/10/12/13等 | 调节和执行的关键蛋白 | L221、L222、L223、L224
|
4. 溶酶体细胞死亡主要相关蛋白
蛋白质 | 作用 | 云克隆检测试剂核心货号 |
Cathepsin B/D | 切割多种细胞底物,引发死亡信号 | C964、B280 |
5. 碱死亡主要相关蛋白
蛋白质 | 作用 | 云克隆检测试剂核心货号 |
NF-κB | 激活引发 | B824 |
CA9 | 维持pH平衡的酶,下调可破坏溶酶体pH平衡 | D076 |
6. 氧死亡主要相关蛋白
蛋白质 | 作用 | 云克隆检测试剂核心货号 |
核心KEAP1-PGAM5-ASK1信号通路 | L648、R880、B358 |
7. 细胞焦亡主要相关蛋白
蛋白质 | 作用 | 云克隆检测试剂核心货号 |
Caspase 1
| 活化的Caspase 1一方面切割GSDMD,形成含有GSDM-NT活性域的肽段,诱导细胞膜穿孔,细胞破裂,释放内容物,引起炎症反应;另一方面,对IL-1β和IL-18前体进行切割,形成有活性的IL-1β和IL-18,并释放到胞外,募集炎症细胞聚集,扩大炎症反应 | B592 |
NLRP3、NLRP1、NLRC4、AIM2、IPAF等 | 炎症小体 | K115、K117、L954、G302、L954 |
Caspase 4/5/11 | 活化的Caspase 4/5/11可以裂解GSDMD蛋白,GSDMD蛋白N端可以介导细胞膜溶解与细胞焦亡;另一方面,活化的Caspase 4/5/11激活NLRP3炎症小体来活化Caspase 1,最终产生IL-1β和IL-18并外释 | B735、A770 |
8. 铁死亡主要相关蛋白
蛋白质 | 作用 | 云克隆检测试剂核心货号 |
GPX4 | 控制铁死亡的核心 | C994
|
Tf、FTH1、FTL | C036、D021、D020
| |
FPN1 | 介导的铁外流和外泌体介导的铁蛋白输出会抑制铁死亡 | C489
|
9. NETosis主要相关蛋白
蛋白质 | 作用 | 云克隆检测试剂核心货号 |
NE、MPO | 释放到细胞核中致使染色质去凝聚和核膜解体 | A181、A601 |
10. Parthanatos主要相关蛋白
蛋白质 | 作用 | 云克隆检测试剂核心货号 |
PARP-1 | 参与DNA修复的重要核酶 | A279 |
AIF、MIF | 导致DNA降解并引发Parthanatos | B064、A698 |
11. 铜死亡主要相关蛋白
蛋白质 | 作用 | 云克隆检测试剂核心货号 |
DLAT
| 表达量变化影响铜死亡的发生 | A696
|
FDX1
| Cu2+还原成更加具有毒性的Cu+,释放到线粒体中 | C475 |
12. 双硫死亡主要相关蛋白
蛋白质 | 作用 | 云克隆检测试剂核心货号 |
SLC7A11 | 将胞外胱氨酸装运到细胞内,当细胞存在SLC7A11高表达时,会引起胱氨酸摄取增加,进而引起NADPH供应不足,最终可能导致细胞死亡 | E410
|
GLUT1 | 葡萄糖的摄取及转运 | B185 |
细胞死亡是由一系列关键蛋白精确调控的主动程序性过程,其核心执行分子如caspase家族、RIPK、MLKL及Gasdermin家族等的激活与相互作用,共同决定不同死亡方式的命运走向。这些细胞死亡途径不仅在正常生理过程中发挥重要作用,还与多种疾病的发生和发展密切相关。
云克隆助力细胞死亡相关研究,为广大科研人员提供相关检测试剂产品,相关靶标核心货号如下:
靶标 | 核心货号 | 靶标 | 核心货号 | 靶标 | 核心货号 |
TNFa | A133 | FasL | A031 | Drp1 | C404 |
CASP8 | A853 | CASP10 | B161 | LAMP2 | B464 |
Bcl2 | A778 | Bcl-xL | E582 | Beclin 1 | J557 |
Bax | B343 | Bak | C324 | HMGB1 | A399 |
Bim | Q166 | Bid | A629 | IL1b | A563 |
CYCS | A594 | CASP9 | A627 | LAMP1 | B441 |
Apaf1 | B054 | CASP3 | A626 | CALR | B486 |
CASP7 | A449 | TNFR1 | B499 | NF-κB | B824 |
RIPK1 |