星形胶质细胞CCN1稳定成人大脑的神经回路
大脑如何从“可塑”变“稳定”?《Nature》研究揭秘关键蛋白的维稳作用
星形胶质细胞CCN1稳定成人大脑的神经回路
大脑在发育关键期具有较高的可塑性,而成年期则转向稳定以维持回路功能。星形胶质细胞如何参与这一转变此前尚不明确。近日,美国研究团队在《Nature》上发表了题为“Astrocyte CCN1 stabilizes neural circuits in the adult brain”的文章。该研究揭示了星形胶质细胞通过分泌因子CCN1在调控大脑感觉回路可塑性与稳定性中的关键作用。研究发现星形胶质细胞释放的CCN1能促进抑制性神经元成熟、少突胶质细胞分化及髓鞘形成,从而在成年视觉皮层中维持突触与回路的稳定。相反,敲除CCN1会导致回路失稳。这表明成年大脑回路的特性需要星形胶质细胞持续的主动维持,CCN1通过协调多种细胞类型的成熟状态成为回路稳定性的核心调控因子。
首先,研究者使用小鼠视觉皮层作为模型来研究星形胶质细胞如何调节回路稳定性。为了确定参与限制视觉皮层可塑性和维持稳定性的星形胶质细胞因子,研究者利用Ribo Tag技术对发育关键期和成年期小鼠的星形胶质细胞进行了mRNA测序,对星形胶质细胞在高稳定性与高可塑性时期和可塑性诱导后的转录谱进行了分析。研究发现,在众多稳定期和关键期差异表达基因中Ccn1是一种可能的促稳定因子,其在成年期表达较高,而在黑暗饲养和单眼剥夺后表达下调。研究者后续通过单分子荧光原位杂交(smFISH)技术对不同年龄和可塑性范式下的视觉皮层星形胶质细胞中的Ccn1进行了表征,发现Ccn1在星形胶质细胞中的表达随发育逐渐升高,并在成年期维持高水平,而在可塑性诱导条件下表达降低。这一表达模式表明,星形胶质细胞来源的CCN1很可能在限制可塑性和维持成年回路稳定性中发挥重要作用。
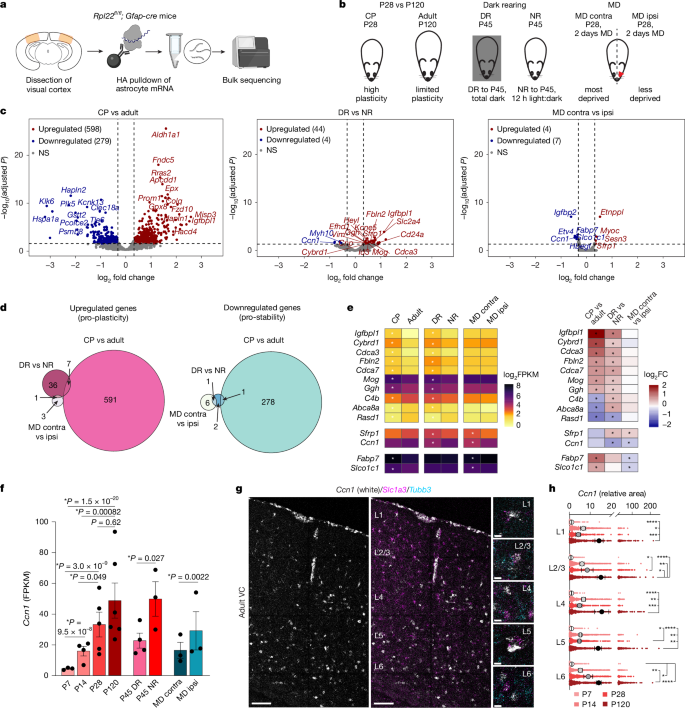
图1. 小鼠视觉皮层星形胶质细胞促稳定因子CCN1的鉴定
(图片源自《Nature》)
为了验证星形胶质细胞分泌的CCN1是否具有稳定神经回路的作用,研究人员分别在发育关键期和成年期对小鼠进行CCN1的过表达或条件性敲除实验。结果发现,在通常可塑性高的关键期过表达CCN1,能显著抑制视觉回路的可塑性;而在可塑性本已很低的成年期过表达CCN1,则没有额外效果。相反,在成年期特异性敲除星形胶质细胞的CCN1,会导致视觉回路稳定性下降,可塑性重新增强。这些结果表明,CCN1是一种由星形胶质细胞分泌的、以年龄依赖性方式主动维持成年期神经回路稳定性的关键因子。
接着,研究者在关键期对小鼠视觉皮层神经元进行了电生理记录,以探究CCN1是否通过调节突触功能来稳定神经回路。实验发现,过表达CCN1会降低锥体神经元上基础兴奋性突触传递的频率,而单眼剥夺可以逆转CCN1引起的这种兴奋性传递降低。这些结果表明,CCN1可能是通过特异性地降低神经元的兴奋性驱动,从而限制回路的可塑性并促进其稳定。
随后,研究人员在关键期过表达CCN1,以探明CCN1如何调节抑制性神经元的成熟。结果发现,CCN1过表达能增加抑制性神经元接收的兴奋性输入,促进其周围致密细胞外基质的形成,并使小胶质细胞趋向于静息状态,从而减少其吞噬活性。这些变化共同表明,星形胶质细胞来源的CCN1能通过促进抑制性神经网络的成熟和改变细胞外基质及免疫微环境,共同推动视觉回路在发育关键期结束后进入稳定状态。
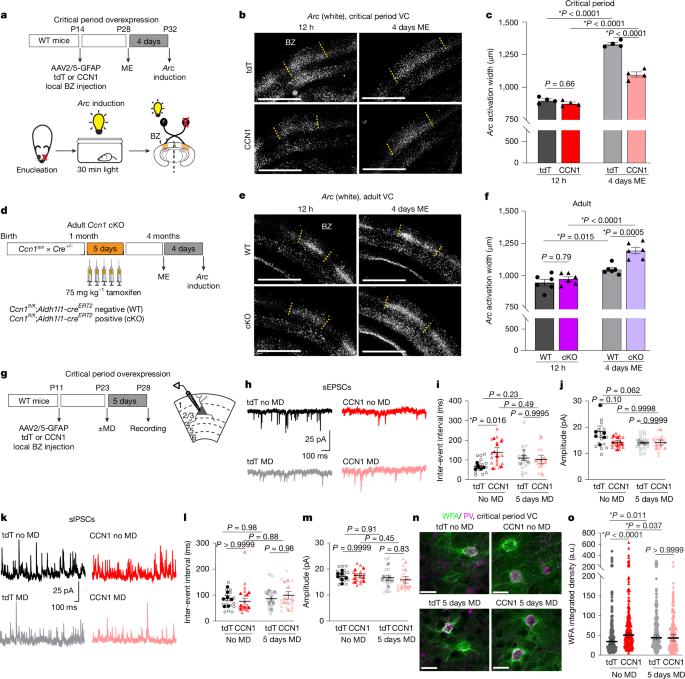
图2. CCN1调节双眼区重塑和突触兴奋
(图片源自《Nature》)
为探究星形胶质细胞分泌的CCN1蛋白对维持成年视觉回路功能是否必需,本研究通过双光子体内钙成像技术,在成年野生型和星形胶质细胞特异性敲除CCN1(Ccn1-cKO)小鼠中进行了单眼剥夺实验。结果表明,Ccn1-cKO小鼠的双眼回路在基础状态下即呈现不成熟特征,表现为对侧眼响应神经元比例偏高、双眼响应神经元比例偏低。更重要的是,成年CCN1敲除小鼠在经历单眼剥夺后,其眼优势指数并未像野生型小鼠那样发生正常偏移,且其回路对剥夺的反应模式发生改变,表明可塑性调控异常。行为学实验进一步证实,这种回路变化导致了深度感知能力的缺陷。这些结果共同证明,星形胶质细胞来源的CCN1是维持成年期双眼回路稳定性与正常功能的必需信号。
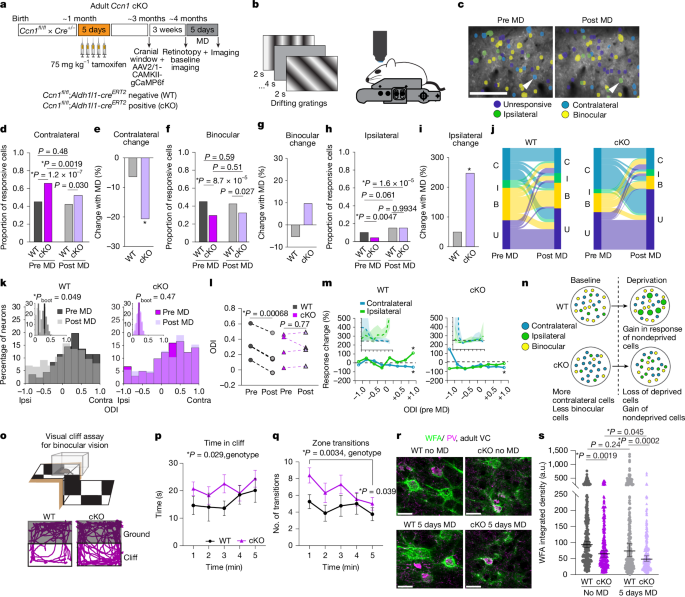
图3. 星形胶质细胞CCN1维持双眼回路
(图片源自《Nature》)
为阐明CCN1的作用机制,研究者聚焦于其与整合素的相互作用。利用一个特异性破坏CCN1与αVβ5/αVβ3整合素结合的单点突变体CCN1(D125A)进行研究。结果显示,在幼年小鼠视觉皮层过表达该突变体,未能再现野生型CCN1抑制视觉剥夺后大规模回路重塑的效应。这表明CCN1通过与αVβ3/αVβ5整合素结合来限制可塑性。进一步分析其对神经元周围网络的影响发现,突变体虽能像野生型一样增加整体神经元周围基质网络(PNNs)的密度,却无法特异性上调PNN中调控可塑性的关键成分----聚集蛋白聚糖。这些结果提示,CCN1通过整合素依赖和依赖的不同机制调控PNN的不同组分,而其整合素结合能力对其调节聚集蛋白聚糖和抑制可塑性至关重要。
随后,研究者通过对关键期对照组(tdT-OE)或处理组(CCN1-OE)小鼠视觉皮层中的所有细胞类型进行了单核RNA测序(snRNA-seq),差异表达基因分析发现,Hippo通路负调控因子Ddx5在多类细胞中普遍下调,提示CCN1能直接向多种细胞发出信号。进一步的细胞类型影响排序(AUGUR)揭示,兴奋性神经元和少突胶质细胞是受CCN1过表达影响最显著的细胞类型。在兴奋性神经元中,许多差异表达基因与突触结构与功能相关,与此前观察到的电生理变化相符。这些数据共同表明,星形胶质细胞分泌的CCN1能够广泛影响神经微环境,并特别促进少突胶质细胞的成熟。
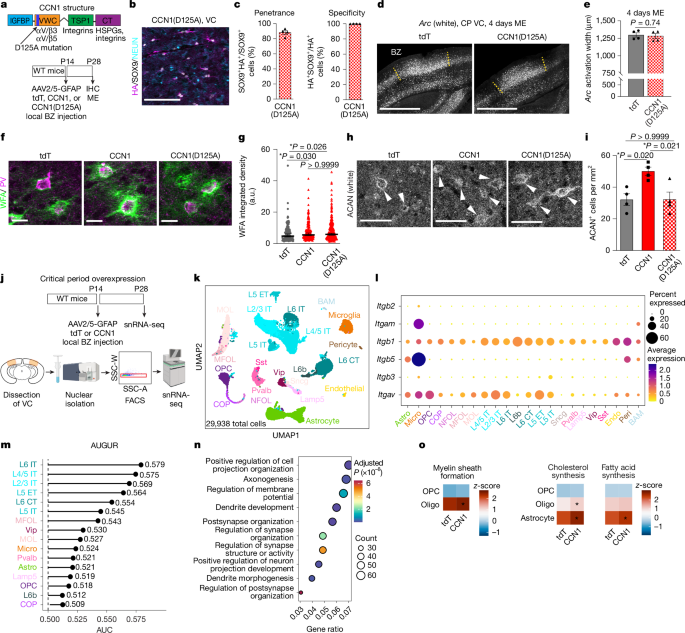
图4. 星形胶质细胞CCN1的作用机制
(图片源自《Nature》)
最后,研究者进一步通过细胞标记实验探究了星形胶质细胞CCN1对少突胶质细胞谱系的调节作用。在关键期小鼠中,野生型CCN1的过表达能促进少突胶质前体细胞向髓鞘形成阶段的分化,表现为少突胶质前体细胞(OPCs)数量减少,而新形成的髓鞘化少突胶质细胞增加。这一效应完全依赖于CCN1与αVβ3/αVβ5整合素的结合,因为无法结合该整合素的突变体CCN1(D125A)丧失了此功能。在成年期敲除星形胶质细胞CCN1则导致视觉皮层(尤其是深层)的髓鞘显著减少,但OPCs数量不变。这些结果表明,星形胶质细胞来源的CCN1通过整合素信号通路,在发育期驱动少突胶质细胞分化,并在成年期主动维持视觉皮层髓鞘的稳定。
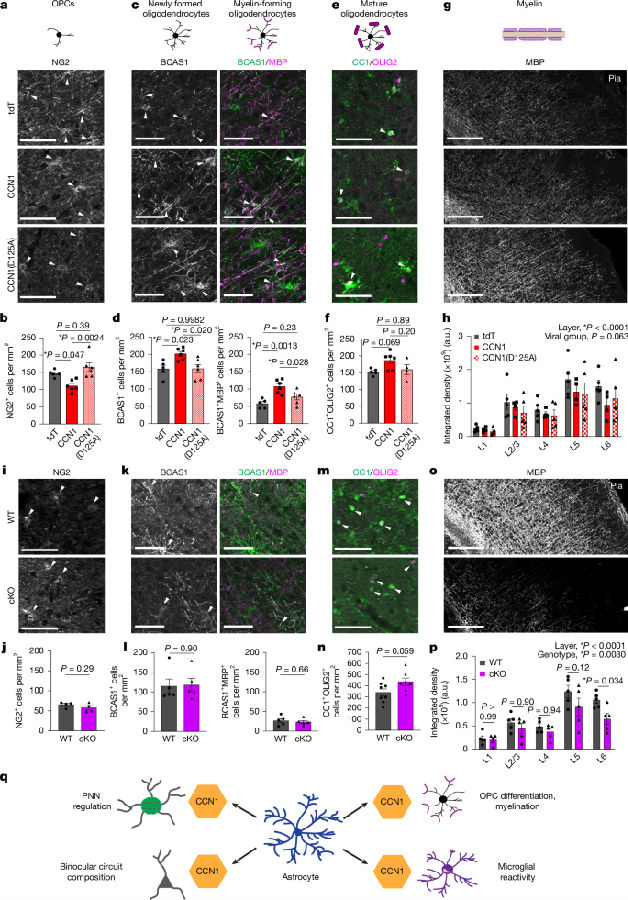
图5. 星形胶质细胞CCN1促进少突胶质细胞分化和成熟
(图片源自《Nature》)
本研究揭示了维持成年大脑稳定性的新机制,不仅为神经发育障碍及可塑性相关疾病提供了潜在治疗靶点,也为脑损伤后通过调控可塑性以促进功能恢复提供了新思路。此外,该发现提示调控星形胶质细胞与神经元、少突胶质细胞间的互作,可能为髓鞘相关疾病的干预开辟新途径。
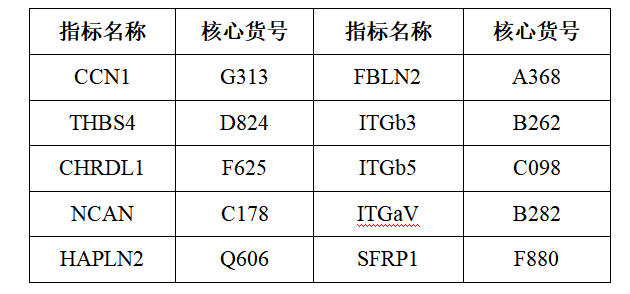
云克隆开发了上述研究中相关指标产品以助力科学研究,部分指标如下,供您参考: