失衡致病,调控为医:聚焦TCR信号转导的疾病密码与治疗突破
失衡致病,调控为医:聚焦TCR信号转导的疾病密码与治疗突破
1. T细胞受体简介
T细胞是产生有效的细胞介导的适应性免疫反应的关键介质。胸腺中T细胞的发育涉及T细胞受体(TCR)信号转导。携带对自身MHC-肽复合物具有高亲和力的TCR的细胞发生凋亡,而携带低亲和力TCR的细胞存活并分化为成熟T细胞。这些成熟T细胞离开胸腺进入外周淋巴器官,在致病性感染期间,暴露于抗原呈递细胞(APC)的MHC分子呈递的外源肽。当TCR与抗原肽结合时,T细胞会被激活,经历克隆扩增和分化,以发挥其效应器功能。因此,TCR信号转导对于有效的T细胞发育、激活和免疫耐受非常重要,其信号失调可能导致免疫无应答或自身免疫。
1.1 TCR复合体的结构
TCR复合体是由负责特异性识别抗原的TCR异二聚体(αβ或γδ链)与负责信号转导的CD3复合体(由γε、δε二聚体及ζζ同二聚体组成)非共价结合而形成的跨膜蛋白复合物。TCR的可变区识别抗原肽-MHC复合物,而CD3亚基的胞内区含有免疫受体酪氨酸激活基序(ITAM),可将识别信号传递至细胞内部,从而启动T细胞的活化与免疫应答。
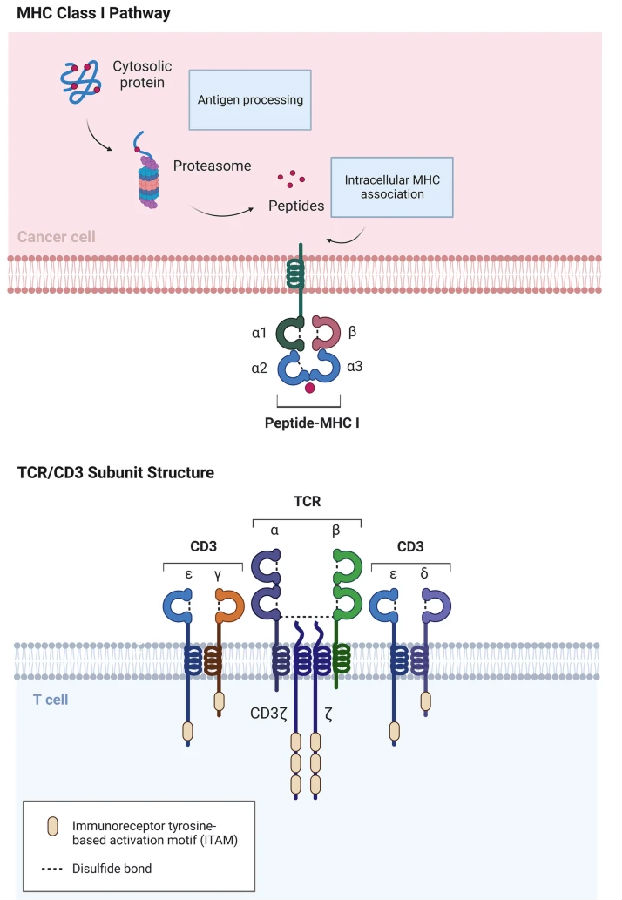
图1 TCR/CD3和MHC-肽结构示意图
(图片源于《Exp Hematol Oncol》[1])
1.2 TCR激活与近端信号转导
TCR的激活始于其与APC表面的MHC-肽复合物特异性结合,这一结合诱导TCR-CD3复合物构象变化,使与CD4或CD8共受体相连的Src家族激酶Lck活化。活化的Lck随即磷酸化CD3链胞内区ITAM上的酪氨酸残基,为下游信号分子提供锚定位点。磷酸化的ITAM募集并活化70kDaζ链关联蛋白激酶(ZAP70),后者进而磷酸化多种衔接蛋白,如T细胞激活连接蛋白(LAT)和含SH2结构域的76kDa白细胞蛋白(SLP76),促使它们组装成大型信号复合体。这一近端信号事件在细胞膜附近迅速放大了初始信号,最终通过磷脂酶Cγ(PLCγ)活化、钙离子动员及Ras/MAPK等多条通路转导,驱动T细胞活化、增殖与效应功能的启动。
1.3 TCR远端信号转导
TCR激活后,远端信号转导是指初始的膜近端信号所触发的一系列下游信号级联反应。这些信号通过主要通路向细胞核传递:一方面,PLCγ水解磷脂酰肌醇4,5-二磷酸(PIP2)产生肌醇1,4,5-三磷酸(IP3)和二酰甘油(DAG),IP3介导胞内钙离子浓度持续升高,激活钙调磷酸酶,使转录因子NFAT去磷酸化并入核;另一方面,DAG与RasGRP等蛋白协同,激活Ras/MAPK通路以及蛋白激酶Cθ(PKCθ),后者进而激活转录因子NF-κB。这些信号最终汇聚于细胞核,通过诱导特定基因的表达,驱动T细胞的克隆增殖、分化和功能执行,完成免疫应答。
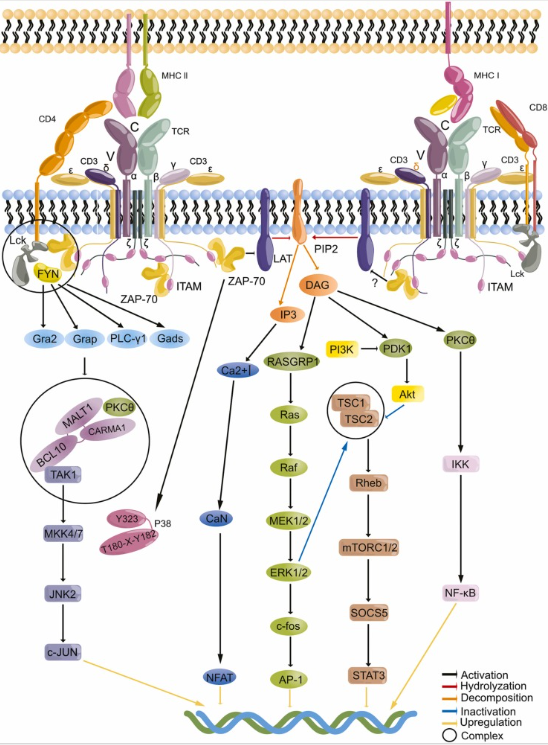
图2 TCR信号转导
(图片源于《Pharmacol Res》[2])
2. TCR信号转导与癌症的相关研究
TCR信号转导是T细胞识别并清除异常细胞的核心机制,其在癌症发生发展中扮演着“双刃剑”角色。皮肤鳞状细胞癌(cSCC)主要由紫外线介导的致癌引起,而β人瘤病毒(HPV)被认为是维持cSCC的辅助因子,T细胞反应受损的个体更易受到β-HPV介导的致癌影响。通过异体造血细胞移植恢复TCR信号完整性,可改善HPV相关侵袭性和难治性cSCC[3]。靶向降解T细胞激酶(ITK)通过调节TCR信号强度,阻断NF-kB/GATA-3信号的激活,提高T细胞淋巴瘤细胞对细胞毒性化疗的敏感性[4]。TCR通路基因在T细胞急性淋巴细胞白血病(T-ALL)和成熟T细胞癌中过度表达,ZAP70的阻断可抑制T-ALL的生长和存活[5]。肠道微生物群中的丁酸代谢物通过调节细胞毒性CD8+ T细胞的TCR信号,促进抗PD-1免疫治疗的抗肿瘤疗效[6]。将CD3ε细胞质结构域纳入第二代嵌合抗原受体(CAR)可提升CAR-T细胞的抗肿瘤活性[7]。在耗竭CD8+ T细胞分化过程中,通过微调胱天蛋白酶招募域家族成员11(CARD11)介导的TCR信号强度来扩大TCR库,重新激活抗肿瘤功能[8]。这些研究彰显了靶向TCR信号通路在癌症免疫治疗中的核心价值。
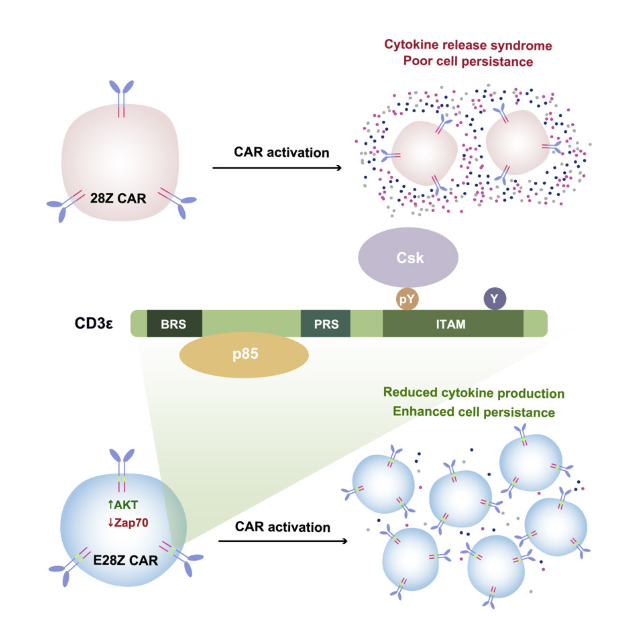
图3 将CD3ε纳入28Z CAR改变信号转导以促进抗肿瘤功能
(图片源于《Cell》[7])
3. TCR信号转导与自身免疫疾病的相关研究
TCR信号通路的失调是打破自身免疫耐受、驱动自身免疫病理发生的关键环节之一。TCR信号通过Lck/Fyn诱导STAT3磷酸化,并与细胞因子信号协同驱动TH17细胞分化[9]。选择性抑制TCR刺激诱导的STAT3磷酸化显著抑制TH17分化并缓解TH17细胞相关自身免疫疾病。淋巴细胞激活基因3(LAG-3)胞内域可与CD3ε形成液-液相分离的凝聚体,破坏CD3ε与Lck的结合,最终削弱TCR的信号转导[10]。利用同时靶向T细胞表面LAG-3与TCR复合物的双特异性抗体可实现LAG-3依赖的T细胞抑制,并有效缓解小鼠模型中的自身免疫症状。一种信号转导接头蛋白1(STAP-1)衍生肽iSP1,可抑制STAP-1与Lck的相互作用,抑制TCR介导的信号转导以及人类和小鼠的T细胞增殖[11]。此外,iSP1通过抑制Th1和Th17细胞的浸润,减缓实验性自身免疫性脑脊髓炎的进展。一种名为Raftlin的蛋白能够调节TCR信号,其缺乏可诱导T细胞依赖性抗体的产生减少,缓解实验性自身免疫性脑脊髓炎[12]。因此,深入研究TCR信号转导机制对于理解自身免疫疾病的发病机理及开发针对性治疗策略具有重要意义。
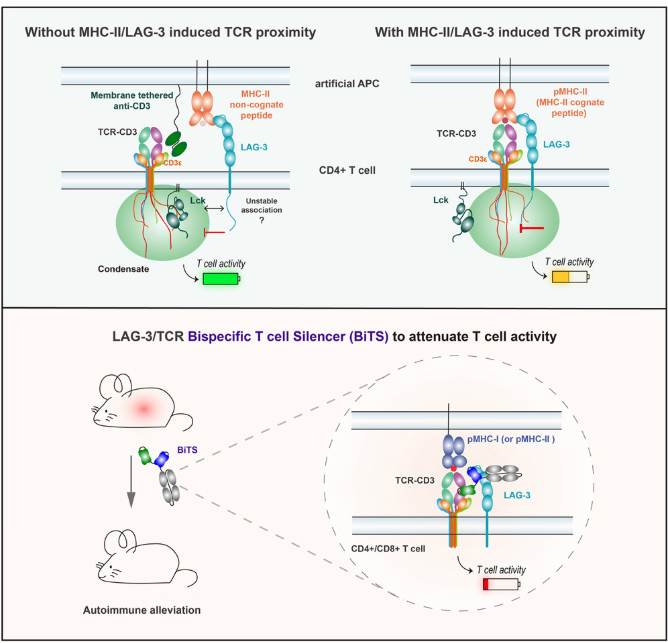
图4 LAG-3/TCR双特异性抗体能有效抑制自身免疫
(图片源于《Cell》[10])
4. TCR信号转导与心血管疾病的相关研究
TCR信号转导是T细胞活化和功能的核心,其在心血管疾病的发生发展中起着重要作用。对30名冠状动脉疾病(CAD)患者和30名对照组CD8+ T细胞的单细胞RNA测序分析中,发现CAD受试者TCR信号通路显著富集[13]。与对照组相比,CAD病例血液中对动脉粥样硬化抗原反应的CD8+ T细胞更为显著。ATP结合盒转运蛋白A1(ABCA1)对T细胞胆固醇稳态至关重要。T细胞中ABCA1的缺失会损害TCR信号转导,抑制T细胞的存活率、增殖率、分化和功能,从而在体内提供动脉粥样保护[14]。天冬酰胺內肽酶(LGMN)在调控CD4+ T细胞功能和动脉粥样硬化进展中起着关键作用。LGMN缺乏会损害TCR信号通路,抑制CD4+ T细胞的激活、存活和增殖,从而减少斑块病变中的T细胞积累[15]。AX-024是一种抑制TCR与酪氨酸激酶非催化区(Nck)蛋白相互作用的分子,能抑制抗原特异性T细胞反应。研究表明,AX-024在小鼠脑出血(ICH)模型中有效抑制出血性脑内抗原特异性和非特异性T细胞激活,以及外周抗原特异性T细胞的激活[16]。AX-024减少了分子和细胞神经炎症,减轻短期和长期脑损伤,并改善了ICH后的功能恢复。因此,靶向TCR信号通路已成为调控心血管疾病免疫炎症进程的潜在治疗策略。
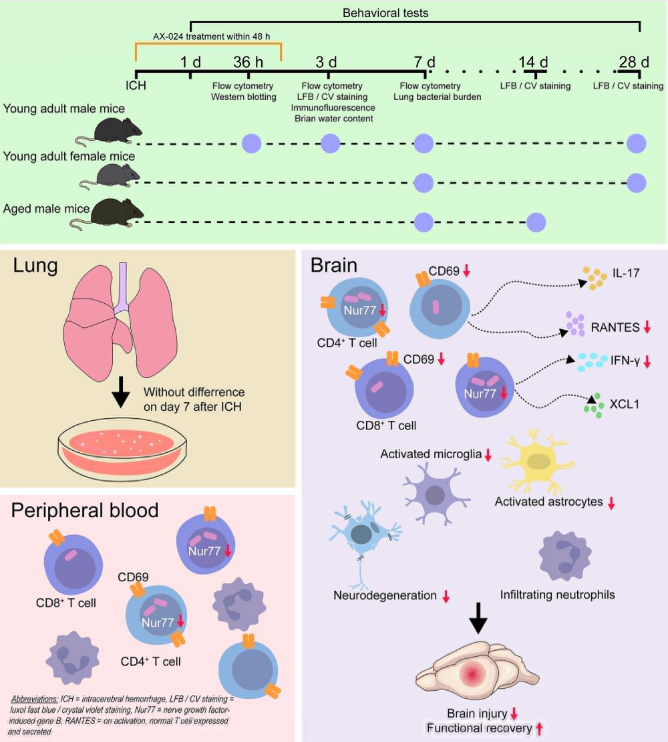
图5 AX-024抑制抗原特异性T细胞反应,改善脑出血结局
(图片源于《Stroke》[16])
5. TCR信号转导与过敏性疾病的相关研究
TCR信号转导是过敏性疾病发生的关键起始环节。CD8表皮常驻记忆T(T+RM)细胞在多种炎症性皮肤病的发病机制中起着重要作用。研究表明,CD8 T+RM细胞可以在缺乏同源抗原的情况下在皮肤中发育,但TCR信号是皮肤中过敏原特异性CD8 T+RM细胞持续存在所必需的[17]。SPA0355通过调节TCR信号转导和细胞因子诱导的JAK/STAT来抑制CD4 T细胞的激活、增殖和分化,调节Th1和Th2反应,并在卵白蛋白诱发的过敏性气道炎症中发挥保护作用[18]。对季节性变应性鼻炎(SAR)患者CD4+细胞的基因表达微阵列分析显示,38个TCR通路基因中有25个表达不同[19]。进一步分析表明覆盖ITK编码序列主要部分的单倍型是SAR的危险因素。IL-2诱导ITK对TCR信号转导至关重要,并在哮喘发病机制中起着关键作用。通过化合物筛选发现了一种新型小分子ITK抑制剂C-161。C-161能以剂量依赖性方式阻止TCR诱导的促炎细胞因子释放,以及Th2和Th17细胞的激活和分化,通过减少炎症细胞浸润和减少黏液和IgE产生,缓解哮喘进展[20]。因此,TCR信号转导是过敏免疫应答的潜在治疗靶点。
云克隆助力科学研究,为广大科研人员提供相关检测试剂产品,相关靶标核心货号如下:
靶标 | 核心货号 | 靶标 | 核心货号 | 靶标 | 核心货号 |
Bcl10 | C326 | CTLA4 | B230 | MAP2K7 | D560 |
CAM | A640 | DAG | C038 | NFAT | A504 |
CaN | B323 | ERK1 | B357 | NFATC1 | L941 |
CD28 | A652 | ERK2 | A930 | NFATC2 | L942 |
CD3d | B872 | GADS | H967 | NFkB | B824 |
CD3e | D117 | Grb2 | C514 | PDK1 | C718 |
CD3g | D118 | IKKA | K407 | PIK3Ca | J830 |
CD3z | A865 | IL2 | A073 | PIK3Cb | J829 |
CD4 | B167 | ITK | H774 | PIP3 | G856 |
CD45 | B030 | LAT | A270 | PLCg1 | A269 |
CD8a | B099 | MAP2K1 | D559 | SHP1 | D589 |
CD8b | Q127 | MAP2K2 | D562 | SLP76 | B205 |
c-Jun | B292 | MAP2K4 | D564 | zAP70 | P541 |
更多科研试剂,欢迎访问云克隆官方网站:http://www.cloud-clone.cn/
参考文献
[1]Shao W, Yao Y, Yang L, et al. Novel insights into TCR-T cell therapy in solid neoplasms: optimizing adoptive immunotherapy. Exp Hematol Oncol. 2024;13(1):37.
[2]Liu Y, Chen S, Liu S, et al. T-cell receptor signaling modulated by the co-receptors: Potential targets for stroke treatment. Pharmacol Res. 2023;192:106797.
[3]Ye P, Bergerson JRE, Brownell I, et al. Resolution of Squamous-Cell Carcinoma by Restoring T-Cell Receptor Signaling. N Engl J Med. 2025;393(5):469-478.
[4]Jiang B, Weinstock DM, Donovan KA, et al. ITK degradation to block T cell receptor signaling and overcome therapeutic resistance in T cell lymphomas. Cell Chem Biol. 2023;30(4):383-393.e6.
[5]Suske T, Sorger H, Manhart G, et al. Hyperactive STAT5 hijacks T cell receptor signaling and drives immature T cell acute lymphoblastic leukemia. J Clin Invest. 2024;134(8):e168536.
[6]Zhu X, Li K, Liu G, et al. Microbial metabolite butyrate promotes anti-PD-1 antitumor efficacy by modulating T cell receptor signaling of cytotoxic CD8 T cell. Gut Microbes. 2023;15(2):2249143.
[7]Wu W, Zhou Q, Masubuchi T, et al. Multiple Signaling Roles of CD3ε and Its Application in CAR-T Cell Therapy. Cell. 2020;182(4):855-871.e23.
[8]Hu Y, Zhao Q, Qin Y, et al. CARD11 signaling regulates CD8+ T cell tumoricidal function. Nat Immunol. 2025;26(7):1113-1126.
[9]Qin Z, Wang R, Hou P, et al. TCR signaling induces STAT3 phosphorylation to promote TH17 cell differentiation. J Exp Med. 2024;221(3):e20230683.
[10]Du J, Chen H, You J, et al. Proximity between LAG-3 and the T cell receptor guides suppression of T cell activation and autoimmunity. Cell. 2025;188(15):4025-4042.e20.
[11]Sasaki Y, Kagohashi K, Kawahara S, et al. STAP-1-derived peptide suppresses TCR-mediated T cell activation and ameliorates immune diseases by inhibiting STAP-1-LCK binding. Immunohorizons. 2025;9(6):vlaf015.
[12]Saeki K, Fukuyama S, Ayada T, et al. A major lipid raft protein raftlin modulates T cell receptor signaling and enhances th17-mediated autoimmune responses. J Immunol. 2009;182(10):5929-5937.
[13]Iqneibi S, Saigusa R, Khan A, et al. Single cell transcriptomics reveals recent CD8T cell receptor signaling in patients with coronary artery disease. Front Immunol. 2023;14:1239148.
[14]Zhao Y, Zhang L, Liu L, et al. Specific Loss of ABCA1 (ATP-Binding Cassette Transporter A1) Suppresses TCR (T-Cell Receptor) Signaling and Provides Protection Against Atherosclerosis. Arterioscler Thromb Vasc Biol. 2022;42(12):e311-e326.
[15]Xiang X, Zhang F, Nie L, et al. Legumain deficiency halts atherogenesis by modulating T cell receptor signaling. Aging Cell. 2025;24(2):e14391.
[16]Chen S, Fu P, Rastegar-Kashkooli Y, et al. AX-024 Inhibits Antigen-Specific T-Cell Response and Improves Intracerebral Hemorrhage Outcomes in Mice. Stroke. 2025;56(5):1253-1265.
[17]Funch AB, Weber JF, Mraz V, et al. CD8+ Skin-Resident Memory T Cells Require TCR Signaling for their Persistence in a Mouse Model of Allergic Contact Dermatitis. J Invest Dermatol. 2026;146(1):165-174.e3.
[18]Jang HY, Jeon R, Kang KW, et al. SPA0355 suppresses T-cell responses and reduces airway inflammation in mice. Eur J Pharmacol. 2014;745:19-28.
[19]Benson M, Mobini R, Barrenäs F, et al. A haplotype in the inducible T-cell tyrosine kinase is a risk factor for seasonal allergic rhinitis. Allergy. 2009;64(9):1286-1291.
[20]Guo Z, Ye F, Zhang Y, et al. A Novel Small Molecule ITK Inhibitor Suppresses Th2/Th17 Differentiation and Attenuates Airway Inflammation in a Mouse Model of HDM-Induced Asthma. Immunology. 2025;176(3):349-362.