即使衰老,免疫力也有望增强
衰老会削弱免疫力,部分原因是T细胞库重塑,导致对感染、恶性肿瘤等的易感性增加。对抗免疫衰老的研究主要集中在通过激素、细胞因子、小分子物质逆转胸腺退化,或直接调控造血功能。但受限于毒性或临床可行性,目前免疫功能的恢复效果十分有限。
2025年12月17日,有研究团队在《Nature》期刊上发表了题为“Transient hepatic reconstitution of trophic factors enhances aged immunity”的文章,该研究证明通过mRNA给药临时改变肝脏功能可恢复衰老小鼠的免疫信号并改善T细胞功能。Notch和Fms-like tyrosine kinase 3 ligand(FLT3L)通路及IL-7信号会随年龄增长而衰退。向肝细胞递送编码Delta-like ligand 1(DLL1)、FLT3L和IL-7的mRNA可增加淋巴祖细胞数量,促进新生胸腺细胞生成而不影响造血干细胞组成。用这些mRNA进行治疗,不仅能增强肽疫苗的免疫应答,还能通过提升肿瘤特异性CD8+细胞浸润,与免疫检查点阻断疗法产生协同效应,从而恢复老年小鼠的抗肿瘤免疫力。且这些效果在停药后可逆,不会破坏自身免疫耐受。

该文章研究思路如下:
一、肝脏中免疫信号的重构
肝脏独特的血流动力学和解剖学特征使其能够启动和维持适应性免疫,且其蛋白质合成能力即使在高龄时仍得以保留,这使其成为调节循环T细胞的理想部位。所以研究者在肝脏中重建了源自胸腺的因子,以解决与年龄相关的免疫功能衰退问题。研究者发现老年小鼠胸腺内及循环T细胞均表现出Notch、IL-7和FLT3L靶基因表达降低。采用三种免疫营养因子——DLL1(用于激活Notch)、FLT3L和IL-7(统称DFI)的全身性脂质纳米颗粒(LNPs)给药,使得编码这些因子的mRNA被递送至肝脏,体内肝细胞中三种DFI mRNA均呈现显著翻译活性,其他组织的翻译水平极低。研究者选择mRNA递送而非重组蛋白,因为重组细胞因子清除迅速,需要频繁高剂量给药导致毒性显著。相比之下,mRNA可实现更可控、短暂的蛋白质生成。而后研究者评估了药代动力学和安全性,观察到老年小鼠(72周龄)在DFI mRNA-LNPs给药4周后,体重、转氨酶及肝功能均未发生变化,组织病理学检查仅显示轻微肝脏炎症。采用相同给药方案(每周两次,持续28天)的重组FLT3L和IL-7则显著提升了GM-CSF、IL-10、IL-12和IL-1β水平,这凸显了重组细胞因子引发全身性炎症的风险更高。(见图1)
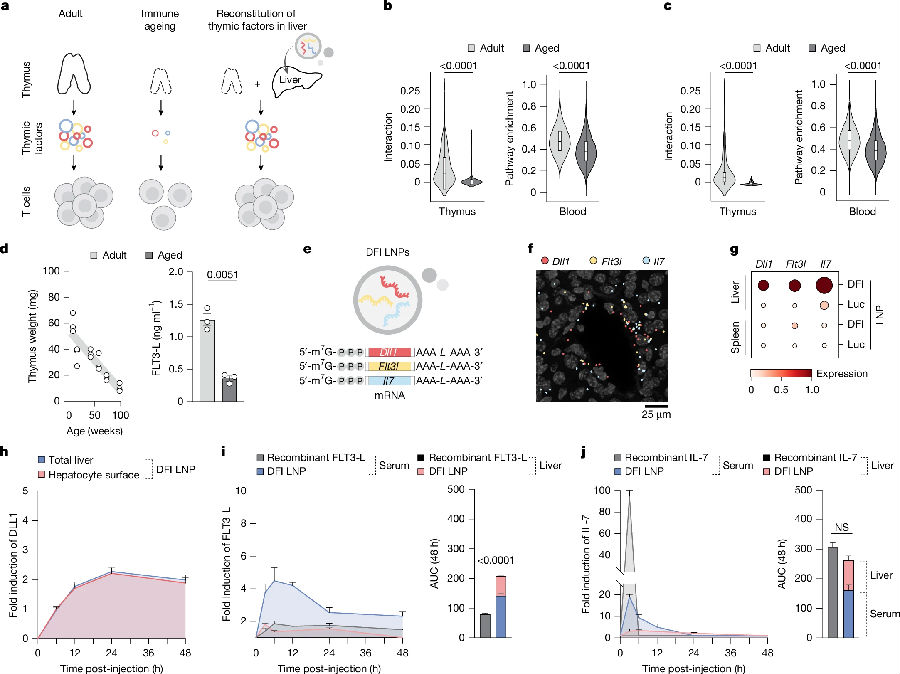
图1. 恢复衰老过程中下降的T细胞信号传导因子的功能,重建肝脏中的免疫信号传导机制。(图片来源于《Nature》杂志)
二、DFI缓解免疫衰老表型
衰老伴随着初始T细胞的丢失及耗竭样状态的积累,这种现象在CD8+T细胞中最为显著,并由胸腺退化、慢性抗原暴露和炎症驱动。老年小鼠每周接受两次DFI mRNA–LNPs或Luc mRNA–LNPs治疗,持续28天。结果发现DFI(而非单一因子)提高了循环中初始(CD44-CD62L+)CD4+和CD8+T细胞的频率和绝对数量,但并未增加记忆亚群。因此,DFI处理动物血液和脾脏中的初始细胞与记忆细胞比例上升。且DFI选择性扩增了早期T细胞谱系定向阶段的胸腺细胞,并在12小时内诱导Rag2–eGFP小鼠胸腺细胞中表达Rag2(在小鼠胸腺细胞中,Rag2会影响T细胞发育、免疫系统功能等)。随后在治疗28天后,成熟的单阳性CD4+和CD8+胸腺细胞数量增加至年轻小鼠水平。循环T细胞中Nur77表达升高,提示胸腺迁移细胞增加。研究者还发现DFI通过扩增定向分化淋巴祖细胞并促进胸腺内成熟,而不改变造血干细胞组成,从而增强初始T细胞的输出。除T细胞外,DFI还减轻了抗原呈递细胞和B细胞区室中与衰老相关的表型。(见图2)
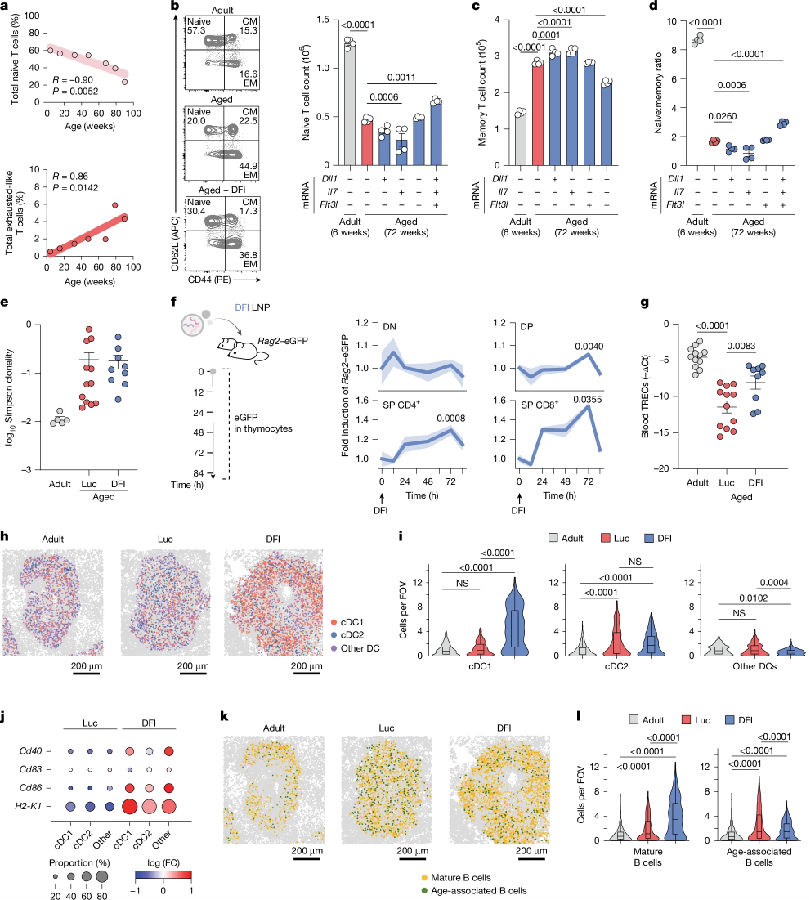
图2. DFI治疗减轻了衰老相关免疫特征。
(图片来源于《Nature》杂志)
三、DFI加强疫苗反应
基于上述发现,研究者接下来测试了DFI能否恢复老年动物的适应性免疫功能。作为测试案例,观察了疫苗应答——一种已知会因衰老而减弱的T细胞介导过程。在成年(6周龄)和老年(72周龄)小鼠的佐剂卵清蛋白(OVA)初免-加强模型中,老年组在接种疫苗后脾脏和血液中OVA特异性CD8+T细胞较少,抗原驱动的细胞增殖受损,再次免疫时IL-2和IFNγ生成量减少,接近假疫苗接种对照小鼠的水平。在接种前用DFI组合对老年小鼠进行预处理显示,总T细胞和OVA特异性CD8+细胞频率同时增加,因而脾脏中抗原特异性CD8+T细胞增加约两倍,血液中也出现类似增幅,而这种表型在重复接种后进一步扩大。DFI处理组在疫苗接种后保留了更高的初始细胞比例,并减少了PD1highCD62L-细胞,产生了更平衡的T细胞组成。功能上,DFI处理小鼠的CD8+T细胞在抗原特异性再刺激下产生了更高水平的IL-2和IFNγ,而OVA特异性CD4+细胞频率和细胞因子基本保持不变,表明DFI优先支持CD8+T细胞反应。DFI治疗能将老年小鼠的疫苗诱导T细胞数提升至与年轻小鼠相当的水平。(见图3)
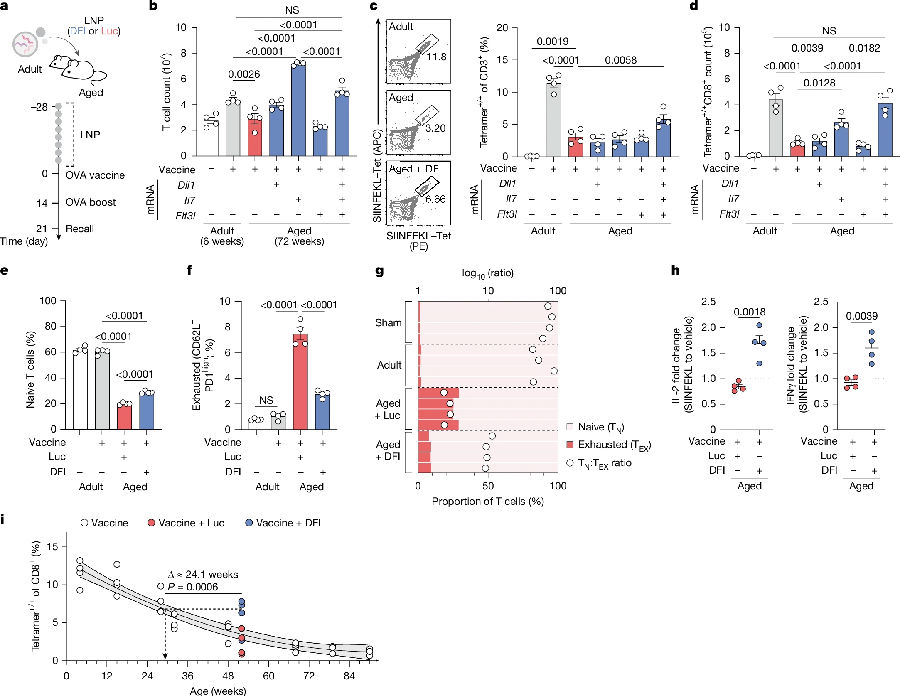
图3. 肝脏DFI重建增强疫苗诱导的衰老宿主T细胞应答。
(图片来源于《Nature》杂志)
四、DFI可增强抗肿瘤反应
研究者随后测试了DFI是否能改善对肿瘤免疫治疗的反应性,这种反应性也会随年龄增长而减弱。在B16-OVA黑色素瘤和MC38-OVA结肠癌模型中,老年小鼠比成年小鼠表现出更快的肿瘤进展和更差的生存率;在成年小鼠中通过PDL1阻断实现的免疫检查点抑制(ICI)虽能控制肿瘤,但在老年组中效果甚微。研究者对MC38-OVA模型进行DFI预处理,发现生存期延长。在更具侵袭性的B16-OVA模型中,DFI使40%的老年小鼠发生完全排斥反应,而所有对照组小鼠尽管接受
抗PDL1治疗,仍于3周内死亡。在已建立肿瘤的老年小鼠中,治疗开始时联合给药与单独PDL1阻断相比,同样能延缓疾病进展并提高生存率。且研究者发现DFI增加了肿瘤内CD8+T细胞频率,肿瘤浸润淋巴细胞总数未发生变化。DFI治疗后,耗竭相关基因(Havcr2、Gzmk、Lag3、Pdcd1和Tigit)表达水平下降。这些研究结果表明单独使用DFI调节即可增强内源性抗肿瘤,与PDL1阻断协同作用可提高老年小鼠的治疗效果。(见图4)
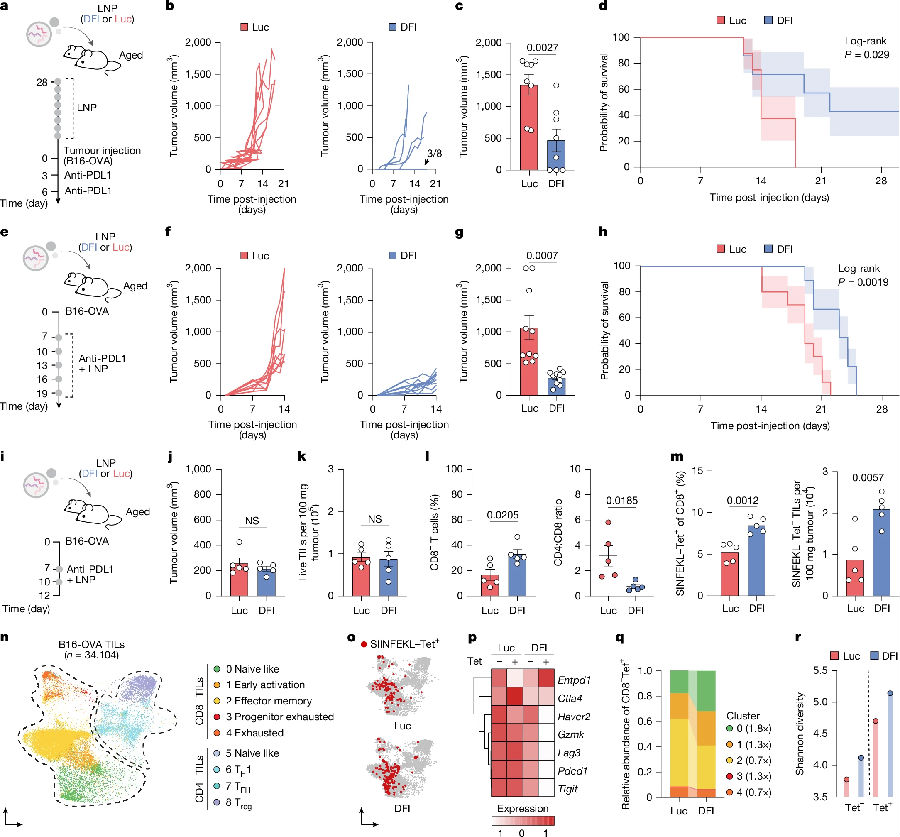
图4. 肝脏DFI重建可增强老年宿主的抗肿瘤T细胞反应。
(图片来源于《Nature》杂志)
五、DFI治疗的免疫安全性
为评估DFI的持久性和安全性,老年小鼠接受DFI或对照mRNA-LNPs治疗28天后,继续观察28天。发现DFI治疗的免疫增强作用主要局限于给药窗口期,并在停药后逆转。随后评估了DFI是否会加剧自身免疫性疾病。在易患1型糖尿病的NOD小鼠中(频繁产生自身反应性TCRs(T cell receptor)),给予4周DFI或对照mRNA后,对血糖、糖尿及疾病发作进行了为期6个月的监测。发现DFI未改变血糖水平、糖尿病发作或自身反应性T细胞频率。后又在实验性自身免疫性脑炎等模型中进行验证,发现DFI在多个模型中可短暂增强老年宿主的抗原特异性免疫,同时维持自身免疫耐受。这些效应具有可逆性和时间限制性。
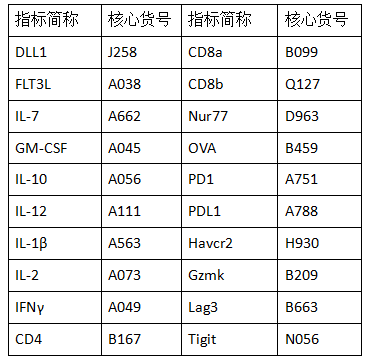
该研究结果表明,通过将肝脏作为异位生产免疫因子的平台,可有效改善免疫功能。向肝脏递送编码DLL1、IL-7和FLT3L的mRNA组合,成功增强了老年小鼠的免疫功能。相较于胸腺移植或操作造血干细胞(HSC)等侵入性更强的方法,该方案临床实施更具可行性。且mRNA疗法缓解了通常与重组细胞因子疗法相关的全身性炎症和自身免疫后遗症。这些发现彰显了mRNA疗法在系统性免疫调节领域的应用前景和在老年群体免疫力减弱干预方面的巨大潜力。云克隆开发了与该研究相关的靶标产品,部分指标节选如下:
更多信息,欢迎访问:http://www.cloud-clone.cn/