云克隆助力探索肥胖代谢疾病治疗新途径
医学上,肥胖被定义为威胁健康的异常或过度脂肪堆积,并非单纯体重超标,而是与心血管疾病、代谢综合征、2型糖尿病、非酒精性脂肪肝等多种合并症高度绑定,成为全球医疗成本居高不下的重要诱因。传统观念将肥胖归咎于热量摄入与消耗失衡,但临床研究证实,其发病涉及全身多器官、多信号通路协同调控,单纯饮食运动干预,对中重度肥胖患者效果十分有限。好消息是,仅减重5%-10%,就能显著改善血糖、血脂等心血管风险标志物,有效降低代谢疾病发病概率,因此研发安全长效的代谢调控手段,成为破局关键。

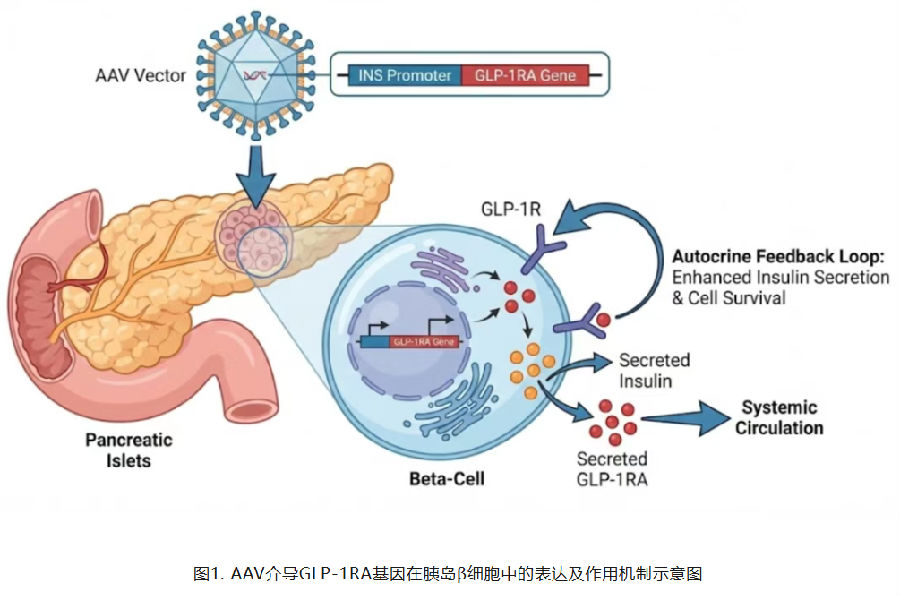
GLP-1受体激动剂是当下减重与降糖领域的绝对明星,第二代长效制剂司美格鲁肽,凭借多器官协同调控机制出圈:它能实现血糖依赖性降糖,规避低血糖风险,同时延缓胃排空延长饱腹感,直接作用于中枢抑制食欲,从控糖、减摄入、调代谢三维度实现高效减重。但传统药物需定期注射,患者依从性差,科研界随即转向AAV基因治疗赛道。科研人员利用腺相关病毒(AAV)载体,将GLP-1长效类似物编码基因靶向导入胰岛β细胞,让细胞持续表达活性蛋白,激活下游信号通路;一方面葡萄糖依赖性促进胰岛素分泌、保护胰岛β细胞功能,另一方面同步实现延缓胃排空、抑制食欲的效果,一次给药即可实现糖代谢与体重的长效稳定调控,突破传统药物局限。

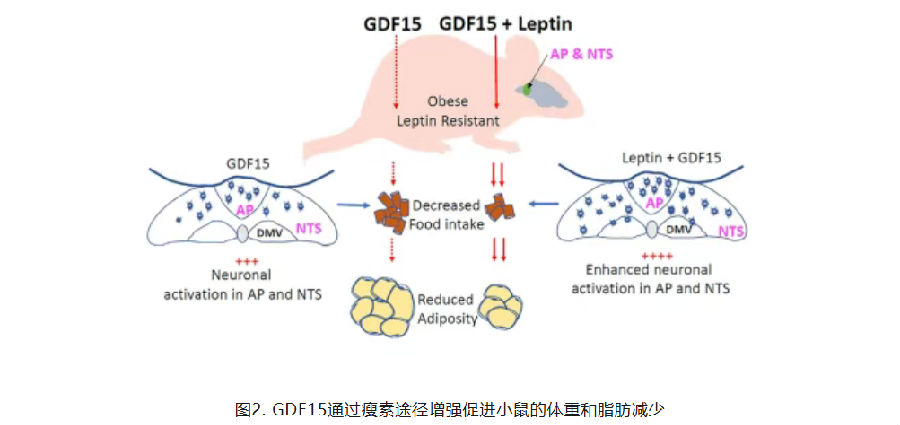
除GLP-1通路外,生长分化因子15(GDF15)成为肥胖治疗潜力新靶点,它通过后脑极后区、孤束核神经元发挥厌食作用,特异性受体GFRAL仅表达于孤束核,精准靶向食欲调控中枢。澳大利亚Samuel N. Breit团队研究揭开核心机制:GDF15与食欲调节因子瘦素存在强效协同作用。高脂饮食诱导的肥胖小鼠实验显示,二者联合用药的减重减脂效果,远优于单一用药;若机体缺乏瘦素或阻断瘦素信号,对GDF15的应答会显著减弱。进一步研究证实,瘦素信号通路可增强GDF15代谢效应,GDF15需借助瘦素通路,才能实现体重与脂肪的双重减少,为联合靶点新药研发提供了核心理论支撑。
无论是GLP-1基因治疗优化,还是GDF15新靶点验证,抑或是肥胖相关合并症药物研发,都离不开高质量科研工具的支撑。武汉云克隆依托超27000种自主研发抗体库,搭建了从靶点发现、机制验证到药物活性检测的全流程科研解决方案,精准覆盖肥胖及代谢疾病研究需求。针对GLP-1、GDF15、瘦素等热门靶点,可提供高特异性抗体、重组蛋白、ELISA试剂盒以及多因子检测试剂盒等核心试剂;同时可提供糖尿病、心血管疾病、高脂诱导肥胖等多种标准化动物模型,精准还原疾病特征,全方位助力科研人员突破研究瓶颈,加速新药与治疗技术临床转化。
糖尿病(DM)大鼠模型
建模方法:
1. 术前12h禁食
2. 模型组大鼠按照55mg/kg剂量的STZ进行腹腔注射,对照组给予相同剂量的柠檬酸钠缓冲液。
3. STZ注射7d后,测空腹血糖,选择血糖为13.5-25mmol/L纳入正式实验。
4. STZ注射后,每周测血糖,称体重,观察体重血糖变化。
5. 第4周检测各组大鼠的体重和空腹血糖值后,摘眼球采血,室温静置2h后于4℃ 3000r离心10分钟提取血清,放入-80℃ 冰箱冻存。同时取黄脂,皮下脂肪,骨骼肌,白脂,肝脏,肺脏,心脏,肾脏用于病理和分子生物学检测。
糖尿病视网膜病变(DR)大鼠模型
建模方法: