聚焦IL6家族:连接免疫、炎症与重大疾病的分子枢纽
聚焦IL6家族:连接免疫、炎症与重大疾病的分子枢纽
1.白细胞介素6家族简介
白细胞介素(IL)6家族是一组参与调节损伤和感染急性期反应的重要细胞因子,由IL6、IL11、IL31、纤毛神经营养因子(CNTF)、白血病抑制因子(LIF)、肿瘤发生素M(OSM)、心肌营养素1(CT1)、心肌样细胞因子(CLC)等组成。该细胞因子家族的成员具有促炎和抗炎特性,激活参与分化、存活、凋亡和增殖的靶基因,是造血、急性期和机体免疫反应的主要参与者。
1.1 IL6与其受体结构
IL6是一种单链糖蛋白,主要由四个螺旋束组成。螺旋A和B沿一个方向延伸,而C和D沿相反方向延伸。IL6通过细胞表面I型受体复合物传递其信号,该复合物由称为IL6受体(IL6R)的配体结合糖蛋白和信号转导成分糖蛋白130(gp130)组成。IL6R是一条80 kDa的α链,也被称为CD126。它由三个结构域组成,即D1、D2和D3。D1也被称为免疫球蛋白(Ig)结构域,D2和D3构成胞外区细胞因子结合结构域(CBD)。gp130是由一个β链组成,也被称为CD130。gp130由六个结构域(D1-D6)组成。与IL6R相似,D1是Ig结构域,D2和D3构成CBD。另外三个结构域(D4-D6)是与IL6结合以及刺激后续信号转导机制的重要组成部分。
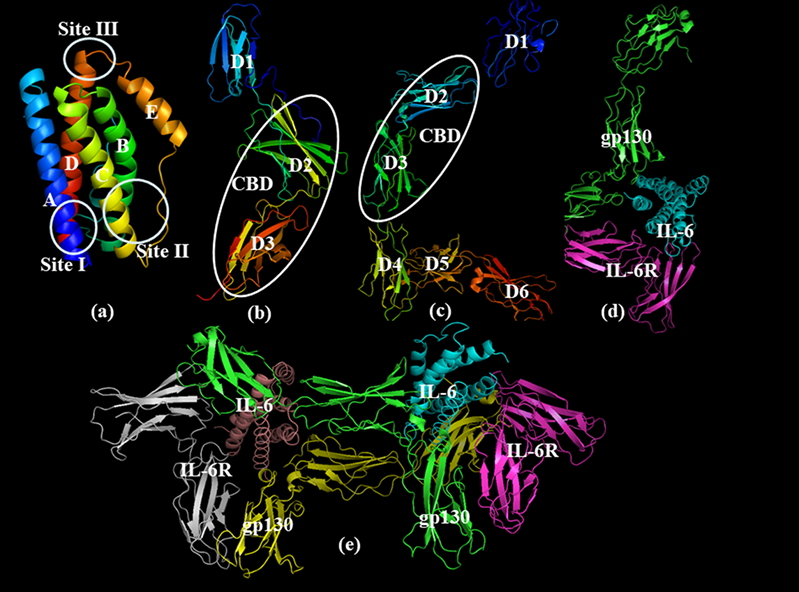
图1 IL6及其受体的结构
(图片源于《Bioorg Med Chem》[1])
1.2 IL6信号转导途径
IL6的信号转导可根据其结合受体分为经典信号转导和反式信号转导。IL6结合无激酶活性的IL6R,随后IL6R结合信号转导受体链糖蛋白130(gp130),从而激活JAK/STAT和MAPK级联反应。IL6R有两种类型。膜IL6R仅由少数细胞(包括肝细胞和淋巴细胞亚群)表达,传递经典信号。因此,IL6传递的经典信号通路仅限于特定细胞。另一种IL6R是可溶性IL6R(sIL6R),它通过蛋白水解切断膜IL6R或通过选择剪接mRNA的翻译表达,并传递反式信号。IL6与sIL6Ra结合形成复合物,随后通过gp130激活细胞内信号转导。由于几乎所有细胞表达gp130,IL6的转运信号几乎存在于所有细胞中。
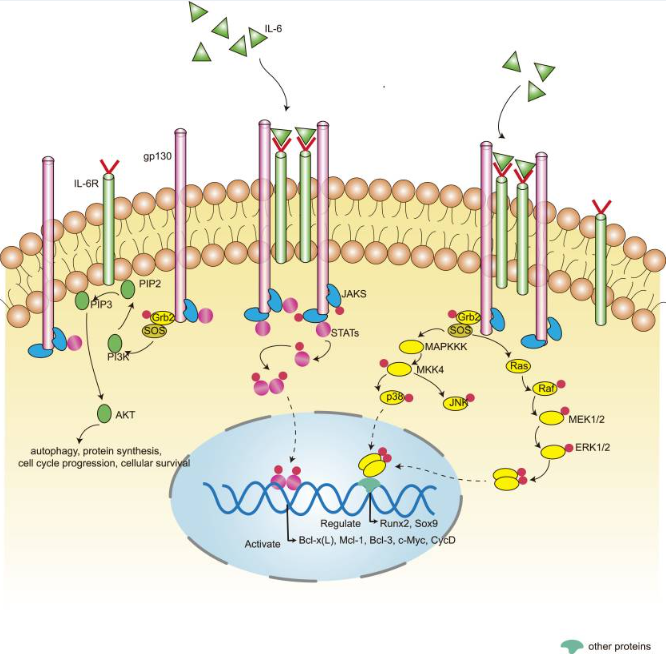
图2 IL6经典信号通路
(图片源于《Kidney Dis (Basel)》[2])
1.3 IL6家族功能
IL6家族细胞因子是一类功能广泛且核心的信号蛋白,它们通过共享gp130受体激活JAK/STAT和MAPK等信号通路,在机体生理和病理过程中扮演“双刃剑”角色。一方面,它们主导急性免疫防御、促进组织修复、调节代谢并维持稳态;另一方面,其过度或持续激活会驱动慢性炎症、自身免疫病、纤维化和癌症进展。因此,该家族是连接免疫、代谢与组织功能的关键枢纽,也是重要的疾病治疗靶标。
2. IL6家族与癌症的相关研究
IL6家族相关细胞因子被认为是炎症与癌症之间的关键因素。IL6的过度表达与肿瘤进展有关,其机制包括抑制癌细胞凋亡、刺激血管生成以及增强耐药性[3-7]。通过抑制IL6/STAT3通路,如使用IL6R抑制剂托珠单抗,可以消除双皮质素样激酶1(DCLK1)对三阴性乳腺癌(TNBC)细胞恶性表型的促进作用[8]。IL6中和抗体司妥昔单抗可能以细胞依赖性方式抑制STAT3酪氨酸磷酸化,从而抑制体内肺癌细胞的生长[9]。选择性雌激素受体调节剂巴多昔芬可能通过干扰IL6家族蛋白与gp130之间的蛋白质相互作用,抑制IL11介导的信号转导来限制肠道肿瘤的生长[10]。一种小分子化合物,SMI-10B13,可抑制OSM信号。在人类乳腺癌小鼠模型中,SMI-10B13减少了肿瘤生长,提升小鼠生存率[11]。LIF是激活胰腺星状细胞作用于癌细胞的关键副分泌因子。药物性LIF阻断显著减缓肿瘤进展,并增强化疗疗效以延长胰导管腺癌小鼠模型的存活期[12]。这些研究突出了靶向IL6家族成员对癌症治疗的潜在临床益处。
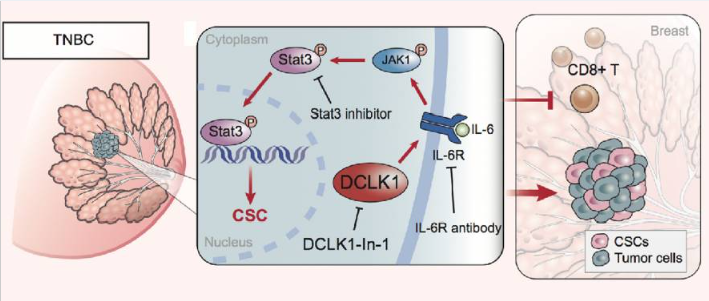
图3 DCLK1激活的IL6/STAT3通路在TNBC恶性表型和抗肿瘤免疫中起关键作用
(图片源于《Breast Cancer Res》[8])
3. IL6家族与自身免疫疾病的相关研究
IL6家族蛋白已被充分描述为慢性炎症的主要因素,而慢性炎症对自身免疫性疾病的发展至关重要。系统性红斑狼疮(SLE)是一种由免疫系统失调引起的自身免疫疾病。抗IL6单克隆抗体抑制了SLE相关自身抗体的产生,可预防严重肾病的发展[13]。IL6有助于博来霉素诱导的皮肤硬化,而IL6受体特异性单克隆抗体可能通过抑制成纤维细胞激活来改善硬皮病症状[14]。IL11在类风湿性关节炎(RA)的发病机制中具有双重作用,既能增强滑膜成纤维细胞的浸润,又能通过增加血管对RA血管翳的侵袭来进一步加重疾病的严重程度[15]。OSM在狼疮肾炎(LN)小鼠肾脏组织中高表达,抗OSM抗体能改善炎症和肾小管间质纤维化,并部分改善24小时尿蛋白排泄和血尿素氮产生[16]。疱疹型天疱疮(PH)中皮下IL31细胞和IL31RA细胞数量有所增加。增强的IL31/IL31RA信号以及皮肤嗜酸性粒细胞和嗜碱性粒细胞数量增加可能参与PH中的瘙痒[17]。基于此,靶向IL6家族通路已成为重要的治疗策略,显著改善自身免疫疾病的临床预后。
4. IL6家族与心血管疾病的相关研究
在炎症介质中,IL6家族蛋白是心血管疾病病理生理的关键因素。多项关联分析研究表明,IL6与主要不良心血管事件和心血管死亡或心力衰竭的风险显著相关[18-20]。在心肌梗死后中和IL6受体抑制了心肌炎症,从而缓解了左心室重塑[21]。临床研究显示IL6抑制剂泽韦奇单抗显著降低了与动脉粥样硬化相关的炎症和血栓形成的生物标志物[22]。在晚期动脉粥样硬化模型中,抑制CT1促进了抗炎和动脉粥样保护作用,从而消除了动脉粥样硬化进展[23]。血浆CT1水平升高与高血压患者心脏衰竭风险相关,可作为确定高血压患者预后的生物标志物[24]。马凡综合征(MFS)小鼠主动脉中的IL11 mRNA和蛋白质升高,抑制IL11通路缓解MFS小鼠疾病症状[25]。OSM通过促进Notch3的产生,抑制心肌细胞凋亡,从而激活PI3K/Akt通路,从而缓解了心脏缺血/再灌注(I/R)损伤[26]。LIF可防止预先形成的动脉粥样硬化斑块的进展,影响病灶大小和血管反应性[27]。这些结果表明IL6家族成员是心血管疾病预防和治疗的可能干预靶点。
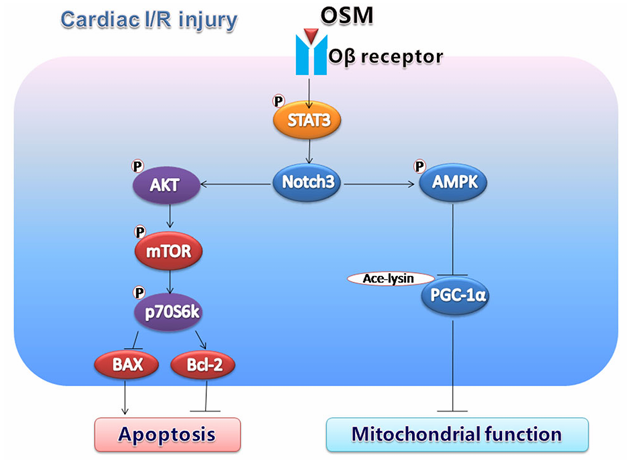
图4 OSM在心脏I/R损伤中保护作用的可能机制的示意图
(图片源于《Apoptosis》[26])
5. IL6家族与纤维化疾病的相关研究
由于炎症与纤维化密切相关,越来越多的研究显示IL6家族成员在器官纤维化中的发挥重要作用。在IL6敲除小鼠中,高盐饮食或血管紧张素II诱导的心脏功能障碍和纤维化有所减少[28]。阻断IL6信号转导降低单侧输尿管阻塞(UUO)小鼠模型肾组织中的炎症水平、免疫细胞浸润以及促纤维化细胞因子的表达,抑制肾纤维化进展[29]。IL6反式信号转导是肺部异体移植物纤维化的关键驱动因素[30]。在小鼠中,特异性IL11转基因表达或重组蛋白注射会导致心脏和肾脏纤维化及器官衰竭[31]。抗IL11治疗减轻了博来霉素肺纤维化小鼠模型的肺部炎症并逆转了肺纤维化[32]。OSM通过调节巨噬细胞活化在慢性肝损伤期间发挥强力的纤维生成活性[33]。在肾小管间质纤维化(TIF)小鼠模型中,LIF过度表达会加重TIF[34]。通过给小鼠施用LIF中和抗体,观察到对TIF的明显疗效。与其他家族成员相反,外源性CT1的给药可以通过抵消炎症、凋亡来减轻UUO小鼠的肾纤维化[35]。因此靶向该家族信号通路已成为抗纤维化治疗的重要策略。
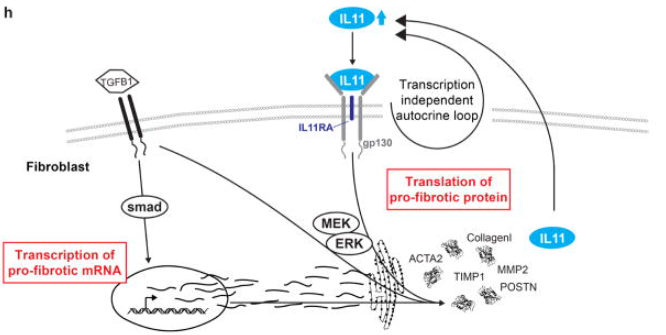
图5 IL11的促纤维化作用
(图片源于《Nature》[31])
云克隆助力科学研究,为广大科研人员提供相关检测试剂产品,相关靶标核心货号如下:
靶标 | 核心货号 | 靶标 | 核心货号 | 靶标 | 核心货号 |
AKT1 | C231 | IL31RA | E763 | OSMR | B761 |
AKT2 | B719 | IL6 | A079 | PDK1 | C718 |
AKT3 | A382 | IL6R | B815 | PIK3Cb | J829 |
CLCF1 | C389 | IRS1 | C546 | PIK3Cd | J832 |
CNTF | A021 | IRS2 | D880 | PKCd | A433 |
CNTFR | C185 | JAK1 | C551 | PTPN11 | D584 |
CREB | B318 | JAK2 | F494 | Rac1 | M427 |
CRLF1 | F303 | JAK3 | F493 | Raf-1 | C232 |
CT1 | A810 | JNK1 | B156 | RASA1 | B616 |
ERK1 | B357 | JNK2 | D576 | RPS6Kb1 | L979 |
ERK2 | A930 | Jun | B292 | RPTOR | M681 |
FOS | B291 | JunB | H765 | SHC1 | E671 |
FOSL1 | J089 | LIF | A085 | SORT1 | C895 |
GAB2 | L533 | LIFR | A561 | STAT1 | B740 |
GbL | N253 | MAP2K1 | D559 | STAT2 | B796 |
gp130 | A046 | MAP2K2 | D562 | STAT3 | B743 |
GRB2 | C514 | MAP2K4 | MKK4 | STAT4 | B739 |
GSK3a | A630 | MAPK11 | B435 | STAT5A | B738 |
GSK3b | D317 | MAPK12 | D577 | STAT5B | B727 |
IL11 | A057 | MAPK13 | D578 | STAT6 | B737 |
IL11Ra | E771 | MAPK14 | B206 | TSC1 | C813 |
IL27A | A385 | MAPK7 | B431 | TYK2 | B595 |
IL27Ra | B194 | mTOR | B806 | Vav1 | C213 |
IL31 | B179 | OSM | A110 |
更多科研试剂,欢迎访问云克隆官方网站:http://www.cloud-clone.cn/
参考文献
[1]Kaur S, Bansal Y, Kumar R, Bansal G. A panoramic review of IL-6: Structure, pathophysiological roles and inhibitors. Bioorg Med Chem. 2020;28(5):115327.
[2]Chen Y, Zhou J, Xu S, Nie J. Role of Interleukin-6 Family Cytokines in Organ Fibrosis. Kidney Dis (Basel). 2023;9(4):239-253.
[3]Ara T, Declerck YA. Interleukin-6 in bone metastasis and cancer progression. Eur J Cancer. 2010;46(7):1223-1231.
[4]Belluco C, Nitti D, Frantz M, et al. Interleukin-6 blood level is associated with circulating carcinoembryonic antigen and prognosis in patients with colorectal cancer. Ann Surg Oncol. 2000;7(2):133-138.
[5]Wei LH, Kuo ML, Chen CA, et al. Interleukin-6 promotes cervical tumor growth by VEGF-dependent angiogenesis via a STAT3 pathway. Oncogene. 2003;22(10):1517-1527.
[6]Shinriki S, Jono H, Ota K, et al. Humanized anti-interleukin-6 receptor antibody suppresses tumor angiogenesis and in vivo growth of human oral squamous cell carcinoma. Clin Cancer Res. 2009;15(17):5426-5434.
[7]Duan Z, Lamendola DE, Penson RT, Kronish KM, Seiden MV. Overexpression of IL-6 but not IL-8 increases paclitaxel resistance of U-2OS human osteosarcoma cells. Cytokine. 2002;17(5):234-242.
[8]Liu H, Yan R, Xiao Z, et al. Targeting DCLK1 attenuates tumor stemness and evokes antitumor immunity in triple-negative breast cancer by inhibiting IL-6/STAT3 signaling. Breast Cancer Res. 2023;25(1):43.
[9]Song L, Rawal B, Nemeth JA, Haura EB. JAK1 activates STAT3 activity in non-small-cell lung cancer cells and IL-6 neutralizing antibodies can suppress JAK1-STAT3 signaling. Mol Cancer Ther. 2011;10(3):481-494.
[10]Thilakasiri P, Huynh J, Poh AR, et al. Repurposing the selective estrogen receptor modulator bazedoxifene to suppress gastrointestinal cancer growth. EMBO Mol Med. 2019;11(4):e9539.
[11]Wolf CL, Feci A, Tuccinardi JP, et al. Development of the First Small-Molecule Inhibitor Targeting Oncostatin M for Treatment of Breast Cancer. J Med Chem. 2025;68(15):15422-15445.
[12]Shi Y, Gao W, Lytle NK, et al. Targeting LIF-mediated paracrine interaction for pancreatic cancer therapy and monitoring. Nature. 2019;569(7754):131-135.
[13]Liang B, Gardner DB, Griswold DE, Bugelski PJ, Song XY. Anti-interleukin-6 monoclonal antibody inhibits autoimmune responses in a murine model of systemic lupus erythematosus. Immunology. 2006;119(3):296-305.
[14]Kitaba S, Murota H, Terao M, et al. Blockade of interleukin-6 receptor alleviates disease in mouse model of scleroderma. Am J Pathol. 2012;180(1):165-176.
[15]Elshabrawy HA, Volin MV, Essani AB, et al. IL-11 facilitates a novel connection between RA joint fibroblasts and endothelial cells. Angiogenesis. 2018;21(2):215-228.
[16]Liu Q, Du Y, Li K, et al. Anti-OSM Antibody Inhibits Tubulointerstitial Lesion in a Murine Model of Lupus Nephritis. Mediators Inflamm. 2017;2017:3038514.
[17]Okuno S, Hashimoto T, Yamazaki Y, Okuzawa M, Satoh T. IL-31 and IL-31 receptor alpha in pemphigus: Contributors to more than just itch?. J Dermatol. 2023;50(7):927-930.
[18]Fanola CL, Morrow DA, Cannon CP, et al. Interleukin-6 and the Risk of Adverse Outcomes in Patients After an Acute Coronary Syndrome: Observations From the SOLID-TIMI 52 (Stabilization of Plaque Using Darapladib-Thrombolysis in Myocardial Infarction 52) Trial. J Am Heart Assoc. 2017;6(10):e005637.
[19]Held C, White HD, Stewart RAH, et al. Inflammatory Biomarkers Interleukin-6 and C-Reactive Protein and Outcomes in Stable Coronary Heart Disease: Experiences From the STABILITY (Stabilization of Atherosclerotic Plaque by Initiation of Darapladib Therapy) Trial. J Am Heart Assoc. 2017;6(10):e005077.
[20]Li H, Liu W, Xie J. Circulating interleukin-6 levels and cardiovascular and all-cause mortality in the elderly population: A meta-analysis. Arch Gerontol Geriatr. 2017;73:257-262.
[21]Kobara M, Noda K, Kitamura M, et al. Antibody against interleukin-6 receptor attenuates left ventricular remodelling after myocardial infarction in mice. Cardiovasc Res. 2010;87(3):424-430.
[22]Ridker PM, Devalaraja M, Baeres FMM, et al. IL-6 inhibition with ziltivekimab in patients at high atherosclerotic risk (RESCUE): a double-blind, randomised, placebo-controlled, phase 2 trial. Lancet. 2021;397(10289):2060-2069.
[23]Miteva K, Baptista D, Montecucco F, et al. Cardiotrophin-1 Deficiency Abrogates Atherosclerosis Progression. Sci Rep. 2020;10(1):5791.
[24]Song K, Wang S, Huang B, Luciano A, Srivastava R, Mani A. Plasma cardiotrophin-1 levels are associated with hypertensive heart disease: a meta-analysis. J Clin Hypertens (Greenwich). 2014;16(9):686-692.
[25]Lim WW, Dong J, Ng B, et al. Inhibition of IL11 Signaling Reduces Aortic Pathology in Murine Marfan Syndrome. Circ Res. 2022;130(5):728-740.
[26]Zhang M, Wang C, Hu J, et al. Notch3/Akt signaling contributes to OSM-induced protection against cardiac ischemia/reperfusion injury. Apoptosis. 2015;20(9):1150-1163.
[27]Rolfe BE, Stamatiou S, World CJ, et al. Leukaemia inhibitory factor retards the progression of atherosclerosis. Cardiovasc Res. 2003;58(1):222-230.
[28]González GE, Rhaleb NE, D'Ambrosio MA, et al. Deletion of interleukin-6 prevents cardiac inflammation, fibrosis and dysfunction without affecting blood pressure in angiotensin II-high salt-induced hypertension. J Hypertens. 2015;33(1):144-152.
[29]Chen W, Yuan H, Cao W, et al. Blocking interleukin-6 trans-signaling protects against renal fibrosis by suppressing STAT3 activation. Theranostics. 2019;9(14):3980-3991.
[30]Wheeler DS, Misumi K, Walker NM, et al. Interleukin 6 trans-signaling is a critical driver of lung allograft fibrosis. Am J Transplant. 2021;21(7):2360-2371.
[31]Schafer S, Viswanathan S, Widjaja AA, et al. IL-11 is a crucial determinant of cardiovascular fibrosis. Nature. 2017;552(7683):110-115.
[32]Ng B, Dong J, D'Agostino G, et al. Interleukin-11 is a therapeutic target in idiopathic pulmonary fibrosis. Sci Transl Med. 2019;11(511):eaaw1237.
[33]Matsuda M, Tsurusaki S, Miyata N, et al. Oncostatin M causes liver fibrosis by regulating cooperation between hepatic stellate cells and macrophages in mice. Hepatology. 2018;67(1):296-312.
[34]Xu S, Yang X, Chen Q, et al. Leukemia inhibitory factor is a therapeutic target for renal interstitial fibrosis. EBioMedicine. 2022;86:104312.
[35]Perretta-Tejedor N, Muñoz-Félix JM, Düwel A, et al. Cardiotrophin-1 opposes renal fibrosis in mice: Potential prevention of chronic kidney disease. Acta Physiol (Oxf). 2019;226(2):e13247.