从免疫风暴到神经损伤:解码JAK激酶的“多病之源”角色
从免疫风暴到神经损伤:解码JAK激酶的“多病之源”角色
在之前的文章里,我们给大家分享了Janus激酶(JAK)家族蛋白结构、激活方式以及JAKs与肿瘤相关研究。https://www.cloud-clone.cn/topic/202506300813197766.html
本期为【JAK家族蛋白】第二期,将给大家分享JAK家族与自身免疫性疾病、过敏性疾病、纤维化疾病以及神经退行性疾病的相关研究。
JAKs是一类非受体酪氨酸激酶,包括JAK1、JAK2、JAK3和TYK2四种成员,它们通过与细胞因子受体的相互作用参与调控多种生物学过程,如造血、免疫反应、炎症以及细胞存活等。近年来,JAKs在多种疾病的发生发展中的作用逐渐被揭示。除恶性肿瘤外,在炎症性自身免疫性疾病(如类风湿关节炎、银屑病)、过敏性疾病、纤维化疾病以及神经退行性疾病中,JAK信号通路的异常活化成为关键驱动因素。随着针对JAKs的小分子抑制剂的研发和临床应用,JAKs在疾病治疗中的价值日益凸显,同时也引发了对其潜在副作用及长期疗效的关注。因此,深入探讨JAKs与疾病的关联机制不仅有助于阐明相关病理生理过程,还可能为新型靶向药物的设计提供重要依据。
1 JAKs与自身免疫性疾病
1.1 JAKs与银屑病
由于JAKs能够选择性调节免疫功能,靶向JAK抑制剂是某些皮肤病的潜在治疗方式。有研究评估了银屑病患者在接受窄带紫外线B疗法(NB-UVB)治疗前后的JAK1水平[1]。银屑病患者的JAK1水平显著高于正常对照组,NB-UVB治疗后JAK1水平下降。在银屑病患者中,JAK1水平与病程、银屑病面积和严重程度指数(PASI)变化呈正相关。据报道,用JAK3的小分子抑制剂R348治疗患有银屑病的小鼠,观察到治疗6周后皮肤病变明显减弱[2]。组织学分析显示,与对照相比,R348处理的CD18缺陷型PL/J小鼠(与人类银屑病相似的自发性T细胞依赖性银屑病样皮肤病)的表皮和真皮病变严重程度评分均显著降低。此外,在IL-23诱导的银屑病样皮肤炎症中,与野生型小鼠相比,注射IL-23的Tyk2-/-小鼠显示耳部皮肤肿胀伴表皮增生和炎性细胞浸润显著减少[3]。Tyk2缺陷减少了促炎细胞因子和银屑病相关抗菌肽的产生。小分子Tyk2抑制剂显著抑制IL-23诱导的皮肤炎症和细胞因子产生。这些发现表明JAKs抑制在人类银屑病中的治疗潜力。
1.2 JAKs与白癜风
一项研究使用免疫组织化学方法探讨JAK1在白癜风发病机制中的可能作用[4]。与正常皮肤相比,白癜风患者JAK1表达水平更高,并且JAK1高表达与较低的黑色素细胞百分比相关。这些结果提示JAK1可能参与白癜风的发病机制。白癜风皮肤T细胞分泌组下调黑色素细胞功能和粘附,同时增加黑色素细胞线粒体代谢和表皮细胞炎性细胞因子和趋化因子的表达。JAK1/2抑制剂Ruxolitinib强烈抑制了对表皮细胞的这种作用[5]。一项2b期临床试验(NCT03715829)评估了口服JAK3/TEC家族激酶抑制剂Ritlecitinib对活动性和非节段性白癜风患者活动性和稳定病灶的疗效[6]。与安慰剂相比,Ritlecitinib显著稳定了活动病灶和稳定病灶的脱色程度,稳定的病灶显示出更大的色素沉着,增加黑色素细胞标志物的表达。这些研究表明JAK抑制剂可以防止T细胞对表皮细胞和色素沉着的影响,突出了它们在白癜风中的潜在临床益处。
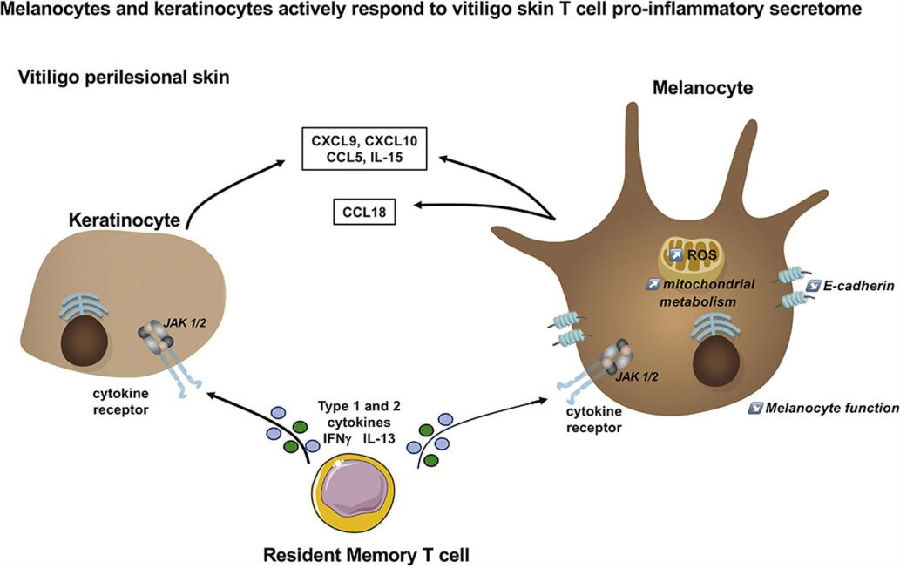
图1 白癜风皮肤T细胞通过细胞因子-JAK信号诱导黑色素细胞功能障碍和表皮炎症
(图片源于《Journal of Investigative Dermatology》[5])
1.3 JAKs与类风湿关节炎
细胞因子是类风湿性关节炎(RA)炎症和组织破坏的重要介质。参与RA发病机制的几种细胞因子通过JAK-STAT通路发挥作用。托法替尼是第一个为治疗RA而开发的JAK抑制剂。研究显示,托法替尼治疗显著降低细胞因子诱导的所有JAK-STAT通路的磷酸化,显著改善RA患者疾病活动评分[7]。一项Meta分析表明,与安慰剂相比,JAK抑制剂具有显著更好的治疗结果[8]。JAK单药治疗被证明比甲氨蝶呤、改善病情抗风湿药(DMARDs)更有效。此外,JAK抑制剂在改善RA患者疼痛上效果更显著,并且在安全性方面与其他RA常用药没有显著差异。有研究进一步探索了RA患者JAK抑制剂治疗效果和B细胞亚群的分布,并分析它们与疾病缓解的相关性[9]。RA患者呈现不同的B细胞亚群,其中未转换记忆B(NSMB)细胞的频率与疾病活动呈负相关。用JAK抑制剂治疗可以抑制NSMB细胞的活化,恢复激酶磷酸化的平衡,并促进RA患者的疾病缓解。另一项研究显示JAK抑制剂的给药减少了RA来源的成纤维细胞样滑膜细胞(RA-FLS)的VEGF产生并抑制了人脐静脉内皮细胞(HUVEC)迁移,抑制了RA-FLS和HUVEC共培养物中的新生血管形成[10]。这提示JAK抑制剂具有抗血管生成作用,为RA治疗提供了新的见解。
1.4 JAKs与系统性红斑狼疮
据报道,在两种系统性红斑狼疮(SLE)小鼠模型中,选择性JAK2抑制剂CEP-33779治疗可延长生存期并减少脾肿大/淋巴肿大[11]。CEP-33779治疗后几种血清细胞因子显著降低,抗核抗体和自身抗原特异性、分泌抗体的细胞的频率下降。CEP-33779治疗能够减轻与SLE进展相关的几个免疫参数,有效改善狼疮性肾炎小鼠的疾病进展。SLE患者早发心血管疾病(CVD)的风险增加已得到充分认识。一项临床研究探索了JAK抑制剂托法替尼治疗SLE的安全性、耐受性、临床反应和相关机制,发现托法替尼在SLE中具有较好的安全性,并改善了与SLE早发动脉粥样硬化相关的心脏代谢和免疫参数[12]。另一项临床研究评估了氘可来昔替尼(TYK2抑制剂)在成年活动性SLE患者中的疗效和安全性[13]。与安慰剂相比,氘可来昔替尼治疗在活动性SLE成年患者中引发了更高的SLE应答者指数-4(SRI-4)和其他终点反应率,具有可接受的安全性。这些数据表明JAK抑制剂对于SLE具有较好的治疗效果和安全性。
1.5 JAKs与其他自身免疫疾病
原发性干燥综合征(SS)是一种全身性自身免疫性疾病,其特征是外分泌腺功能障碍,导致患者出现干燥症状。通过病灶评分评估,原发性SS患者唾液腺中干扰素γ(IFNg)和B细胞活化因子(BAFF)的表达增加[14]。JAK抑制剂可抑制IFN诱导的人原代唾液腺上皮细胞(SGEC)中BAFF的转录,导致人唾液腺类器官培养物中BAFF的分泌减少。此外,非戈替尼(JAK1抑制剂)处理的SS模型小鼠表现出唾液流速增加和唾液腺淋巴细胞浸润的显著减少。这些结果表明JAK抑制控制SGEC的异常激活,可能是原发性SS的一种新型治疗方法。
难治性慢性自身免疫性疾病系统性硬化症(SSc)的特征是广泛器官纤维化和血管内皮增生引起的血管病。吡西替尼是一种新型JAK抑制剂。有研究表征了吡西替尼的药理学特性,并发现JAK/STAT通路在SSc中被组成型激活[15]。吡西替尼抑制各种细胞因子诱导的STAT磷酸化,还抑制外周血单核细胞和皮肤成纤维细胞产生细胞因子和趋化因子。这提示JAK抑制剂可能作为SSc的新型治疗选择。
巨细胞动脉炎是主动脉及其大分支的一种慢性自身免疫性疾病,并发动脉瘤形成、夹层和动脉闭塞。据报道,JAK抑制剂托法替尼能有效抑制携带发炎人动脉的免疫缺陷小鼠血管壁中的先天免疫和适应性免疫[16]。托法替尼抑制病变区域T细胞增殖,降低效应因子的表达。托法替尼破坏了外膜微血管生成,减少了增生性内膜的生长,有效抑制组织驻留的记忆T细胞。这些结果表明JAK抑制剂通过靶向失调的T细胞有望成为动脉炎的潜在治疗方式。
2 JAKs与过敏性疾病
哮喘的一个亚群是由2型细胞因子驱动的,这些细胞因子依赖于JAK1的信号转导。因此,研究者探讨了肺限制性JAK1抑制可能会带来治疗益处[17]。iJak-381(肺部局部JAK1抑制剂)在小鼠和豚鼠哮喘模型中抑制卵清蛋白诱导的肺部炎症,并改善了过敏原诱导的小鼠气道高反应性。另一项研究探讨吸入途径抑制JAK是否足以抑制气道炎症[18]。LAS194046是一种选择性吸入pan-JAK抑制剂,可减少大鼠卵清蛋白模型中过敏原诱导的气道炎症、晚期哮喘反应和STAT激活。这些结果表明,在没有相关全身暴露的情况下,局部抑制肺部的JAK足以减轻哮喘模型中的肺部炎症并改善肺功能。
过敏性鼻炎(AR)是一种上气道炎症性疾病。JAK1被发现参与免疫反应和过敏性气道疾病的发展。研究者评估中国汉族人群中JAK1多态性与AR的潜在关联[19]。在中国汉族人群中检测到JAK1基因中的SNP rs310241与AR之间存在关联。对于rs310241,CC基因型和C等位基因显著增加了AR的风险,与AR易感性有关。CP-690550是一种JAK3小分子抑制剂。研究显示,在卵清蛋白抗原致敏和增强期间服用CP-690550的小鼠支气管肺泡灌洗液(BAL)嗜酸性粒细胞以及IL-13和嗜酸性粒细胞趋化因子水平的显著降低[20]。研究数据表明JAK3参与导致过敏小鼠模型中肺嗜酸性粒细胞增多的过程。这提示CP-690550可用于治疗与气道嗜酸性粒细胞增多症相关的过敏性疾病,包括哮喘和鼻炎。
3 JAKs与纤维化疾病
JAK1和JAK2作为成纤维细胞相关标志物与纤维化和癌症有关。据报道,JAK1/2表达与人类肝细胞癌的进展和小鼠肝纤维化水平呈正相关[21]。JAK1/2的沉默下调了下游信号传导,并在体外抑制了肝星状细胞(HSC)的增殖、迁移和激活,而Ruxolitinib对HSC也有类似的作用。Ruxolitinib显著减轻了CCl4或TAA处理的小鼠肝脏的纤维化进展,改善了细胞损伤,加速了纤维化逆转。
特发性肺纤维化(IPF)是进展最快且致命的纤维化疾病之一。研究显示,JSI-124对p-JAK2/p-STAT3的双重抑制或JAK2和STAT3基因的沉默抑制了Ⅱ型肺泡上皮细胞(ATII)和成纤维细胞向肌成纤维细胞的转变[22]。双重抑制比单一抑制更有效地抑制成纤维细胞迁移,防止成纤维细胞衰老和Bcl-2表达的增加,改善受损的自噬。在博来霉素诱导的肺纤维化大鼠模型中,JSI-124给药后肺纤维化减少,肺中的胶原沉积受到抑制。
在单侧输尿管梗阻(UUO)模型和TGF-β1处理的成纤维细胞和肾小管上皮细胞中,Ruxolitinib治疗抑制UUO肾脏和TGF-β1处理的成纤维细胞中的成纤维细胞活化和细胞外基质(ECM)的产生[23]。Ruxolitinib治疗还阻断了UUO肾脏和TGF-β1处理的肾小管上皮细胞中的上皮-间充质转化(EMT),减轻了UUO诱导的炎症、氧化应激和细胞凋亡。这些结果表明Ruxolitinib可能用于治疗纤维化肾病。
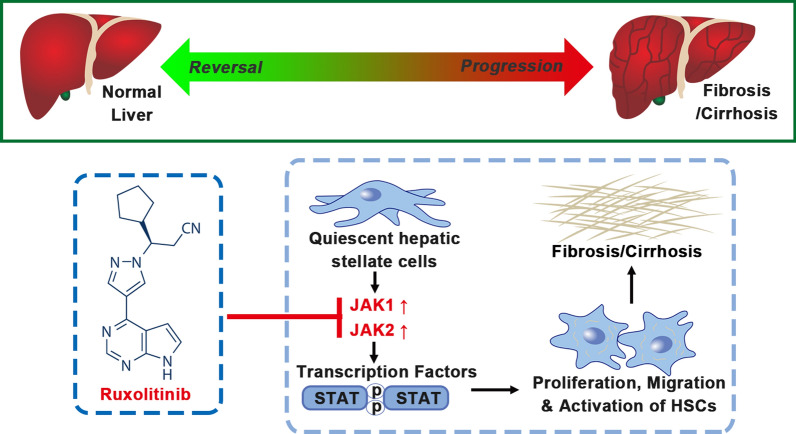
图2 Ruxolitinib通过选择性靶向JAK1/2抑制肝纤维化进展并加速纤维化逆转
(图片源于《Journal of Translational Medicine》[21])
4 JAKs与神经退行性疾病
帕金森病(PD)是一种与年龄相关的慢性神经退行性疾病。使用α-突触核蛋白(α-SYN)过表达PD模型,研究团队证明JAK1/2的特异性抑制剂AZD1480在抑制神经炎症和神经退行性变方面的有益治疗作用[24]。抑制JAK/STAT通路通过抑制α-SYN诱导的小胶质细胞和巨噬细胞活化以及CD4+ T细胞募集到中枢神经系统(CNS)来影响先天性和适应性免疫反应,最终抑制神经退行性变。这些发现表明JAK抑制剂可能是治疗PD患者的可行治疗选择。
神经炎症在淀粉样蛋白β(Aβ)斑块的形成中起着关键作用,这是阿尔茨海默病(AD)的标志之一。选择性JAK2/STAT3抑制剂巴瑞克替尼减轻了卵巢切除/D-半乳糖(OVX/D-gal)诱导的AD大鼠模型中JAK2/STAT3信号通路的异常激活,导致p-JAK和p-STAT3水平的表达显著降低[25]。巴瑞克替尼给药还成功地逆转了由OVX/D-gal引起的组织病理学改变,增加了完整神经元的数量,降低了Aβ水平并改善AD大鼠模型的认知障碍。这些结果提示抑制JAK2/STAT3可能在AD治疗中起着至关重要的作用。
基因C9ORF72中的六核苷酸重复扩增是肌萎缩侧索硬化症(ALS)和额颞叶变性(FTLD)的主要原因。C9ORF72缺陷会导致小鼠出现严重的炎症表型。据报道,C9ORF72缺失导致JAK-STAT通路的过度激活和STING蛋白水平的增加[26]。用JAK抑制剂治疗可挽救细胞培养物和小鼠中由C9ORF72缺陷引起的增强炎症表型。C9ORF72消融会导致溶酶体完整性受损,这可能导致JAK/STAT依赖性炎症反应的激活。这项研究确定了C9ORF72调节炎症的一种机制,靶向抑制JAK可能有助于C9ORF72突变的ALS/FTLD的治疗开发。
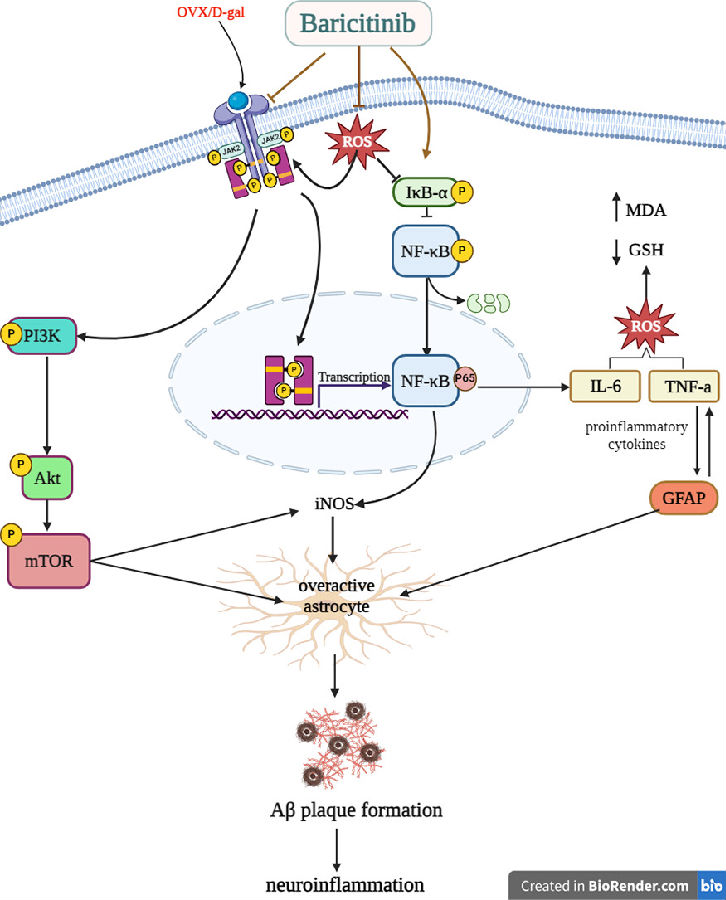
图3 巴瑞克替尼治疗改善AD大鼠模型记忆障碍
(图片源于《Life Sciences》[25])
云克隆助力科学研究,为广大科研人员提供相关检测试剂产品,相关靶标核心货号如下:
靶标 | 核心货号 | 靶标 | 核心货号 |
JAK1 | C551 | CISH | C383 |
JAK2 | F494 | IRF9 | H780 |
JAK3 | F493 | PIAS1 | B736 |
TYK2 | B595 | PIAS3 | E590 |
STAT1 | B740 | PIAS4 | E591 |
STAT2 | B796 | PTPN11 | D584 |
STAT3 | B743 | PTPN2 | D585 |
STAT4 | B739 | PTPN6 | D589 |
STAT5A | B738 | SOCS1 | H158 |
STAT5B | B727 | SOCS2 | H154 |
STAT6 | B737 | SOCS3 | B684 |
更多科研试剂,欢迎访问云克隆官方网站:http://www.cloud-clone.cn/
参考文献
[1]Nada HR, El Sharkawy DA, Elmasry MF, Rashed LA, Mamdouh S. Expression of Janus Kinase 1 in vitiligo & psoriasis before and after narrow band UVB: a case-control study. Arch Dermatol Res. 2018;310(1):39-46.
[2]Chang BY, Zhao F, He X, et al. JAK3 inhibition significantly attenuates psoriasiform skin inflammation in CD18 mutant PL/J mice. J Immunol. 2009;183(3):2183-2192.
[3]Ishizaki M, Muromoto R, Akimoto T, et al. Tyk2 is a therapeutic target for psoriasis-like skin inflammation. Int Immunol. 2014;26(5):257-267.
[4]Abdou AG, Maraee A, Yassien H, Sarhan M. Immunohistochemistry of Janus Kinase 1 (JAK1) Expression in Vitiligo. J Pathol Transl Med. 2018;52(6):363-368.
[5]Martins C, Migayron L, Drullion C, et al. Vitiligo Skin T Cells Are Prone to Produce Type 1 and Type 2 Cytokines to Induce Melanocyte Dysfunction and Epidermal Inflammatory Response Through Jak Signaling. J Invest Dermatol. 2022;142(4):1194-1205.e7.
[6]Yamaguchi Y, Peeva E, Duca ED, et al. Ritlecitinib, a JAK3/TEC family kinase inhibitor, stabilizes active lesions and repigments stable lesions in vitiligo. Arch Dermatol Res. 2024;316(7):478.
[7]Palmroth M, Kuuliala K, Peltomaa R, et al. Tofacitinib Suppresses Several JAK-STAT Pathways in Rheumatoid Arthritis In Vivo and Baseline Signaling Profile Associates With Treatment Response. Front Immunol. 2021;12:738481.
[8]Tóth L, Juhász MF, Szabó L, et al. Janus Kinase Inhibitors Improve Disease Activity and Patient-Reported Outcomes in Rheumatoid Arthritis: A Systematic Review and Meta-Analysis of 24,135 Patients. Int J Mol Sci. 2022;23(3):1246.
[9]Luo J, Zhang J, Ju B, et al. JAK inhibitors attenuate hyperactivation of nonswitched memory B cells in rheumatoid arthritis patients in remission. Arthritis Res Ther. 2024;26(1):134.
[10]Anjiki K, Hayashi S, Ikuta K, et al. JAK inhibitors inhibit angiogenesis by reducing VEGF production from rheumatoid arthritis-derived fibroblast-like synoviocytes. Clin Rheumatol. 2024;43(11):3525-3536.
[11]Lu LD, Stump KL, Wallace NH, et al. Depletion of autoreactive plasma cells and treatment of lupus nephritis in mice using CEP-33779, a novel, orally active, selective inhibitor of JAK2. J Immunol. 2011;187(7):3840-3853.
[12]Hasni SA, Gupta S, Davis M, et al. Phase 1 double-blind randomized safety trial of the Janus kinase inhibitor tofacitinib in systemic lupus erythematosus. Nat Commun. 2021;12(1):3391.
[13]Morand E, Pike M, Merrill JT, et al. Deucravacitinib, a Tyrosine Kinase 2 Inhibitor, in Systemic Lupus Erythematosus: A Phase II, Randomized, Double-Blind, Placebo-Controlled Trial. Arthritis Rheumatol. 2023;75(2):242-252.
[14]Lee J, Lee J, Kwok SK, et al. JAK-1 Inhibition Suppresses Interferon-Induced BAFF Production in Human Salivary Gland: Potential Therapeutic Strategy for Primary Sjögren's Syndrome. Arthritis Rheumatol. 2018;70(12):2057-2066.
[15]Kitanaga Y, Imamura E, Nakahara Y, et al. In vitro pharmacological effects of peficitinib on lymphocyte activation: a potential treatment for systemic sclerosis with JAK inhibitors. Rheumatology (Oxford). 2020;59(8):1957-1968.
[16]Zhang H, Watanabe R, Berry GJ, Tian L, Goronzy JJ, Weyand CM. Inhibition of JAK-STAT Signaling Suppresses Pathogenic Immune Responses in Medium and Large Vessel Vasculitis. Circulation. 2018;137(18):1934-1948.
[17]Dengler HS, Wu X, Peng I, et al. Lung-restricted inhibition of Janus kinase 1 is effective in rodent models of asthma. Sci Transl Med. 2018;10(468):eaao2151.
[18]Calbet M, Ramis I, Calama E, et al. Novel Inhaled Pan-JAK Inhibitor, LAS194046, Reduces Allergen-Induced Airway Inflammation, Late Asthmatic Response, and pSTAT Activation in Brown Norway Rats. J Pharmacol Exp Ther. 2019;370(2):137-147.
[19]Shen Y, Liu Y, Ke X, Kang HY, Hu GH, Hong SL. Association between JAK1 gene polymorphisms and susceptibility to allergic rhinitis. Asian Pac J Allergy Immunol. 2016;34(2):124-129.
[20]Kudlacz E, Conklyn M, Andresen C, Whitney-Pickett C, Changelian P. The JAK-3 inhibitor CP-690550 is a potent anti-inflammatory agent in a murine model of pulmonary eosinophilia. Eur J Pharmacol. 2008;582(1-3):154-161.
[21]Song Z, Liu X, Zhang W, et al. Ruxolitinib suppresses liver fibrosis progression and accelerates fibrosis reversal via selectively targeting Janus kinase 1/2. J Transl Med. 2022;20(1):157.
[22]Milara J, Hernandez G, Ballester B, et al. The JAK2 pathway is activated in idiopathic pulmonary fibrosis. Respir Res. 2018;19(1):24.
[23]Bai Y, Wang W, Yin P, et al. Ruxolitinib Alleviates Renal Interstitial Fibrosis in UUO Mice. Int J Biol Sci. 2020;16(2):194-203.
[24]Qin H, Buckley JA, Li X, et al. Inhibition of the JAK/STAT Pathway Protects Against α-Synuclein-Induced Neuroinflammation and Dopaminergic Neurodegeneration. J Neurosci. 2016;36(18):5144-5159.
[25]Hindam MO, Ahmed LA, El Sayed NS, Khattab M, Sallam NA. Repositioning of baricitinib for management of memory impairment in ovariectomized/D-galactose treated rats: A potential role of JAK2/STAT3-PI3K/AKT/mTOR signaling pathway. Life Sci. 2024;351:122838.
[26]Pang W, Hu F. C9ORF72 suppresses JAK-STAT mediated inflammation. iScience. 2023;26(5):106579.