氧化钨纳米颗粒(WO3NPs)在炎症性肠病中的治疗潜力

文献导读
2021年6月18日,来自国家纳米科学中心的聂广军研究员及其团队在国际期刊《nano today》上发表了题为“Colonic mucus-accumulating tungsten oxide nanoparticles improve the colitis therapy by targeting Enterobacteriaceae”的文章。

研究介绍
炎症性肠病(IBD)是一种非特异性的慢性肠道炎性疾病,主要包括溃疡性结肠炎和克罗恩病。其特征是肠屏障功能中断和之久的粘膜炎症。在我国,IBD的发病率和患病率急剧上升。尽管IBD的病因和发病机制尚不清楚,但越来越多的证据表明,生物失调诱导的肠道炎症和渗漏是引发IBD发展的重要因素。兼性厌氧肠杆菌科(Enterobacteriaceae),如大肠杆菌(Escherichia coli, E. coli)的失调加重了肠道炎症,加剧了肠道屏障损伤,这也会影响结直肠癌的进展。这些发现使人们开始重视基于微生物疗法(MBT)的开发,旨在通过精准靶向炎性结肠中溃疡相关肠杆菌科的细菌呼吸和能量代谢来治疗IBD。
传统的MBT治疗方法主要侧重于广谱抗生素,以预防肠道致病性感染。然而,在IBD治疗中使用抗生素也会清除有益的肠道微生物。因此,这种非特异性策略增加了病原体扩散和抗生素耐药性的风险。更重要的是,耐药菌的增加已经成为人类健康的最大威胁之一。因此,靶向抑制致病菌的生长和调节肠道微生物稳态是干预IBD进展的新策略。
氧化钨纳米颗粒(WO3NPs)因其独特的理化性质以及在生物传感器、光声成像和肿瘤治疗等生物医学领域的巨大应用潜力而备受关注。因此,作者探索了WO3NPs在DSS诱导的急性结肠炎小鼠中的治疗潜力。
作者研究发现与钨酸钠(Na2WO4)相比,WO3NPs(直径47.9 nm)显著减少了炎症,减弱了细菌易位,恢复了结肠上皮屏障,重塑了炎症结肠中的肠道微生物稳态。重要的是,WO3NPs通过选择性抑制肠道细菌呼吸和能量代谢,特异性积聚在黏液层,引起全身毒性最小,提高了钨酸盐对急性结肠炎的治疗效果,干预了IBD的进展。与Na2WO4、5-ASA和ZnONPs相比,WO3NPs对急性结直肠炎的治疗效果更强。因此,WO3NPs可能作为一种安全、有效的MBT纳米药物用于IBD的临床治疗。


肠胃病学
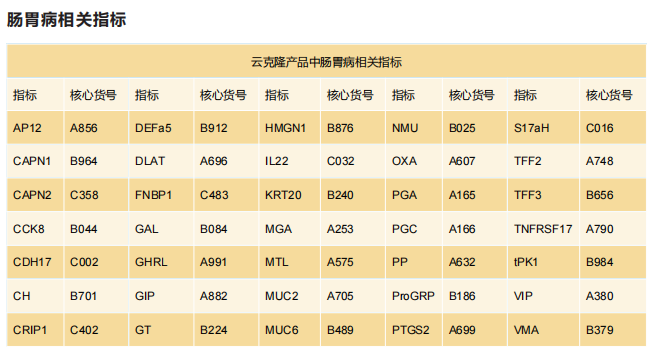
胃肠道疾病主要指一般炎症性胃肠道疾病(急、慢性胃炎,急、慢性阑尾炎等)、消化性溃疡、胃癌、食道癌、大肠癌及肠易激综合征等。一般炎症性的肠胃炎主要是由于外界刺激引起的炎症反应,会破坏消化道的内表皮细胞,导致消化道内表皮和内基质损伤,表现出肠胃病。与此同时随着内皮和基质细胞的损伤,细胞基质中的蛋白也会出现粪便或者血清中,只需要检测这些样本中标志性蛋白的含量,就可以很容易判断疾病的发展及轻重。比如胃粘膜损伤:在粪便和血清中胃蛋白酶(PP)、胃泌素释放肽前体(ProGRP)的含量都有所上升。目前科研结果表明,胃肠道癌症的发生与长期的炎症、遗传因素等密切相关。癌细胞在生长、分裂以及迁移的过程中,会分泌特异性的物质或者刺激宿主细胞产生特有的物质,这类物质我们成为TM(Tumor marker, 肿瘤标志物),对这些物质的检测能反映癌症发生、发展,以及癌症对治疗药物的反应。
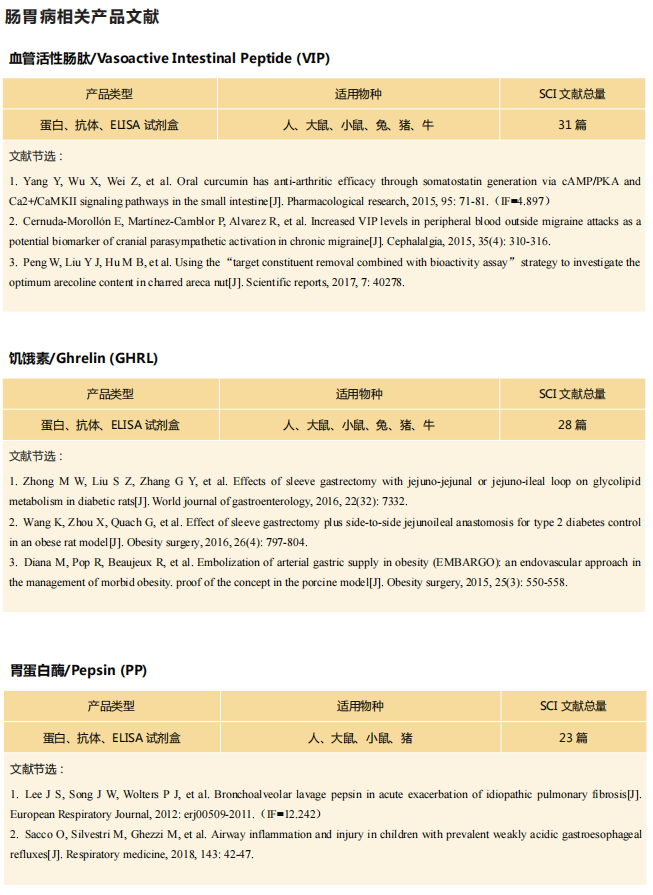
云克隆提供肠胃病相关的多种指标蛋白、抗体以及ELISA试剂盒产品,广泛的应用于人、小鼠、大鼠、猪、羊等多个物种的检测。目前客户使用云克隆肠胃病相关指标产品发表的SCI文献已超过240篇。