文献解读 | 肝骨轴缺陷导致肝性骨营养不良疾病进展

2022年3月1日,南京大学医学院附属南京鼓楼医院Qing Jiang、南京医科大学邵逸夫医院Bin Xue、南京大学医学院模型动物研究中心Chao-Jun Li和中国科学院深圳先进技术研究所药学院Di Chen及团队联合在《Cell Metabolism》上发表题为“Defects in a liver-bone axis contribute to hepatic osteodystrophy disease progression”的文章,表明可以针对肝性骨营养不良期间发生肝骨轴缺陷改善疾病进展。

在这篇文章中,云克隆试剂盒【Ⅰ型胶原交联羧基端肽(CTXI)检测试剂盒(酶联免疫吸附试验法),CEA665Mu;卵磷脂胆固醇脂酰转移酶(LCAT)检测试剂盒(酶联免疫吸附试验法),SEJ516Hu/SEJ516Mu】受到科研工作者的认可,荣登优秀国际期刊。


研究简介
代谢稳定性对于维持身体稳态非常重要。肝脏作为代谢中心,通过与多个器官相互作用以调节身体稳态。另一个重要的代谢器官是骨骼,已被证明具有重要的内分泌功能。研究表明肝脏和骨骼之间存在一条信号轴,调节它们各自的功能。肝性骨营养不良(HOD)是一种与慢性肝病相关的代谢性骨病,通常以骨质减少或骨质疏松症为特征。目前HOD的临床治疗仅限于补充VitD和Ca2+或双膦酸盐治疗。但这些治疗并非基于大型多中心随机对照试验的结果,反映了HOD 治疗需求的未得到满足。因此,了解肝骨轴调节缺陷的分子机制是开发更有效治疗HOD方法的关键。
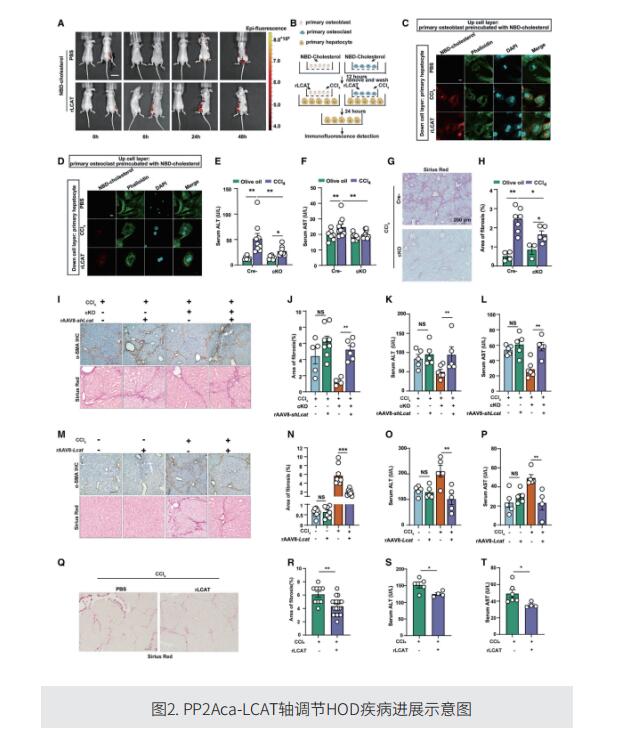
作为蛋白磷酸酶家族的重要成员,PP2A 调节 90% 的真核蛋白去磷酸化事件。PP2A催化亚基PP2Aca在心肌细胞的Ca2+平衡和骨骼肌的胰岛素抵抗中起重要作用。在之前的研究中,作者发现 PP2Aca 通过 AKT-GSK3b-Cyclin D1 通路参与肝脏再生。在这项研究中,他们使用基于蛋白质组学的方法来分析 HOD 患者肝脏中蛋白质表达的变化,发现 PP2Aca 蛋白表达显著增加,蛋白磷酸化发生显著变化。体内研究表明,PP2Aca 抑制可诱导 LCAT 表达,并且 LCAT 不仅可以防止骨质流失,还可以改善慢性肝损伤。相反,LCAT 功能的丧失显著加剧了 HOD 的这些表型变化。从机制上讲,LCAT 表达受到 PP2Aca 介导的 USF1 去磷酸化的负调控。此外,作者发现胆固醇水平改变与成骨细胞和破骨细胞活性的调节有关。LCAT 通过促进胆固醇从骨骼到肝脏的转运逆转来改善小鼠 HOD 模型中的肝功能并缓解肝纤维化。
综上所述,作者提出肝脏 PP2Aca 表达可能通过 LCAT 影响骨代谢。这些结果有助于阐明HOD的发病机制,同时阐明肝脏和骨骼之间新的代谢信号轴的机制,可能为HOD的治疗提供新的治疗靶点。