动脉粥样硬化治疗新靶点
动脉粥样硬化(AS)是心血管疾病的主要原因。内皮功能障碍和血管炎症在AS的发生发展中起着至关重要的作用。AS由内皮细胞 (EC) 通过修饰的脂质激活而引发,激活的 EC 释放趋化因子,将免疫细胞募集到称为内膜的内皮下空间。募集的白细胞产生炎症介质,从而增强动脉部位的慢性炎症过程,协调单核细胞向巨噬细胞的分化、泡沫细胞的形成、迁移和平滑肌细胞的增殖。随着疾病的进展,复杂的炎症环境导致不稳定病变的破裂和随后的血栓形成,这可能导致严重的临床并发症。因此,探索AS形成机制,寻找可用的治疗靶点有助于预防和改善心血管相关疾病。
1. BACH1缺陷通过减少内皮炎症减轻AS
转录因子BACH1可抑制EC增殖和迁移并损害血管生成。复旦大学基础医学院Dan Meng团队利用EC特异性Bach1基因敲除AS小鼠模型研究BACH1在调节AS形成中的作用及其潜在机制[1]。内皮BACH1缺乏会降低湍流血流或饮食诱导的AS病变、斑块中的巨噬细胞含量、内皮粘附分子的表达,并降低AS小鼠血浆 TNF-α和 IL-1β 水平。机制研究表明,在振荡剪切应力或 TNF-α 刺激下,BACH1 通过与 YAP 启动子结合上调 YAP 表达,并与 YAP 形成复合物,诱导粘附分子的转录(图1)。EC 中的 YAP 过表达抵消了BACH1 缺失介导的小鼠抗AS作用。瑞舒伐他汀通过上调 EC 中的 microRNA let-7a 抑制 BACH1 表达,并降低高脂血症小鼠血管内皮中BACH1 的表达。这些数据将 BACH1 鉴定为血流动力学压力的机械传感器,并揭示 BACH1-YAP 转录网络对血管炎症和AS形成至关重要,显示出BACH1作为AS新治疗靶点的潜力。

2. 嗅觉受体 2 通过 NLRP3 依赖性 IL-1 的产生驱动AS
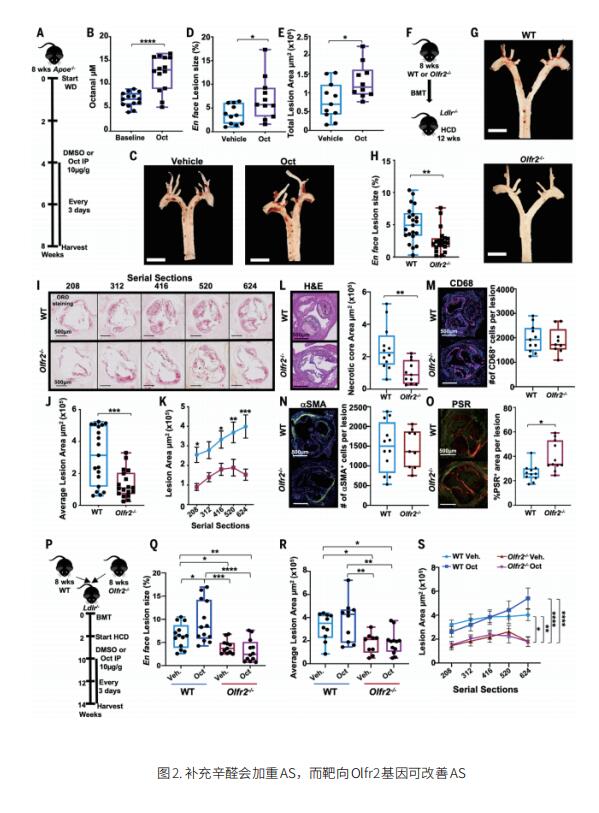
嗅觉受体 (OLFR) 是 G 蛋白偶联的化学感受器,在检测气味和嗅觉方面具有重要作用。 美国拉霍亚免疫学研究所Klaus Ley团队发现小鼠血管巨噬细胞表达嗅觉受体 Olfr2 和所相关的运输和信号分子[2]。他们证明小鼠中的Olfr2 和人血管巨噬细胞中的 OR6A2 (Olfr2人类直系同源嗅觉受体) 可响应辛醛,与 TLR4 结合诱导NLRP3炎症小体激活,从而导致 IL-1a 和 IL-1b 的产生和分泌。辛醛的来源可能是AS进展过程中油酸的脂质过氧化。提高辛醛水平会加剧AS,而靶向小鼠中 Olfr2 的基因可显著减少AS斑块(图2)。这一研究结果表明,OR6A2 和其他 OLFR 可能是治疗、预防和逆转AS的新治疗靶点。
3. 表观遗传酶 DOT1L 协调血管平滑肌细胞-单核细胞串扰并通过 NF-κB 通路防止AS
AS的一个标志是新内膜形成,即血管平滑肌细胞 (VSMC) 的增生,导致血管腔逐渐变窄甚至闭塞。DOT1L是一种组蛋白H3K79甲基转移酶。意大利 IRCCS Humanitas研究医院Leonardo Elia团队旨在确定 DOT1L 是否调节VSMC 表型以及它如何在体外和体内影响AS及相关机制[3]。对血小板衍生生长因子BB亚型刺激的VSMC进行基因表达筛选,他们发现DOT1L是一个早期上调的表观遗传因子。对小鼠和人动脉粥样硬化病变进行DOT1L表达评估,发现其特异性定位于VSMC间室。DOT1L 的失活显著降低AS小鼠疾病进展。通过结合 RNA 和染色质免疫沉淀测序,他们发现 DOT1L 及其诱导的 H3K79me2 标记直接调节炎症主要调节剂 Nf-κB-1 和 -2 的转录,进而诱导参与AS发展的细胞因子CCL5 和 CXCL10的表达(图3)。这些结果揭示DOT1L在VSMC基因表达的表观遗传调控中起关键作用,导致AS的发展,表明DOT1L是可作为血管疾病的潜在治疗靶点。

参考文献
[1]Jia M, Li Q, Guo J, et al. Deletion of BACH1 Attenuates Atherosclerosis by Reducing Endothelial Inflammation [J]. Circ Res. 2022, CIRCRESAHA121319540. (IF=17.364)
[2]Orecchioni M, Kobiyama K, Winkels H, et al. Olfactory receptor 2 in vascular macrophages drives atherosclerosis by NLRP3-dependent IL-1 production. Science. 2022, 375(6577):214-221. (IF=47.728)
[3]Farina FM, Serio S, Hall IF, et al. The epigenetic enzyme DOT1L orchestrates vascular smooth muscle cell-monocyte crosstalk and protects against atherosclerosis via the NF-κB pathway [J]. Eur Heart J. 2022, ehac097. (IF=29.983)
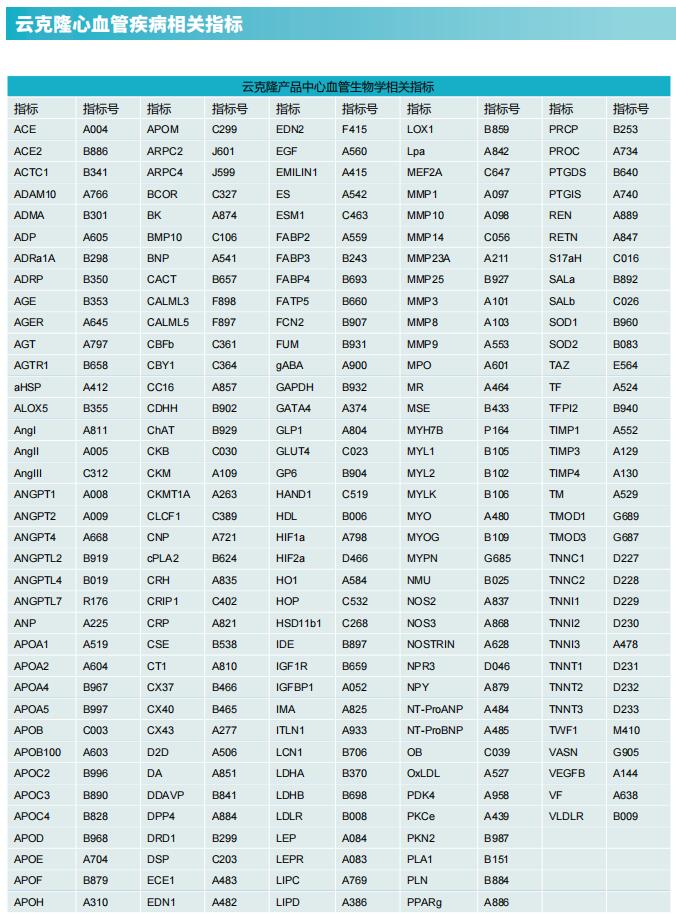
云克隆不仅可提供多种心血管系统疾病模型,包括高血脂及动脉粥样硬化、高血压、心肌肥厚、心肌梗死、心律失常、心力衰竭等,涵盖常见心血管系统疾病。还具有各类心血管系统信号通路常用指标及炎症指标相关产品,可助力广大科研工作者进行心血管系统疾病研究。