Science 新发现:铜死亡
我们前面为大家介绍过铁死亡,其发生的生物学基础是细胞内脂质活性氧(reactive oxygen species,ROS)生成与降解的平衡失调,具有铁离子依赖性。却很少有人知道铜死亡,铜死亡是依赖铜的,铜过量如何诱发细胞死亡目前尚不清楚。
1. 铜死亡概念的提出
2022年3月,麻省理工学院和哈佛大学Broad研究所Peter Tsvetkov和Todd R. Golub团队在《Science》上在线发表“Copper induces cell death by targeting lipoylated TCA cycle proteins”,首次提出细胞死亡的新感念——铜死亡。
铜死亡是依赖于铜的,通过铜离子直接结合三羧酸循环途径中的脂酰化成分,导致脂酰化蛋白异常聚集以及铁硫簇蛋白的丢失,从而导致蛋白质毒性应激反应最终导致细胞死亡的新的死亡方式。
2. 铜死亡的机制
2.1 依赖于铜离子的过度积累
首先利用不同结构的铜离子载体对489种细胞系进行实验,证明了铜离子载体可以诱导并介导细胞死亡。研究人员进一步发现,这种新的细胞死亡不同于之前发现的细胞调亡、细胞坏死、细胞焦亡和铁死亡,铜离子载体的细胞死亡不需要caspase 3的激活,也不需要细胞凋亡关键因子BAX和BAK1,并且,使用各种的细胞死亡方式的抑制剂均不能阻止这种新的细胞死亡。
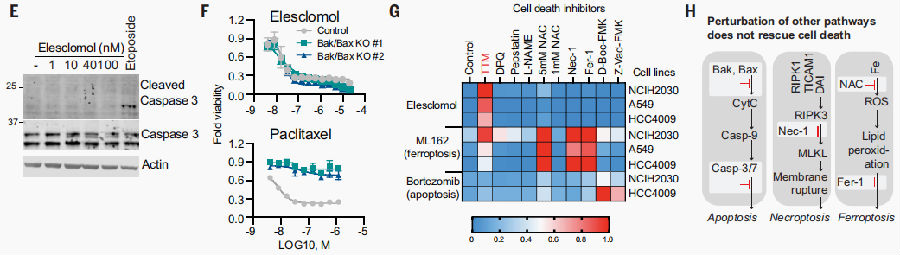
2.2 线粒体呼吸在三羧酸循环中发挥关键作用
研究发现依赖线粒体呼吸的细胞对铜离子的敏感性比正在进行糖酵解的细胞高近1000倍。使用线粒体抗氧化剂、脂肪酸以及线粒体功能抑制剂处理细胞,会显著影响细胞对铜离子载体的敏感性。重要的是,线粒体解偶联剂FCCP对铜离子诱导的细胞死亡没有影响,即铜离子依赖的细胞死亡需要线粒体呼吸而不需要ATP合成。铜离子载体的处理并没有显著降低基础呼吸或与ATP 相关的呼吸,但却显著降低了呼吸潜力,这就说明铜离子不会直接作用于电子传递链(ETC),而是在三羧酸(TCA)循环中发挥作用。
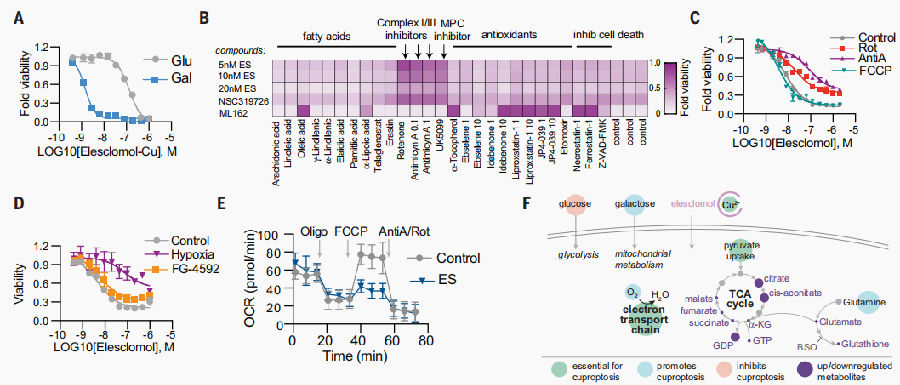
2.3 铜离子诱导细胞死亡的关键基因
为筛选铜诱导细胞死亡的基因,进行了全基因组 CRISPR-Cas9 loss-of-function,并结合knock out验证,最终确定铜死亡的两个关键基因:FDX1和LIAS。
FDX1,可编码还原酶,将 Cu2+ 还原为毒性更强的Cu1+,而且是铜离子载体(elesclomol)的直接靶标。LIAS,硫辛酸合成酶,定位于线粒体,是一种有效的线粒体抗氧化剂,催化硫辛酸的合成。脂酰化是线粒体蛋白特有的一种翻译后修饰,这个修饰依赖于硫辛酸。
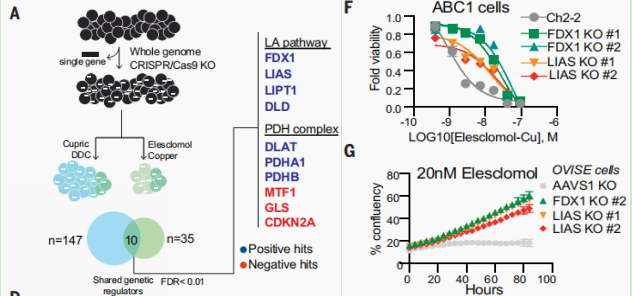
研究团队将这种新发现的细胞死亡命名为——Cuproptosis,该死亡方式跟以往发现的细胞死亡均不同,依赖于细胞内铜离子的积累,铜离子直接作用于三羧酸循环(TCA)并确定了是铜死亡的关键调控因子。然而,铜死亡的深入研究还需要科研人员的进一步探索,例如,为什么铜离子积累会作用于有氧呼吸?
铜死亡相关云克隆靶标如下:
靶标 | 靶标号 | 靶标 | 靶标号 |
FDX1 | C475 | LIAS | G355 |
DLD | A919 | DLAT | A696 |
PDHA1 | A776 | PDHb | B923 |
MTF1 | C633 | GLS | J026 |
CDKN2A | A794 | PDHA1 | A776 |
MPC1 | Q978 | SLC31A1 | E493 |
Atp7b | G386 | Hsp70 | A873 |
SDHB | J756 | POLD1 | C717 |