免疫反应的重要调节因子-SLAM家族受体
信号淋巴细胞活化分子(SLAM) 家族受体(SFRs)在多种造血细胞表达,包括T淋巴细胞、NK细胞和巨噬细胞,由9种跨膜蛋白(SLAMF1-9)组成,除SLAMF2是SLAMF4的受体外,大多数SLAMF可作为自身配体。其在细胞质的尾部结构与SLAM相关蛋白(SAP)、其同系物尤因肉瘤相关转录物2(EAT-2)或EAT-2相关转录物(ERT)等蛋白有极高亲和力,通过与这些蛋白结合传递活化信号,调节多种免疫反应,如NK细胞活化,NK-T细胞发育和抗体产生等。此外,一些SFR成员充当微生物传感器来调节巨噬细胞功能。越来越多的证据表明,SLAM家族受体成员是炎症和自身免疫性疾病的潜在靶标。
1.命名与结构
SFRs由九个不同的成员组成,SLAMF1(SLAM或CD150), SLAMF2(CD48),SLAMF3(Ly-9 或 CD229),SLAMF4(2B4 或 CD244),SLAMF5 (CD84),SLAMF6 (Ly108 (小鼠),NTB-A(人) 或 SF2000 (人)),SLAMF7 (CRACC,CD319或CS1),SLAMF8(CD353 或 BLAME),SLAMF9 (SF2001或CD84H)。在分类方面,SLAMF2、SLAMF8和SLAMF9不被视为SLAM系列的正式成员,被当做非典型SFR成员。这是因为与典型SFR成员相比,SLAMF2、SLAMF8和SLAMF9在其细胞质域中不具有同源性。
SFRs是I型糖蛋白,胞外由缺乏典型二硫键的N端Ig可变区(V 区)和以保守半胱氨酸为特征的C端Ig恒定2-SET区(C区)组成。其中,SLAMF3具有重复的IgV区和C2区。典型SFR成员的细胞质尾部包含多个基于免疫受体酪氨酸的开关基序(ITSM),而SLAMF2、SLAMF8和SLAMF9则不含ITSM。这些ITSM可偶联SAP、EAT-2和ERT来发挥作用。每个典型SFR成员至少包含一个ITSM,并且细胞质结构域中ITSMs的同源性是TxYxxV / I / L /(其中x是任何氨基酸)。
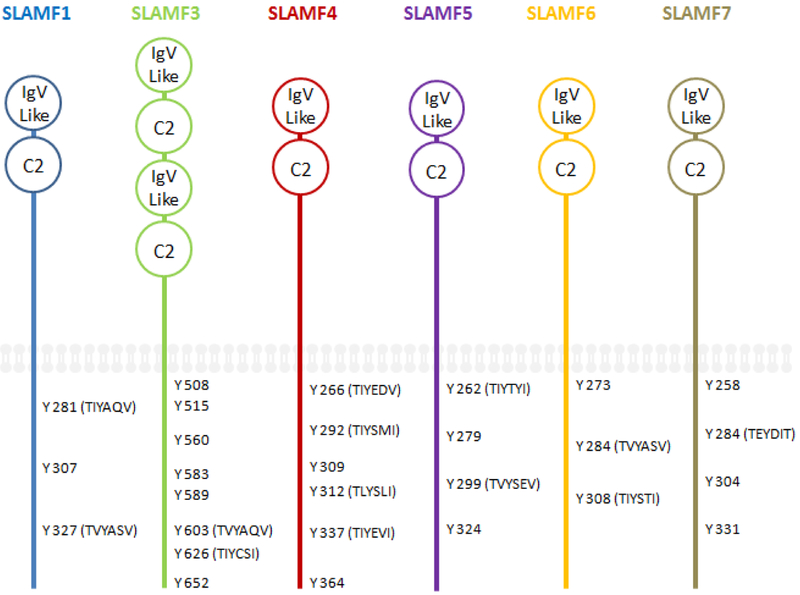
图1 典型SLAM家族受体的结构(图片来自于《Autoimmunity Reviews》)
2.作用机制
SFRs可以作为抑制受体或激活受体,其与SAP的双重作用机制控制NK细胞和CD8+T细胞活化的能力。SAP家族通过其SH2结构域与SFRs的ITSM的磷酸化酪氨酸(pY) 结合。这种相互作用阻止了SFRs与含有SH2结构域的抑制性磷酸酶如SHP-1、SHP-2和SHIP-1的偶联,从而阻止了SFRs的抑制功能。此外,SAP可以转换激活信号。SAP通过SAP的含精氨酸78 (R78)基序和Fyn的SH3结构域的相互作用募集Src家族酪氨酸激酶Fyn。Fyn磷酸化SFRs细胞质结构域中的其他基于酪氨酸的基序,也磷酸化Vav-1以转导下游激活信号。与SAP不同,EAT-2通过其位于羧基末端的酪氨酸和PLC-γ的SH2结构域结合激活PLC-γ,从而促进细胞活化的钙通量。
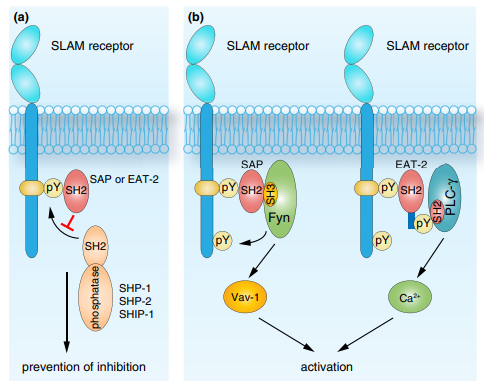
图2 SAP的双重作用机制(图片来自于《Current Opinion in Immunology》)
3. 疾病中的作用
SFRs与人类疾病发病机制的关联性表现在SAP编码基因在X-连锁淋巴组织增生性疾病(XLP)中发生突变,这是一种原发性人类免疫缺陷疾病。在XLP疾病中,SAP的缺失增加了SFRs的抑制潜力,从而抑制了NK细胞和CD8+T细胞对造血靶细胞的反应。SFRs参与的另一种自身免疫性疾病是系统性红斑狼疮(SLE)。已有研究确定Sle1b,一个与小鼠SLE易感性增加相关的基因座,实际上是Slam基因座。Slam基因座包含小鼠和人类的6个典型SLAM家族受体编码基因。Slamf6中的多态性导致SLAMF6受体信号增强,被证明对Sle1b增强SLE易感性的能力很重要。此外SFRs还可以充当病原体进入细胞的受体。并且,SLAMF1还是人类麻疹病毒以及其他物种的其他麻疹病毒的淋巴细胞特异性受体。
SFRs在抑制巨噬细胞吞噬功能中具有重要作用。SFRs广泛表达于造血细胞,并形成同型相互作用。最近的研究表明,特定的SFR成员,主要是SLAMF3和SLAMF4,被鉴定为巨噬细胞上的“don’t eat me”受体。这些受体通过含有SH2结构域的磷酸酶抑制“eat me”信号,如LRP1介导的mTOR和Syk的激活。SFRs与CD47共同抑制巨噬细胞的吞噬作用,但缺失CD47并不会阻断这种抑制作用。SFRs和CD47的联合缺失会导致造血细胞减少。这种SFRs介导的耐受性在噬血细胞性淋巴组织细胞增多症(一种以不适当的吞噬造血细胞为特征的综合征)患者中被削弱。SFRs的丢失可能引起造血肿瘤的巨噬细胞排斥反应,并且显著增强了表达嵌合CD19抗原受体的巨噬细胞对CD19阳性造血靶点的吞噬作用。因此,SFRs介导的巨噬细胞吞噬功能的抑制对造血稳态至关重要,可能是肿瘤免疫治疗的未知靶点。
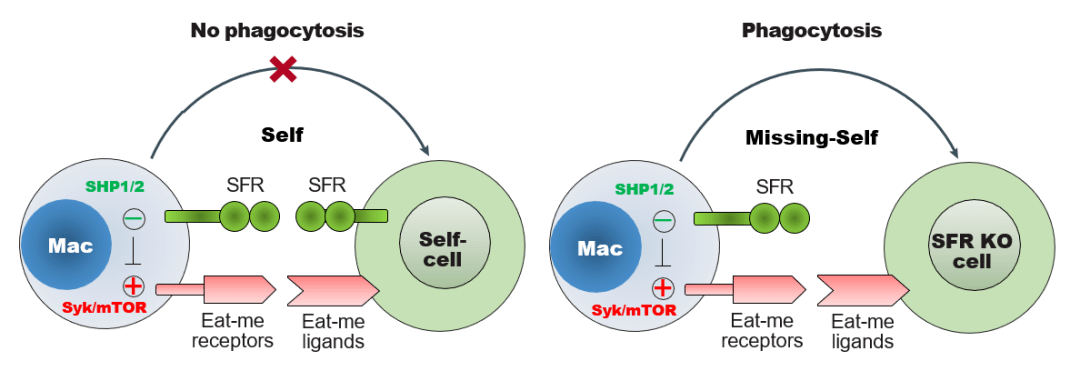
图3 SLAM家族受体抑制巨噬细胞吞噬的新机制(图片来自于《Science Immunology》)
SFRs是可以介导免疫细胞中相反功能的关键调节因子,其在自身免疫性疾病的发病机制中起着不可或缺的作用。全面了解这些蛋白质在健康和疾病中发挥作用的机制可能对炎症和靶向肿瘤的治疗提供新的方法。
云克隆相关产品:
靶标 | 靶标号 | 靶标 | 靶标号 |
SLAMF1 | B546 | PLCγ1 | A269 |
SLAMF2 | B843 | LRP1 | B010 |
SLAMF5 | B155 | mTOR | B806 |
SLAMF7 | K384 | SYK | E275 |
FYN | K247 | CD19 | B873 |