利用合成的IL-9受体增强过继细胞疗法在实体瘤治疗中的疗效
过继性免疫细胞疗法(Adoptive Cell Transfer Therapy,ACT)是指将收集的患者自身的免疫细胞(杀伤性T细胞),在体外培养改造后,增强其靶向杀伤功能,再回输到患者体内,达到消灭肿瘤细胞的目的。采用这种方法合成的免疫细胞能够以强大和精准的方式识别和消除癌症。过继性免疫细胞疗法可分为工程T细胞受体(TCR)治疗、嵌合抗原受体(CAR)T细胞治疗、自然杀伤细胞(NK)治疗和肿瘤浸润淋巴细胞 (TIL)治疗。目前ACT疗法的临床应用主要集中在白血病、淋巴瘤和多发性骨髓瘤等液体肿瘤。实体肿瘤由于表达的特异性抗原多,使用ACT疗法存在较大的局限性。2022年6月,加州大学洛杉矶分校的Anusha Kalbasi博士领导的研究团队与斯坦福大学及宾夕法尼亚大学的研究人员开展合作,在《Nature》上共同发表了名为“Potentiating adoptive cell therapy using synthetic IL-9 receptors”的文章。研究结果显示,人工合成的IL-9受体可以让ACT疗法在实体肿瘤小鼠模型中发挥强大的抗肿瘤能力。
众所周知,ACT疗法改造后的免疫细胞回输入体内后不久可能逐渐死亡,无法在体内有效增殖,使得治疗持续时间较短。因此,在接受过继性免疫细胞治疗之前要通过大剂量的化疗或放疗来清除体内免疫抑制细胞,以延长过继性免疫细胞在体内的生存时间。但大剂量化疗或放疗带来的副作用也非常明显。有研究人员提出可以尝试向患者体内输入共刺激因子IL-2,诱导T细胞成为广谱杀伤性细胞,来改善T细胞的存活、功能和抗肿瘤活性,作为一种辅助治疗手段。但是,IL-2的作用多效且复杂,IL-2R也不只存在于杀伤性T细胞,由于缺乏选择性,直接输入IL-2可能会导致其他非杀伤T细胞的激活,如IL-2还可激活Treg细胞从而抑制免疫作用。输入高剂量IL-2会造成严重的毒性,比如毛细血管渗漏综合征,这可能是由血管内皮细胞驱动的。正交细胞因子受体(Orthogonal receptor)是正常受体的一种突变形式,可选择性地结合突变的细胞因子,而不与正常的细胞因子结合, 可以保留功能的同时减少毒副作用。基于这个特性,研究人员使用昆虫表达系统设计了一个新的IL-2嵌合受体,它由正交IL-2的受体胞外结构域(ECD)和融合的受体胞内结构域(ICD)组成,并且和小鼠血清白蛋白(MSA)融合表达。接下来他们使正交IL-2细胞因子引发相应的γc细胞因子信号。γc细胞因子是一组哺乳动物细胞因子,主要由上皮、基质和免疫细胞产生,控制着不同系列的淋巴细胞的正常及病理性激活,主要包括IL-4、IL-7、IL-9和IL-21。进一步研究发现,用MSA-IL-2(mouse albumin-IL-2)以及MSA-oIL-2(mouse albumin-Orthogonal IL-2)刺激T细胞,MSA-oIL-2刺激o9R(Orthogonal IL-9 receptor)改造的T细胞引起了STAT1、STAT3和STAT5的明显磷酸化且o9R和o21R(Orthogonal IL-21 receptor)改造的T细胞高表达CD62L+、Fas(CD95)和Sca-1,出现与记忆干
细胞样T细胞(TSCM)相似的表型,具有良好的抗肿瘤活性。

图1 嵌合正交IL-2受体揭示IL-9R在T细胞中的信号传导特性
为了探究o9R信号在实体肿瘤中的作用,研究人员选择黑色素瘤模型小鼠作为研究对象,采用基因工程改造后使其得以表达对gp100具有特异性的T细胞受体(TCR)。这是一种在B16黑色素瘤中过度表达的黑色素细胞抗原。研究人员从小鼠脾脏中分离出Pmel-1T细胞,分别改造为o2R和o9R Pmel T细胞,然后过继转移至黑色素瘤荷瘤鼠体内。荷瘤鼠接受辐照,或MSA-IL-2和MSA-oIL-2治疗。7天后取小鼠外周血进行Pmel T细胞定量,结果显示,未经放化疗(未清除淋巴细胞)的情况下,o9R Pmel T细胞数量显著高于对照组,且MSA-oIL-2+o9R Pmel T细胞处理的小鼠瘤体增长更为缓慢,生存时间也存活率也显著增加。另外肿瘤浸润量化试验显示,与o2R Pmel T细胞相比,o9R Pmel T细胞浸润更大(图2)。以上数据表明,MSA-oIL-2处理的o9R Pmel T细胞在该模型中抗肿瘤效果更为显著。

图2 o9R信号促进Pmel T细胞的抗肿瘤疗效
接下来研究人员探索了 o9R信号在CAR-T疗法中的作用。他们选用具有免疫治疗抗性的胰腺癌模型作为研究对象。 采用具有IL受体模拟信号的CAR来转导小鼠原代T细胞,从而得到了CAR-o2R和CAR-o9R T细胞。体外细胞实验结果显示,CAR-o9R T细胞在体外对间皮素(MSLN)阳性的胰腺导管腺癌(PDA)细胞系(PDA7940b)显示了优越的抗肿瘤疗效。与前面的研究结果相似,CAR-o9R T细胞在接受MSA-oIL-2刺激后,也出现与TSCM相似的表型,IFNγ、TNF、IL-4、IL-9、IL-10、IL-18、IL-22和IL-23分泌水平较CAR-o9R细胞更高(图3)。
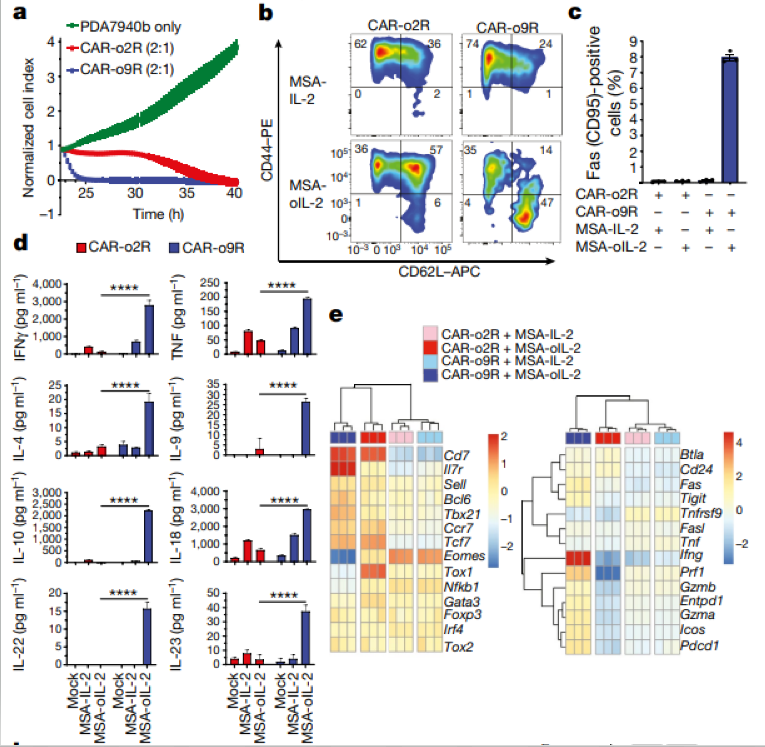
图3 o9R信号促进CAR-T细胞的抗肿瘤疗效
综上所述,研究人员通过靶向天然的T细胞受体或嵌合抗原受体的T细胞来攻击小鼠癌细胞,并利用合成的细胞因子信号来强化T细胞的肿瘤杀伤功能,在两种难治的癌症模型(胰腺癌和黑色素瘤)上均取得良好的试验效果。
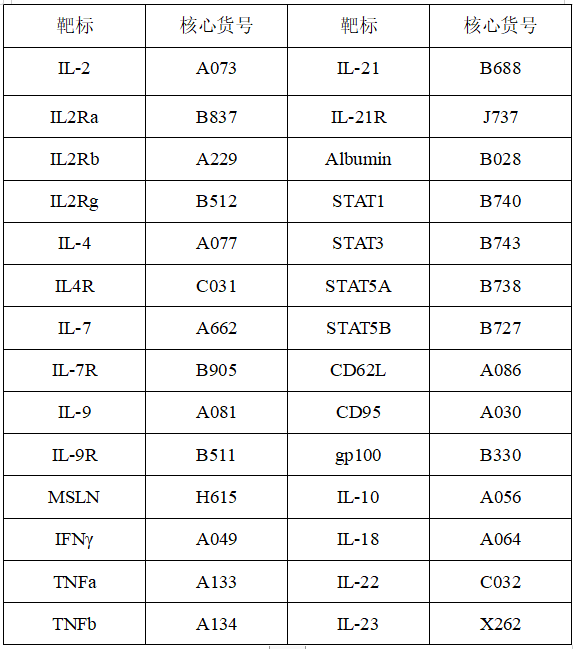
云克隆公司提供上述研究中涉及相关指标的蛋白、抗体、ELISA试剂盒等产品,助力相关研究: