IRAK-4:自身免疫疾病和肿瘤治疗的共同靶点
白介素-1受体相关激酶4(IRAK-4)是参与机体先天性免疫反应过程中的关键分子。它与另外3个成员IRAK-1、IRAK-2、IRAK-3(IRAK-M)同属于细胞内丝氨酸-苏氨酸激酶IRAK家族。IRAK家族成员都有一个含丝氨酸和苏氨酸的激酶结构域和保守的死亡结构域,除IRAK-4之外,其他三个IRAKs都有一个长的C末端结构。IRAK-4是固有免疫系统上IL-1家族和TLR(Toll样受体)家族这两大信号通路交汇的最重要的节点,在全身炎症反应中起非常重要的作用。相关研究发现,许多自身免疫疾病和肿瘤也与介导炎症的信号有关,因此IRAK-4可以作为一个有效的治疗靶点。
一、IRAK-4参与TLRs/IL-1R信号通路
TLRs/IL-1R与配体结合以后,募集MyD88分子,MyD88通过其N末端的死亡结构域进一步募集IRAK-4。IRAK-4通过自身磷酸化反应,发挥激酶活性,激活其底物IRAK-1,使其磷酸化。磷酸化的IRAK-1构型发生改变,导致其与受体复合物的亲和力下降而分离,并与TNF受体相关因子6(TRAF-6 ) 形成复合物,使TRAF-6发生低聚作用,进一步通过转接蛋白TAB激活转化生长因子β活化激酶和NF-κB诱导激酶(NIK)。NIK激活IκB激酶(IKK)复合物,IKK复合物进而磷酸化IκB。磷酸化的IκB随后被降解,从而解除了对NF-κB 的抑制作用,导致NF-κB 活化。活化的NF-κB进入细胞核,引起促炎细胞因子基因的转录和表达。TRAF-6还可通过另外一条途径激活丝裂原活化蛋白激酶(MAPK)引起转录因子c-Jun氨基末端激酶(JNK)的活化。IRAK-4在整个信号通路起到承上启下的作用,通过激活下游信号通路,产生促炎症因子。
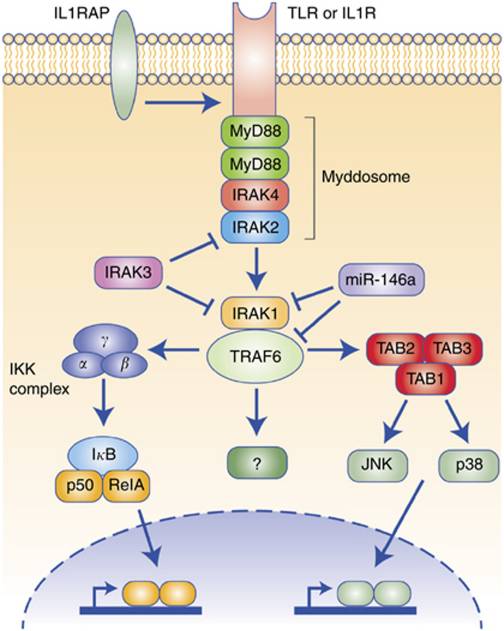
图1 TLR/IL-1R信号通路
(图片源自《British Journal of Cancer》)
二、IRAK-4与自身免疫疾病
IRAK-4的作用,特别是其在先天免疫以及自身免疫和炎性疾病患者的发病机理中的作用被逐渐认识。irak4不稳定或无效突变的患者表现出toll样受体信号传导和促炎性细胞因子(如IL-1和TNFα)以及抗病毒细胞因子(如IFNα和IFNβ)产生的缺陷。这些患者的细胞也对通过MyD88发出信号的TLR或IL-1R家族配体没有反应。并且在小鼠中,IRAK-4的缺失或失活可防止多种炎症性疾病模型的炎症发展,包括:脓毒症休克、系统性红斑狼疮、急性肝损伤、心血管疾病和阿尔茨海默病等。有研究表明,理论上通过口服用药靶向IRAK-4可以同时阻断 TLRs、IL-1α、IL-1β、IL-18、IL-33、和IL-36 等上游信号。能够直接从一开始就抑制住后面的关键免疫反应信号 TNFα和 IL-6(启动Th17的核心信号)的表达。另外,由于NF-κB被激活后还会进一步增加IL-1的表达,抑制IRAK-4可以阻止IL-1信号正反馈的形成和作用。
比利时Galapagos NV的Reginald Brys和法国Galapagos SASU的Stéphanie Lavazais研究团队证实抑制IRAK-4可以作为人类皮肤疾病的潜在临床靶点。该团队选用IRAK-4抑制剂GLPG2534,并开发出一套翻译验证策略(translational validation strategy),在动物模型以及牛皮癣和过敏性皮肤炎病人来源的细胞中,绘制了IRAK-4抑制的响应图谱。在体外,抑制IRAK-4可以抑制多种细胞,包括:树突状细胞、角质形成细胞、巨噬细胞,并且巨噬细胞中的TLRs和IL-1R信号通路得到显著抑制。另外,抑制小鼠IRAK-4,可以明显缓解IL-23、IL-33、咪喹莫特(imiquimod)和MC903诱导的皮肤炎症。最后,团队还发现,在人类牛皮癣和过敏性皮炎样本中,抑制IRAK-4可以明显逆转这些样本的病理性分子特征。
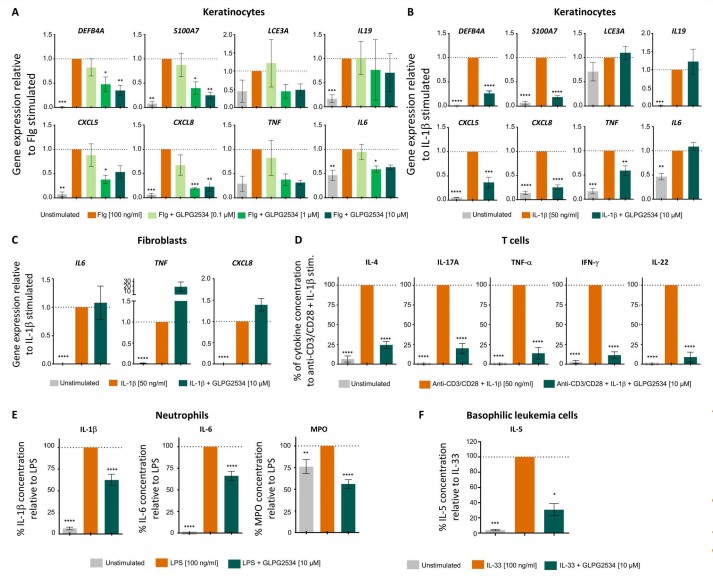
图2 GLPG2534在与皮肤炎症疾病相关的测定中表现出活性
(图片源自《Science Translational Medicine》)
风湿关节炎(RA)是目前最常见的自身免疫系统疾病之一。 RA的滑膜炎症特征受Th1和Th17免疫反应驱动,并产生TNFα和IL-1的家族细胞因子,包括IL-1、IL-18、IL-33、IL-6和IL-17。目前已有针对这些细胞因子的多种疗法用于治疗RA。抑制或者降解IRAK-4也是一种有效地治疗方法。IRAK-4不止位于TNFα、IL-6上游,也在IL-17、JAK-1(酪氨酸激酶1)、JAK-3(酪氨酸激酶3)等其它重要节点的上游,可以从源头上就抑制IRAK-4或者和这些下游的靶点一起联合用药来提高疗效。
近几年,多家药企也致力于利用靶向IRAK-4来治疗自身免疫和炎性疾病。以辉瑞的PF-06550833为代表的多款IRAK-4小分子激酶抑制剂已进入临床阶段。进展较快的是Kymera Therapeutics(Kymera)旗下的KT-474,其在1期临床试验患者队列的临床治疗结果显示,在化脓性汗腺炎(HS)和特应性皮炎(AD)患者中,血液和活动性皮肤病变中的IRAK-4被抑制,全身促炎细胞因子和趋化因子也被抑制,药物具有良好的安全性。此外,大多数HS和AD患者疾病负担和症状的临床终点,在给药四周后均有显著缓解。
二、IRAK-4与肿瘤
先天免疫信号传导成分的失调越来越被认为是癌症发生和发展的重要介质。在一些恶性肿瘤中,TLRs和IL1R信号传导失调的典型表现为NF-κB活性的增加。而体细胞突变、染色体缺失和/或转录失调是导致信号传导失调的原因。IRAK家族成员是TLRs/IL1R超家族信号传导的介质,越来越多的证据表明这些激酶是可行的癌症靶标。
检查点免疫疗法对一些顽固性肿瘤(如转移性黑色素瘤和非小细胞肺癌)的癌症具有良好的效果,但是对胰腺导管腺癌(PDACs)几乎没有作用。在一项针对小鼠的新研究中,华盛顿大学医学院的研究者们发现IRAK-4在胰腺肿瘤中引发炎症,并导致一种称为“T细胞衰竭”的现象,即在慢性感染和癌症中,T细胞长时间暴露于抗原和/或炎症信号的刺激,会失去强大的效应功能,导致细胞因子产生减少,存活率降低,并且表达多种抑制受体。该团队使用一种名为CA-4948的IRAK-4抑制剂治疗KPC小鼠(与临床相关的PDAC小鼠模型),这种治疗降低了肿瘤中的炎症信号,增加了免疫T细胞浸润到肿瘤中的能力,并使肿瘤对增强T细胞活性的检查点免疫疗法敏感。CA-4948阻断驱动癌症的NF-κB信号通路的激活。与化疗或安慰剂对照组相比,使用CA-4948或选择性删除IRAK-4治疗可提高KPC小鼠的存活率。当IRAK-4抑制剂与化疗或检查点免疫疗法结合使用时,可进一步提高生存率。
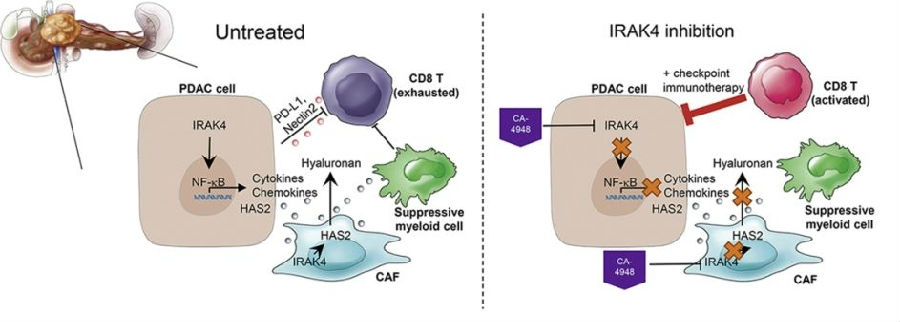
图3 IRAK-4抑制剂作用通路模型
(图片源自《Gastroenterology》)
在淋巴恶性肿瘤中,靶向IRAK-4也可以作为一个治疗方向。在弥漫性大B细胞淋巴瘤中发现致癌活性MyD88突变后,癌症对IRAK信号传导的特异性依赖变得明显。在大量肿瘤活检中发现,29%的淋巴恶性肿瘤含有L265P MyD88突变体。L265P MyD88突变体通过自发组装含有IRAK-1和IRAK-4的蛋白质信号复合物促进细胞存活,导致IRAK-4激酶活化、IRAK-1磷酸化以及活化JAK-STAT和NF-κB信号。而IRAK-4或IRAK-1的敲低消除了NF-κB活化并诱导快速细胞凋亡。持续的MyD88-IRAK信号传导对于这种淋巴恶性肿瘤发病机制和肿瘤细胞存活是必要的。因此,开发IRAK-4选择性激酶抑制剂,可用于治疗含有致癌MyD88突变的肿瘤。也有相关研究表明IRAK信号传导与血液系统恶性肿瘤有关,许多与白血病相关的遗传病变会诱导细胞内IRAK信号传导中心的改变。
IRAK-4在TLRs/IL-1R信号通路中的关键位置使其在多种疾病中都有关键作用。以IRAK-4为靶点的特异性药物,或者通过基因治疗手段干预IRAK-4表达,为部分疾病的控制和治疗提供了新的方向。
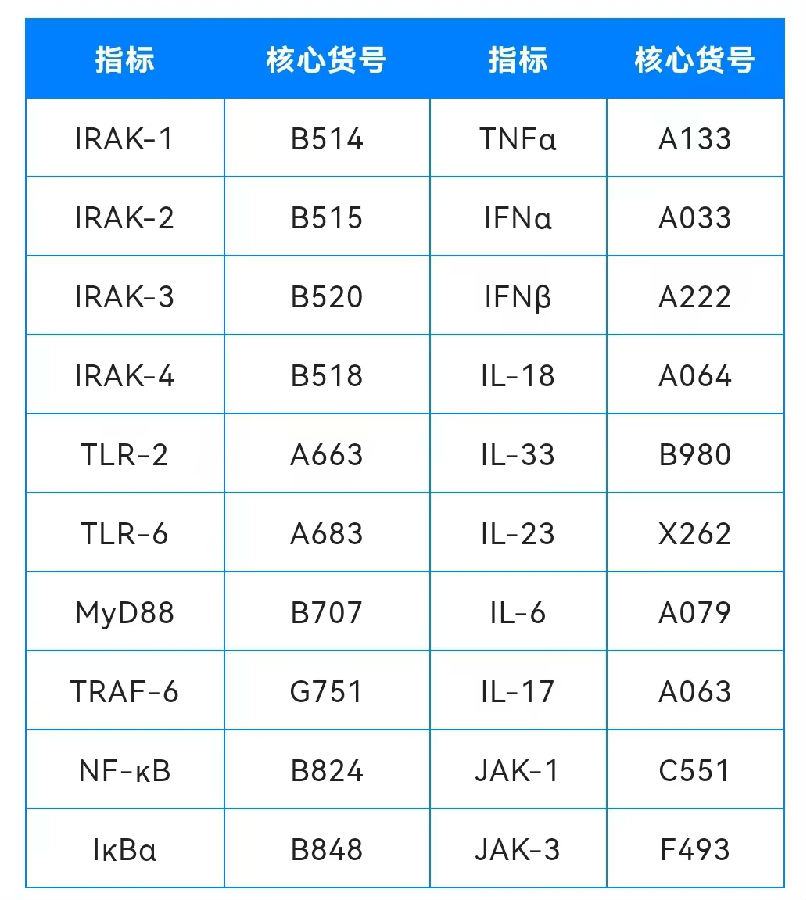
云克隆期望能为广大研究者在疾病治疗以及药物研发方面提供帮助,相关指标如下: