USP11或可揭秘为何女性更易患阿尔茨海默病
女性患阿尔茨海默病(Alzheimer's Disease, AD)的概率约是男性的1.7倍,tau聚集也明显高于男性。已有大量研究表明tau蛋白在神经细胞中异常聚集是造成AD的重要原因,但女性易患AD的机制还尚未可知。近期,美国凯斯西储大学医学院研究团队在《Cell》杂志上发表的题为“X-linked Ubiquitin-Specific Peptidase 11 Increases Tauopathy Vulnerability in Women”的文章揭示了女性更易患AD的可能分子机制。
该文章显示:x-连锁的泛素特异性肽酶11(USP11)在女性大脑中表达水平更高,研究者通过体外、体内模型以及人AD脑组织证明USP11通过赖氨酸-281(K281)启动的tau去泛素化增强病理性tau聚集,去泛素后tau蛋白在赖氨酸281和274处发生乙酰化。在tau蛋白病小鼠模型中,敲除usp11优先保护雌鼠免受乙酰化的tau积累和认知障碍的影响。因此,女性脑中USP11的高表达或许导致了tau蛋白在女性大脑中的积累水平更高,使女性对tau蛋白病的易感性增加。(见图1)
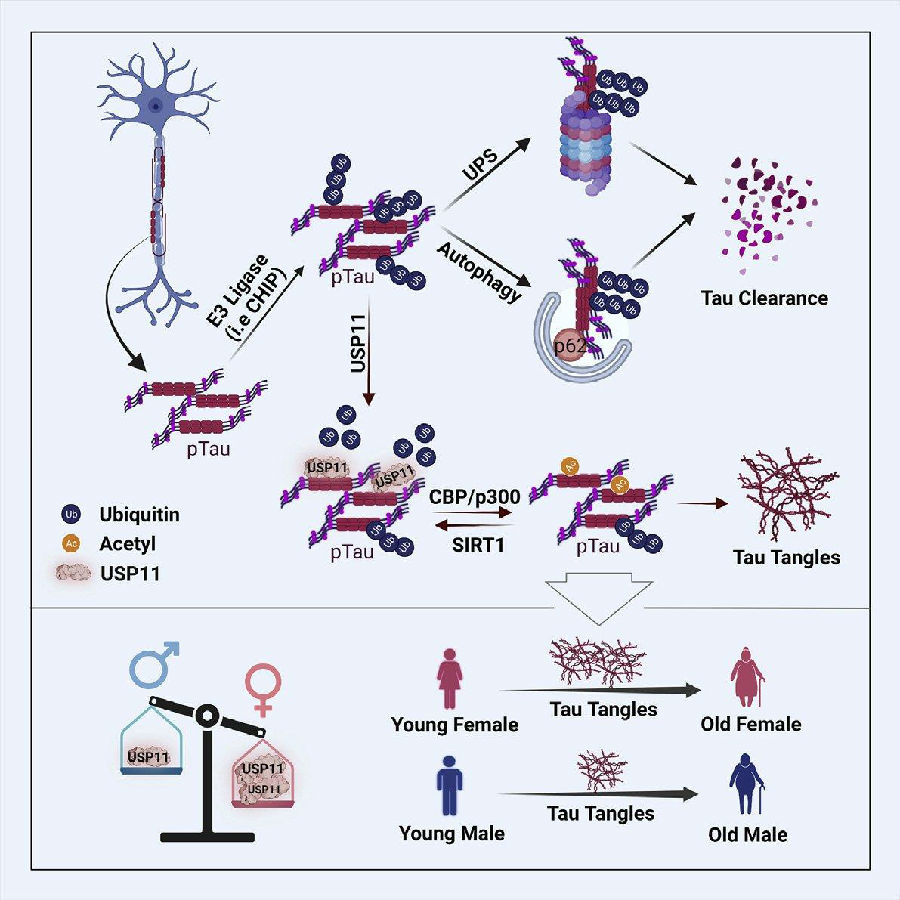
图1. 女性更易患AD的分子机制(图片来源于《Cell》杂志)
Tau是一种微管相关蛋白,其聚集和清除受多种翻译后修饰控制,包括磷酸化、甲基化、乙酰化和泛素化。泛素化是通过泛素-蛋白酶体系和自噬-溶酶体途径控制tau清除的最终修饰,即多余的tau蛋白在被清除前,需要先泛素化。而tau蛋白乙酰化是AD的病理学标志之一,tau蛋白的乙酰化会促进tau的累积和毒性。在患有AD和相关tau蛋白病患者的大脑中,tau蛋白无法正常清除并异常聚集和积累,从而导致神经细胞丧失功能。
该研究首先在稳定表达野生型tau的Hela细胞(HeLa-V5-tau, 0N4R)中对22个中枢神经系统去泛素化酶(DUBs)进行功能性小干扰RNA(siRNA)筛选,发现敲低usp11或usp13均显著降低tau蛋白水平,确定了USP13和USP11为tau的两个正调节因子。由于USP11位于X染色体上,故研究者着力研究USP11。
进一步的细胞实验发现usp11敲低(USP11 siRNA)使HeLa细胞及iHEK-tauP301L细胞中tau减少45%(iHEK-tauP301L细胞是表达FTDP-17 MAPT基因突变tauP301L 的iHEK细胞。FTDP-17指额颞叶痴呆(FTD),为继阿尔茨海默病之后第二常见痴呆症。部分FTD具有与17号染色体连锁关系,故命名为FTDP-17。FTDP-17是位于17号染色体上的MAPT基因突变所致。在家族性额颞叶痴呆病例中,已陆续发现MAPT基因中大约有80个致病性错义突变,大多落在Tau蛋白结合微管的编码区,其中P301S和P301L分别是指Tau蛋白氨基酸残基301的脯氨酸突变为丝氨酸或亮氨酸)。在iHEK-tauP301L细胞和Hela-V5-tau细胞中过表达USP11显著增加了不溶性tau量,而不改变可溶性tau量。此外,提高USP11表达水平后,USP11会通过其DUB催化活性促进tau不溶性和病理性聚集。在转染USP11的iHEK-tauP301L细胞中发现tau免疫复合物中的多泛素结合tau显著降低,表明tau通过USP11去泛素化。且研究者外源添加重组USP11后(24小时),发现除K254外,tau上几乎所有的泛素结合物都被移除了。(见图2)
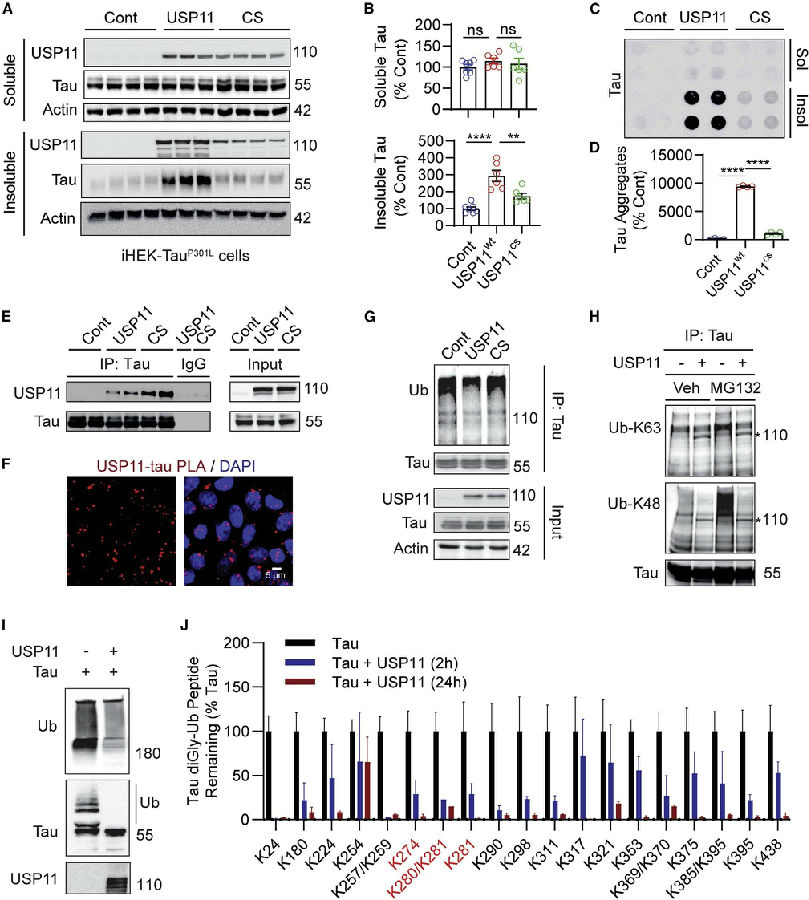
图2. USP11催化活性介导tau聚集和去泛素化(图片来源于《Cell》杂志)
大多数可以泛素化的tau赖氨酸也会发生乙酰化,但是同一个赖氨酸很难同时既泛素化又乙酰化,所以研究人员利用tau乙酰化模拟物(K274Q、K280Q和K281Q)来研究tau的溶解度,已有文献报道这3种tau乙酰化模拟物能促进tau聚集和/或诱导tau病理转化。结果表明在tau免疫复合物中,tau-K281Q突变体表现出多泛素化显著降低,但K280Q突变体没有显示显著性的泛素化降低,K274Q突变体没有变化,表明K281处的tau去泛素是USP11驱动tau蛋白病的关键。
进一步研究发现,过量的USP11与病理性tau聚集相关。相对非痴呆对照组,人类tau蛋白病中的USP11的表达水平更高。且通过定量细胞质/细胞核USP11比值发现USP11的细胞质/细胞核比例也显著增加,而在非痴呆对照组中,USP11主要在核表达。此外,与男性AD大脑相比,USP11强度与女性AD大脑中的tau病理学呈高度显著正相关。说明USP11积累是女性tau病理的更重要驱动因素。由于usp11同样位于啮齿动物的X染色体上,研究者做了小鼠额皮质染色,发现7个月大的WT雌性小鼠(usp11 + / +)的USP11含量比WT雄性小鼠(usp11 +)高很多,而雌性和雄性usp11敲除小鼠均未检测到USP11。这表明USP11在女性tau蛋白病理中起着重要作用。 (见图3)
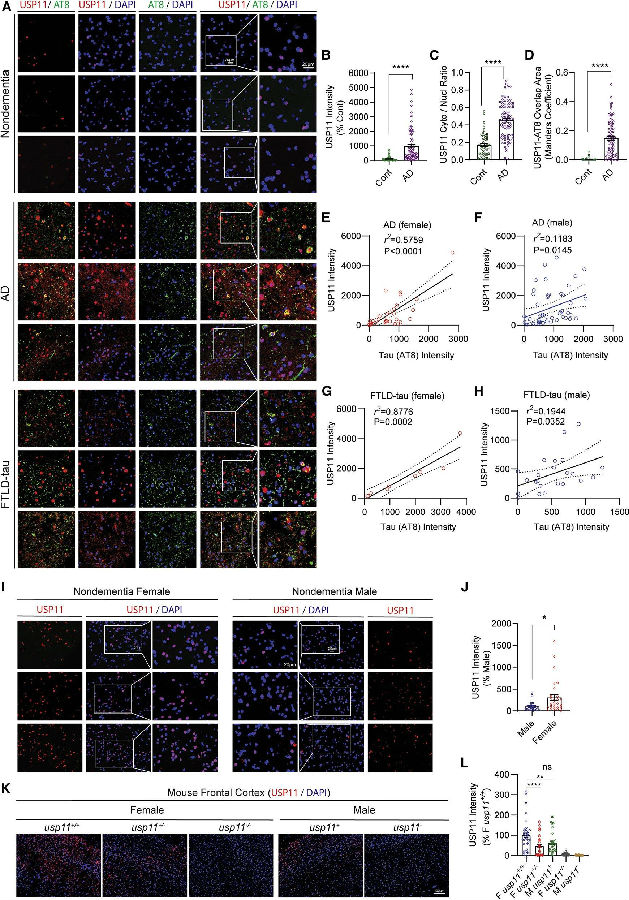
图3. USP11与女性tau蛋白病有很高的相关性(图片来源于《Cell》杂志)
进一步通过usp11-/-基因敲除鼠发现,与tauP301S雌鼠相比,tauP301S; usp11 -/-雌鼠中,不溶性 Ac274-tau和Ac281-tau显著降低。通过电生理评估USP11对短期和长期突触可塑性的影响,发现usp11减少或丢失可恢复tauP301S小鼠的长期突触可塑性(见图4)。最后,从行为学上发现usp11的缺失逆转了tauP301S诱导的雌性小鼠空间记忆障碍。
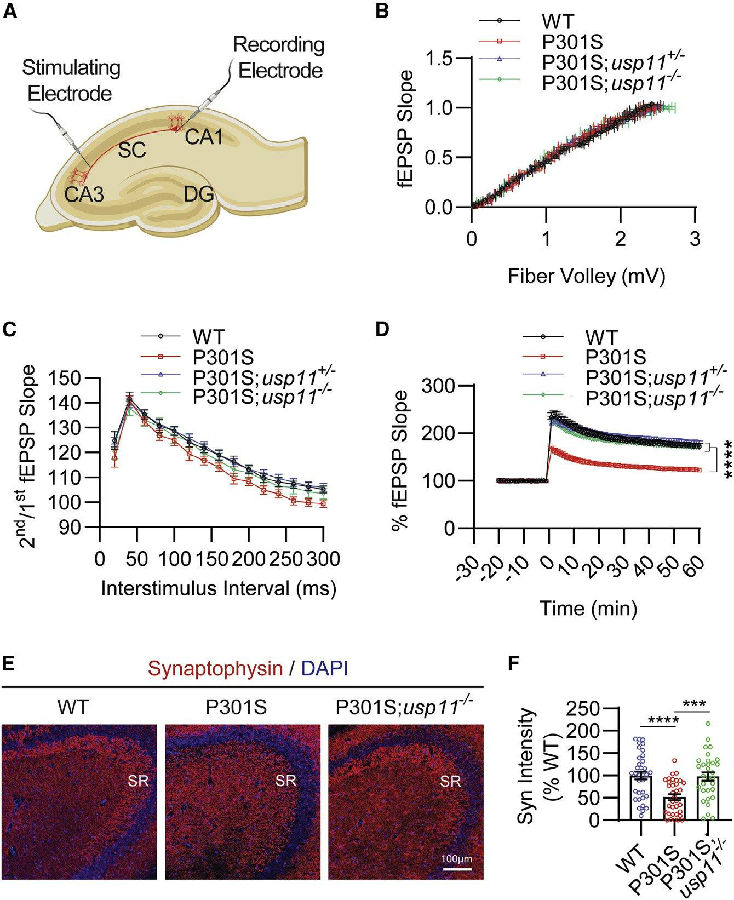
图4. usp11的缺失挽救了雌性tauP301S小鼠的突触可塑性缺陷 (图片来源于《Cell》杂志)
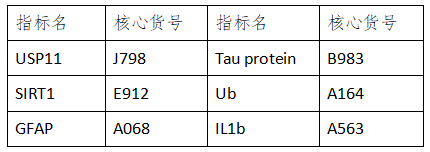
根据此文章可知,USP11 的蛋白表达量在女性大脑中高于男性,女性大脑中过量的USP11水平会导致tau过度去泛素化,导致女性较男性有更多的异常tau蛋白沉积,从而增大了女性患AD的风险。USP11是一种酶,而酶传统上可以通过药理来抑制,因此,抑制USP11介导的tau去泛素化可能可以为患者提供有效的治疗机会,以保护女性免受AD和其他tau蛋白病的影响。该研究为AD的临床早筛提供了方向,为人类攻克AD提供了理论基础。但这不代表 USP11 是唯一的AD病理机制,未来还需要更多更深入的研究去助力AD的治疗。云克隆开发了与该研究相关的靶标产品,部分指标节选如下:
更多信息,欢迎访问:http://www.cloud-clone.cn/