文献解读 | M2巨噬细胞衍生的sEV调节促炎CCR2+巨噬细胞亚群有利于AMI后心脏修复

2023年3月22日,天津中医药大学现代中医药国家重点实验室Guanwei Fan团队在《Advanced Science》上发表题为“M2 Macrophage-Derived sEV Regulate Pro-Inflammatory CCR2+ Macrophage Subpopulations to Favor Post-AMI Cardiac Repair”的文章,他们表明M2巨噬细胞来源的细胞外囊泡(sEV)通过mir -181b-5p依赖机制调节CCR2+巨噬细胞,挽救心肌功能,改善心肌修复。

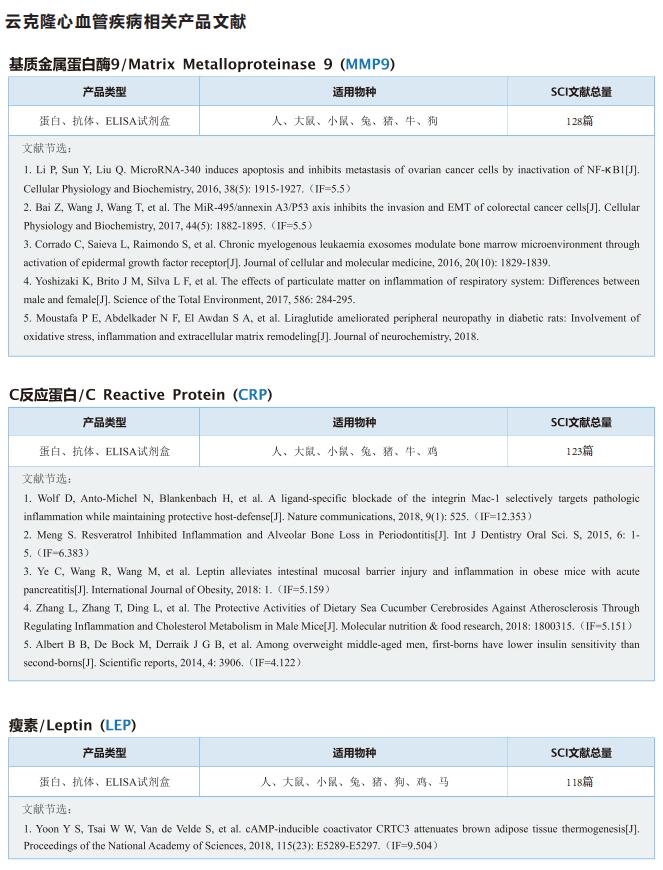
在这篇文章中,云克隆蛋白【干扰素γ(IFNg)重组蛋白,RPA049Ra01;白介素4(IL4)重组蛋白,RPA077Ra01;白介素13(IL13)重组蛋白,RPA060Ra01】受到科研工作者的认可,荣登优秀国际期刊。


急性心肌梗死(AMI)是世界范围内死亡的主要原因。不完全再灌注和大面积或多个部位梗死会导致缺血再灌注(I/R)损伤,从而促进左心室重构和进行性心力衰竭。组织驻留的心脏巨噬细胞亚群介导AMI后的心脏组织炎症和修复。表达CC趋化因子受体2(CCR2)的巨噬细胞与M1极化巨噬细胞具有表型相似性,具有促炎作用,将CCR2+循环单核细胞募集到梗死心肌,并与促进致病性不良心脏重构有关。然而,循环源性巨噬细胞和常驻巨噬细胞不同亚群之间的调节机制和相互作用仍不清楚。
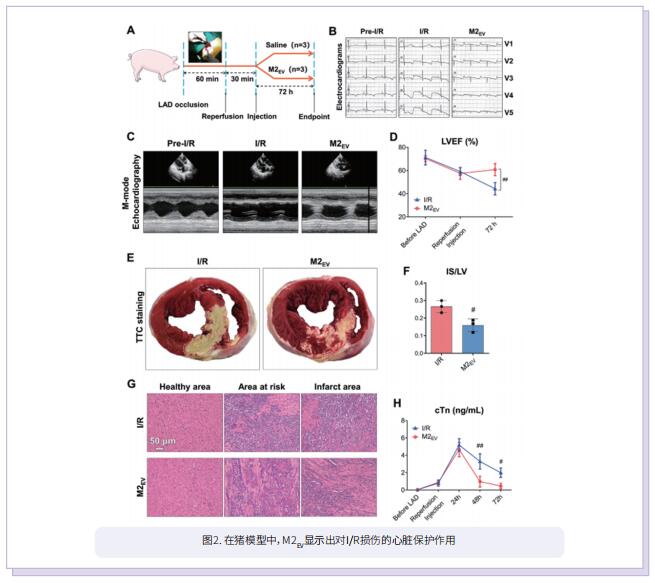
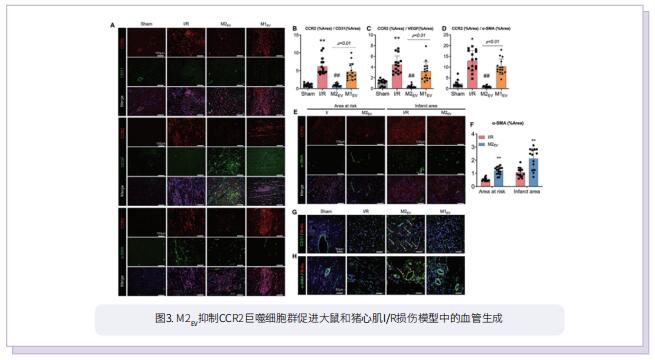
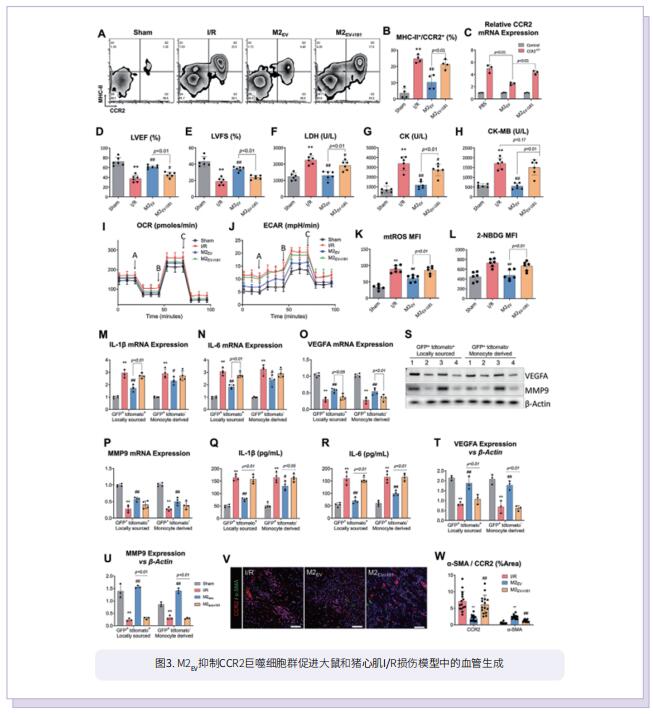
小的细胞外囊泡(sEV)是一类细胞衍生的囊泡,能传递细胞间通信并促进细胞物质和信息的交换。在这项研究中,作者评估了M2巨噬细胞衍生的sEV(M2EV)在大鼠和猪心肌I/R损伤模型中的可塑性和修复作用。将实验大鼠和猪分别进行假手术、未经治疗I/R、自体M2EV治疗I/R处理。M2EV挽救了心功能,减弱了损伤标志物、梗死面积和疤痕面积。M2EV抑制CCR2+巨噬细胞数量,减少单核细胞来源的CCR2+巨噬细胞向梗死部位募集,诱导M1-M2巨噬细胞转换,促进新生血管形成。M2EV microRNA含量分析显示,miR-181b-5p含量丰富,其调节巨噬细胞葡萄糖摄取、糖酵解,并减轻线粒体活性氧的产生。miR-181b-5p的功能阻断不利于有益的M2EV作用,导致无法抑制CCR2+巨噬细胞数量和梗死面积。
综上所述,这项研究表明M2EV通过miR-181b-5p依赖机制挽救心肌功能,改善心肌修复,调节CCR2+巨噬细胞,可能是无细胞治疗AMI的一种选择。