肠易激综合征研究新进展
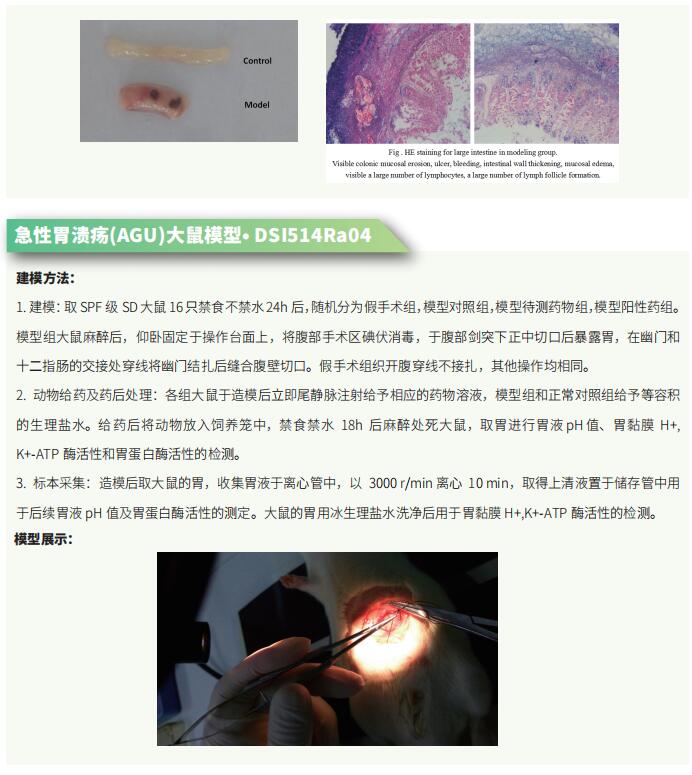
肠易激综合征(IBS)是一种常见的疾病,其特征是在没有其他器质性胃肠道疾病的情况下发生的慢性、复发性腹痛和腹部不适,以及排便习惯的改变。IBS可造成严重的医疗负担,并严重损害患者生活质量。IBS病因尚不清楚,涉及多种因素。胃肠动力改变、内脏超敏反应、感染后反应性、脑肠相互作用、粪便微生物群改变、细菌过度生长、食物敏感性、碳水化合物吸收不良和肠道炎症等都与IBS的发病机制有关。进一步了解IBS的发病机制有助于开发新的治疗方法以改善患者生活质量。
1. 结肠TRPV1谱系神经元表达的Piezo2通道介导内脏机械超敏反应
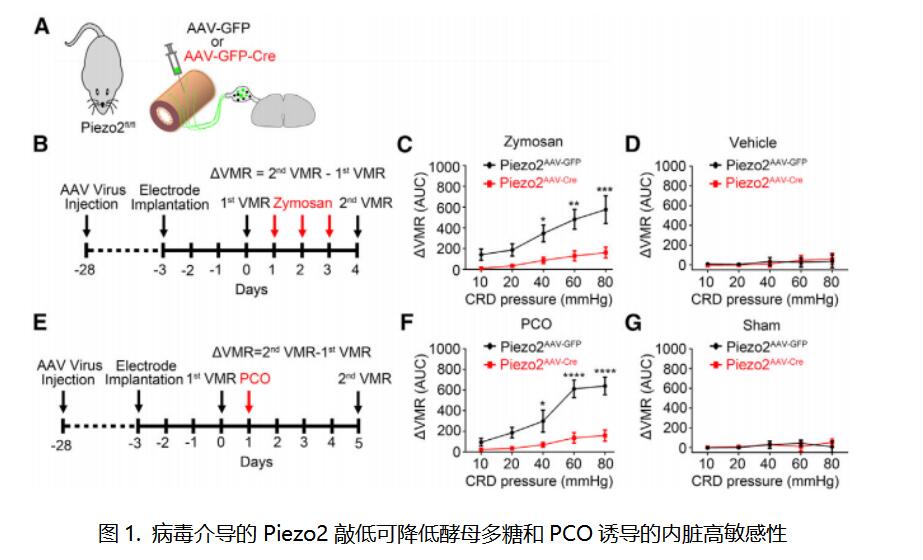
炎症性和功能性胃肠道疾病,如IBS和梗阻性肠病(PCO),是引起内脏疼痛的原因之一。尽管内脏疼痛通常可以由机械扩张/拉伸引起,但结肠支配内脏传入神经的内脏机械敏感性的机制仍然难以捉摸。华盛顿大学医学院Hongzhen Hu团队发现TRPV1谱系神经元表达的机械敏感的Piezo2通道,参与内脏机械伤害性感受和机械超敏反应的产生[1]。在生理条件下,以及酵母多糖诱导的IBS和部分PCO小鼠模型中,选择性消融TRPV1谱系神经元激活的Piezo2通道可显著减少机械诱发的内脏传入动作电位放电和结肠扩张诱发的内脏运动反应(图1)。这些结果表明Piezo2通道是病理性内脏机械超敏的关键介质,从而确定Piezo2是治疗慢性内脏疼痛的潜在治疗靶点。
2. 瘤胃球菌通过增加血清素生物合成在腹泻型肠易激综合征中起致病作用
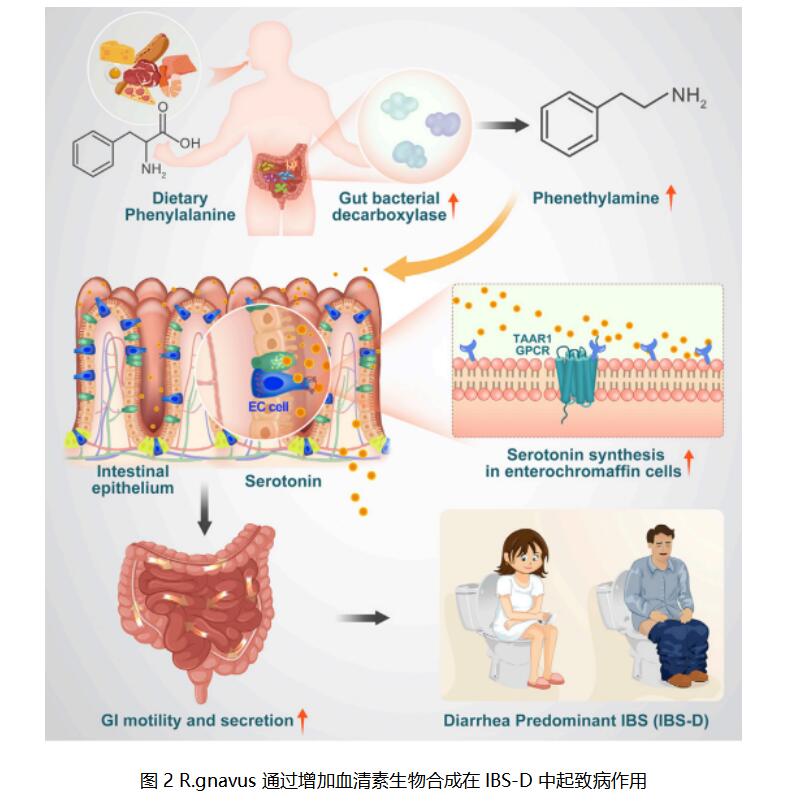
腹泻型肠易激综合征(IBS-D)是一种全球流行的功能性胃肠道疾病,与可增加肠道动力的血清素升高相关。香港浸会大学中药开发中心有限公司Zhao-xiang Bian团队确定Ruminococcus gnavus在IBS-D中起致病作用[2]。单定植R. gnavus的无菌小鼠可通过刺激外周血清素的产生,诱导IBS-D样症状,包括胃肠道传输和结肠分泌增加。R.gnavus介导的膳食苯丙氨酸和色氨酸的分解代谢产生了苯乙胺和色胺,通过激活微量胺相关受体1(TAAR1)的机制直接刺激肠嗜铬细胞中5-羟色胺的生物合成(图2)。临床前研究表明,TAAR1的药理学拮抗作用可缓解R.gnavus定植小鼠的IBS-D样症状,揭示了靶向苯乙胺和色胺-TAAR1信号轴治疗IBS-D的治疗潜力。
3. 肠道嗜铬细胞驱动内脏疼痛和焦虑
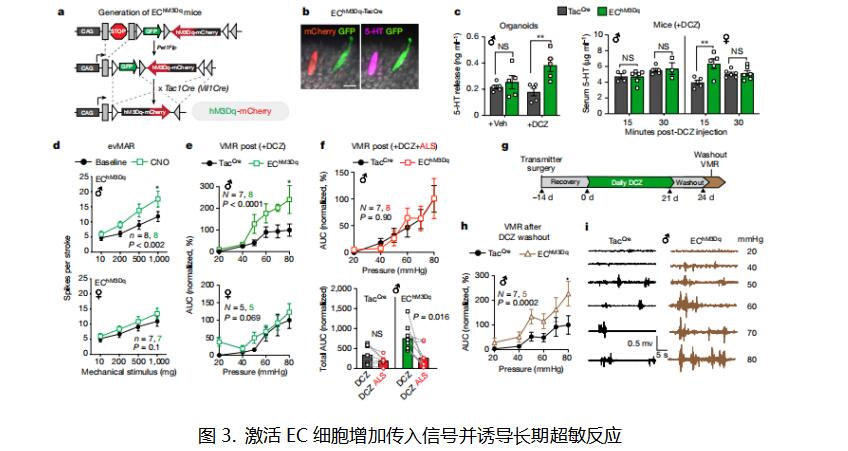
IBS患者的胃肠道超敏反应和疼痛在组织损伤解决后很长一段时间内仍会持续。美国加利福尼亚大学生理学系David Julius团队关注肠嗜铬(EC)细胞在内脏疼痛中的作用[3]。通过增强或抑制体内EC细胞功能,他们发现这些细胞足以引发对肠道扩张的超敏反应,并且是异戊酸(一种与胃肠道炎症相关的细菌短链脂肪酸)增敏作用所必需的。值得注意的是,即使在没有引发炎症的情况下,EC细胞的长期激活也会产生持续的内脏超敏反应(图3)。此外,干扰EC细胞活性促进了焦虑样行为,这种行为在阻断5-羟色胺能信号传导后正常化。这些研究结果证实了EC细胞-粘膜传入信号在急性和持续性胃肠道疼痛中的关键作用。
参考文献
[1]Xie Z, Feng J, Hibberd TJ, et al. Piezo2 channels expressed by colon-innervating TRPV1-lineage neurons mediate visceral mechanical hypersensitivity. Neuron. 2023;111(4):526-538.e4. (IF=18.688)
[2]Zhai L, Huang C, Ning Z, et al. Ruminococcus gnavus plays a pathogenic role in diarrhea-predominant irritable bowel syndrome by increasing serotonin biosynthesis. Cell Host Microbe. 2023;31(1):33-44.e5. (IF=31.316)
[3]Bayrer JR, Castro J, Venkataraman A, et al. Gut enterochromaffin cells drive visceral pain and anxiety. Nature. 2023;616(7955):137-142. (IF=69.504)
云克隆不仅可提供肠易激综合征、克罗恩病、溃疡性结肠炎、胃溃疡、胃炎、十二指肠溃疡等常见消化疾病动物模型,还具有各类肠胃疾病检测指标及上述TRPV1、TAAR、5-羟色胺等相关产品,可助力广大科研工作者进行消化道疾病相关研究。