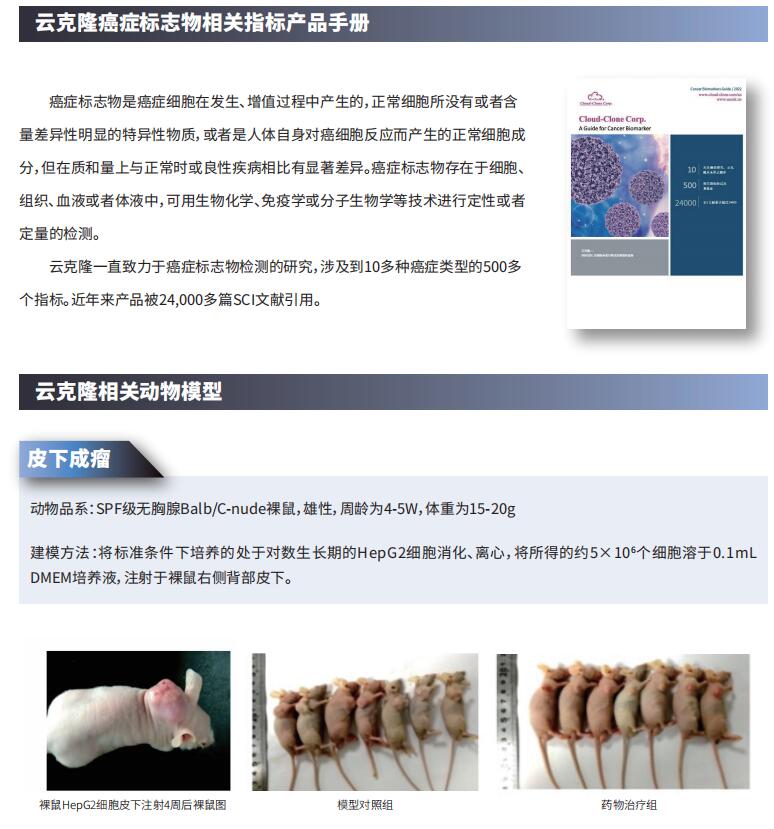
食管癌研究新进展
食管癌(EC)是全球第八大最常见的癌症,由于其侵袭性和低生存率,预后排名第六。世界范围内EC的发病率一直在增加,鳞状细胞癌和腺癌是两种主要的组织学亚型。食管鳞状细胞癌(ESCC)是更常见的EC类型,79%的ESCC病例发生在亚洲。然而,在西方工业化国家,食管腺癌(EAC)的发病率迅速上升。EAC的总体中位生存率通常高于ESCC,尤其是在早期疾病中。尽管在过去的三十年中,诊断和治疗技术有了无数的改进,EC的预后仍然很差。近期,多篇文献报道了EC相关研究,可能为EC的早期诊断和治疗提供帮助。
1. 上皮细胞激活成纤维细胞促进EC的发展
ESCC是通过多阶段上皮癌症形成发展起来的,即从正常上皮、低级别上皮内瘤变到侵袭性癌。然而,癌前病变如何发展为癌症仍然难以捉摸。北京协和医学院病因学与致癌学系Chen Wu团队报告了对29例ESCC患者的79个多期食管病变的全面单细胞RNA测序和空间转录组学研究[1]。他们发现上皮细胞中由于转录因子KLF4在病变进展过程中受到抑制,ANXA1的表达逐渐显著下降。ANXA1是成纤维细胞中维持成纤维细胞稳态的2型甲酰基肽受体(FPR2)的配体(图1)。ANXA1的缺失导致正常成纤维细胞不受控制地转化为癌症相关成纤维细胞(CAFs),这可以通过恶性上皮细胞分泌的TGF-b来增强。鉴于CAFs在癌症中的作用,这项研究强调了ANXA1/FPR2信号是上皮细胞和成纤维细胞之间促进ESCC的重要串扰机制。

2. Barrett食管癌转化中的染色体外DNA
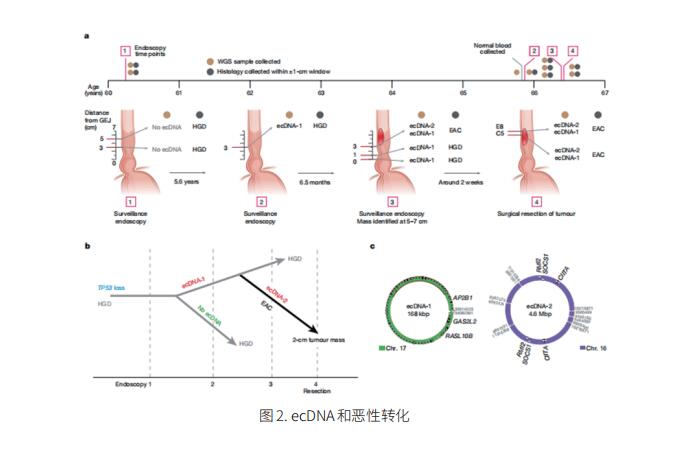
染色体外DNA(ecDNA)上的癌基因扩增驱动肿瘤的进化及其对治疗的耐药性,并与癌症患者的不良预后相关。Barrett食管,一种由正常食管鳞状黏膜向柱状内膜的化生转化,是已知的EAC的前兆。为了更好地了解ecDNA的发展,美国斯坦福大学医学院病理学系Paul S. Mischel团队分析了EAC或巴雷特食管患者的全基因组测序(WGS)数据[2]。ecDNA的频率在Barrett食管相关的早期EAC(24%)和晚期EAC(43%)之间增加,这表明ecDNA是在癌症进展过程中形成的。在癌症诊断前收集的活检中,后来发生EAC的患者样本中的ecDNA水平高于未发生EAC的患者样本。他们还发现ecDNA包含多种致癌基因和免疫调节基因(图2)。此外,在疾病晚期,ecDNA的拷贝数和结构复杂性都有所增加。这些研究结果表明,ecDNA是从高度不典型增生到癌症转变的早期事件,并提高了对含ecDNA肿瘤患者进行早期干预或预防的可能性。
3. 肿瘤单核细胞含量预测EAC免疫化疗结果
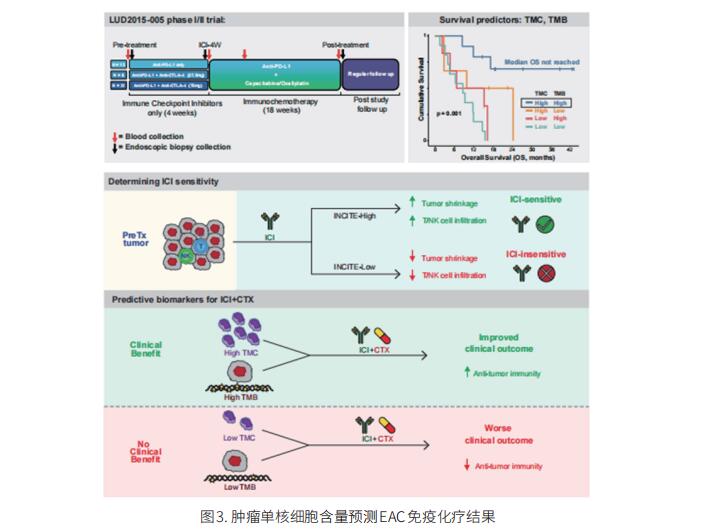
对于无法手术治疗的EAC患者,确定是否能从免疫化疗(ICI+CTX)中受益仍然是一个关键挑战。英国牛津大学路德维希癌症研究所Xin Lu团队通过一项独特设计的临床试验(LUD2015-005)解决了这个问题,在该试验中,35名不能手术的EAC患者接受了为期四周的一线免疫检查点抑制剂(ICI-4W)以及随后的ICI+CTX治疗[3]。全面的生物标志物分析,包括食管癌症65000个细胞的单细胞RNA序列图谱的生成,以及ICI-4W治疗期间EAC的多时间点转录组分析,揭示了一种新的T细胞炎症特征(INCITE),其上调与ICI诱导的肿瘤缩小相关。使用构建的单细胞图谱对治疗前胃食管癌转录组进行反卷积,发现高肿瘤单核细胞含量(TMC)是LUD2015-005患者更高总生存率(OS)的特异性预测因子(图3)。肿瘤突变负荷(TMB)是LUD2015-005 OS的一个额外的独立和加性预测因子。这些结果确定TMB和TMC的组合是免疫化疗反应的潜在生物标志物,改善EAC患者的治疗选择。
参考文献
[1]Chen Y, Zhu S, Liu T, et al. Epithelial cells activate fibroblasts to promote esophageal cancer development [J]. Cancer Cell. 2023;41(5):903-918.e8. (IF=50.3)
[2]Luebeck J, Ng AWT, Galipeau PC, et al. Extrachromosomal DNA in the cancerous transformation of Barrett's oesophagus [J]. Nature. 2023;616(7958):798-805. (IF=64.8)
[3]Carroll TM, Chadwick JA, Owen RP, et al. Tumor monocyte content predicts immunochemotherapy outcomes in esophageal adenocarcinoma [J]. Cancer Cell. 2023;41(7):1222-1241.e7. (IF=50.3)
云克隆不仅可提供多种肿瘤实验动物模型,包括肿瘤移植动物模型、自发性肿瘤动物模型、诱发性肿瘤动物模型、肿瘤转移动物模型等,涵盖常见肿瘤研究。还具有各类癌症检测指标及上述KLF4、ANXA1、FPR2、TGF-b等相关产品,可助力广大科研工作者进行癌症相关研究。