重新激活癌细胞凋亡的新分子——TCIP1
在生命的过程中,细胞凋亡是一种正常的细胞死亡方式,是维持生命平衡的重要手段。但不是所有细胞都会接受细胞死亡的命运,癌细胞就是个代表,它们逃避细胞凋亡,成为机体内的不死细胞。如果我们能重新找到让癌细胞凋亡的开关,是不是就可以战胜癌症呢?
斯坦福大学研究团队近期发表在《Nature》上的题为“Rewiring cancer drivers to activate apoptosis”的文章,发现了一种诱导癌细胞调亡的方法,他们描述了一类名为转录/表观遗传邻近化学诱导剂(Transcriptional/Epigenetic Chemically Induced Proximity, TCIP)的新分子,邻近化学诱导剂利用化学小分子诱导两种生物大分子发生临近互作从而调控细胞进程,TCIPs可以借助癌细胞内癌症生长基因的表达激活细胞凋亡。

下面,我们参考这篇文献看一下研究团队的研究思路:
1. TCIPs分子的设计和筛选及体外杀伤效果
研究团队构建了一系列将特定转录抑制剂与转录激活剂结合在一起的分子。其中最有效的分子是TCIP1,将结合BCL6的小分子与结合转录激活剂BRD4的小分子连接起来发挥作用,BRD4将激活BCL6所结合的任何东西,激活癌细胞试图用BCL6抑制的任何基因表达,包括凋亡基因。BCL6的功能是抑制转录、抑制细胞凋亡,BRD4在癌细胞中的正常作用是促进癌细胞的快速生长和增殖。TCIP1成功杀死4种高表达BCL6的大B细胞淋巴瘤细胞系(DLBCL),包括化疗耐药的TP53突变系(KARPAS422细胞),并表现出细胞特异性和组织特异性效应。细胞凋亡的激活到细胞死亡的完成只需72小时。

图1. TCIP1的合成及重新激活癌细胞转录通路
(图片源自《Nature》)
2. 淋巴瘤细胞的杀伤需要形成BRD4、BCL6和TCIP1的三元复合物
仅通过增加BRD4或BCL6抑制剂(JQ1或BI3812),TCIP1分子的选择性杀伤效应非常有限。与此同时,研究团队还合成了阴性对照化合物Neg1和Neg2(与TCP1有相同的结构,但具有已知的分别改进过的与BRD4或BCL6弱结合的能力),以验证TCIP1分子的特异性作用。结果显示,这两种化合物与BRD4或BCL6的结合能力均受到削弱,因此无法有效地杀伤DLBCL细胞。这些实验结果表明TCIP1分子的选择性杀伤作用需要BRD4、BCL6和TCIP1三者的三元复合物的共同参与。

图2. TCIP1的杀伤作用需要形成三元复合物
(图片源自《Nature》)
3. TCIP1激活的细胞凋亡在整个细胞周期都可发生
很多化疗药物仅在特定的细胞周期发挥作用,一些癌细胞可以据此躲避化疗药物的杀伤作用,而TCIP1可在整个细胞周期活化癌细胞调亡并具有剂量依赖性。进一步通过血清饥饿模型发现,TCIP1诱导的癌细胞调亡对血清浓度的降低更加敏感。这些观察结果表明,TCIP1是淋巴瘤细胞凋亡的有效诱导剂。
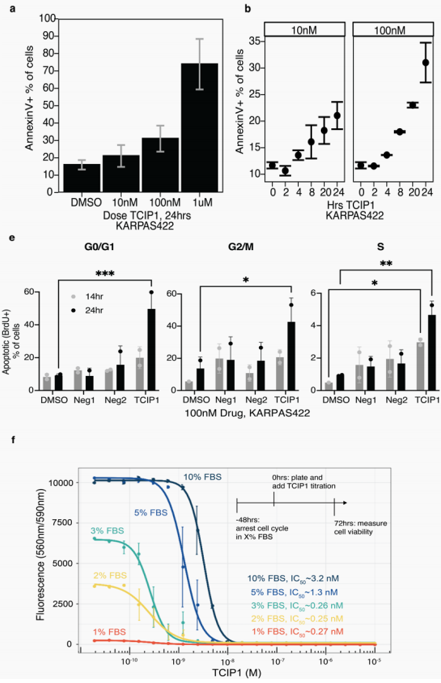
图3. TCIP1激活的细胞凋亡发生在整个细胞周期
(图片源自《Nature》)
4. TCIP1重新编辑基因表达
向KARPAS422细胞中加入TCIP1分子,发现1674个基因的表达上调,1364个基因的表达下调。其中,被TCIP1激活的这些基因包括被BCL6抑制的靶基因,如:CDKN1A(p21)、FOXO3、PMAIP1/NOXA、TP53。并且,TCIP1还下调了MYC(编码转录因子的促肿瘤基因)及其多个转录靶标的表达。这些结果表明,TCIP1分子能够直接调节多个基因的表达,从而影响细胞的生长和凋亡,TCIP1有效地重新编辑了DLBCLs的转录调控网络,激活了细胞凋亡的途径从而有效的对癌细胞发挥杀伤作用。
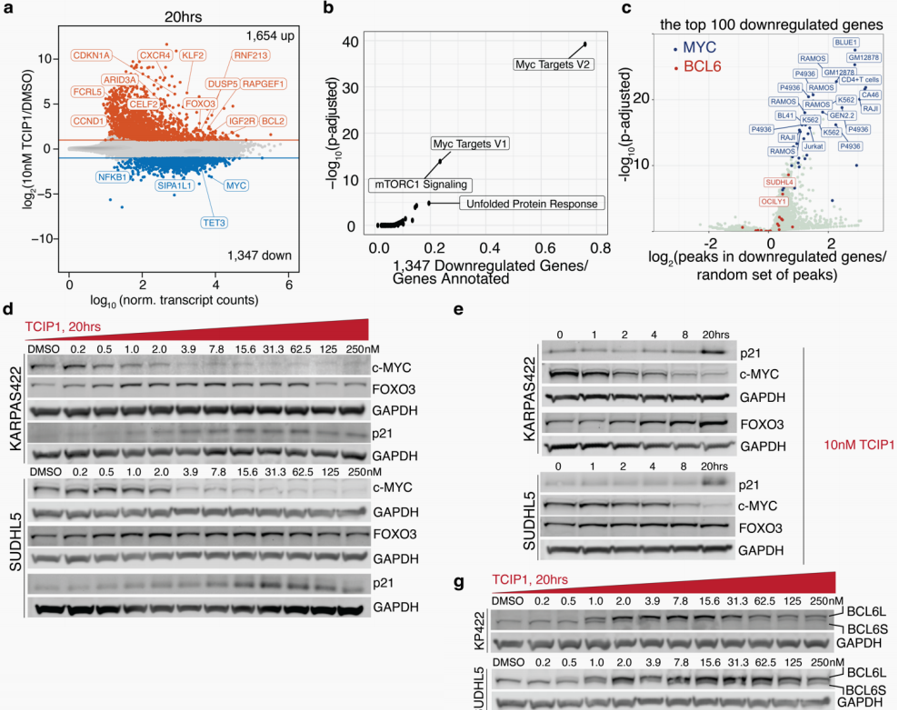
图4. TCIP1重新编辑DLBCLs的转录调控网络
(图片源自《Nature》)
5. TCIP1对人原代细胞和小鼠的无毒性
TCIP1导致的细胞死亡是否精确地靶向于癌细胞,而不是正常细胞。为了验证这一预测,研究团队检测了原代人类细胞,包括成纤维细胞和淋巴细胞,尤其是T和B淋巴细胞,因为T和B淋巴细胞高表达BCL6。研究发现,TCIP1同时可以杀死成纤维细胞和淋巴细胞所需的TCIP1用量至少是杀死过表达BCL6的DLBCLs所需水平的100倍,表明存在一个实质性的治疗窗口。TCIP1的无毒性同时在小鼠肿瘤模型上得到了进一步验证。
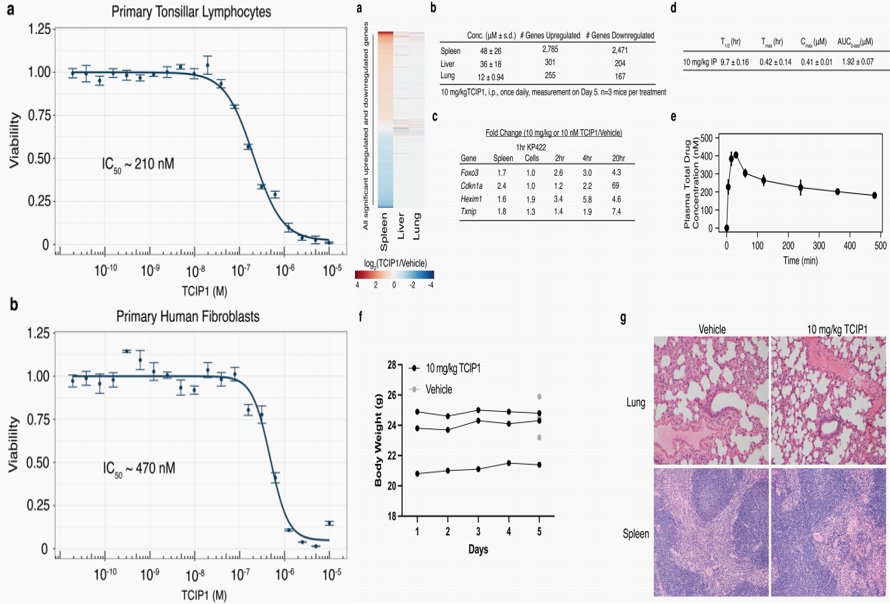
图5. TCIP1的体内外毒性验证
(图片源自《Nature》)
该研究介绍了一种新的治疗癌症的策略,利用TCIP分子来激活细胞凋亡途径,从而抑制癌细胞的增殖和生存。研究团队设计了一种邻近化学诱导剂——TCIP1,可结合BCL6与BRD4,这种化合物形成了一个三元复合物,TCIP1可以杀死表达BCL6的DLBCLs细胞。并认为TCIP1的普适性,认为TCIP1除了治疗DLBCLs外,还可以用于治疗多种表达BCL6的肿瘤,该研究为癌症治疗策略提供了新思路和方法。
云克隆可提供以上研究的相关指标产品:
靶标 | 核心货号 | 靶标 | 核心货号 |
BCL6 | E586 | TP53 | A928 |
CD95 | A030 | BRD4 | F129 |
c-MYC | B290 | BCOR | C327 |
NCOR | F100 | BCL2 | A778 |
CASP8 | A853 | FOXO3 | A762 |
CDK9 | A496 | p21 | E624 |
BCL2L11 | Q166 |
更多信息,欢迎访问:http://www.cloud-clone.cn/