突破光穿透深度限制,光纤疗法带来的癌症治疗革命
国际癌症研究机构估计,全世界20%的人一生中将患上癌症。传统的手术、化疗和放疗目前被用作大多数癌症患者的可用临床方法。然而,由于不可避免地对药物和放疗产生耐药性,传统的化疗和放疗疗效不佳。作为一种新兴的以光为介质的癌症治疗方法,纳米材料从光子中吸收能量并部分以热的形式消散以引发癌症细胞死亡的光热疗法(PTT)因其无创性、高特异性和高效率以及不显著的副作用而引起了人们的广泛关注。然而,PTT仍然面临着一个重大挑战,即光在体内的穿透深度有限。考虑到上述问题,光纤提供了解决这些问题的可能性。在PTT领域,光纤可以在体内用作光导介质,从而大大减少光在组织中的散射和吸收,克服光穿透深度有限的障碍。
2023年11月29日,暨南大学光子技术研究所Bai-Ou Guan和Yunyun Huang团队在《Advanced Materials》上发表题为“Marriage of a Dual-Plasmonic Interface and Optical Microfiber for NIR-II Cancer Theranostics”的文章,报道了一种集癌症检测和治疗功能于一体的光热治疗纤维。

在这篇文章中,云克隆蛋白【甲胎蛋白(AFP)重组蛋白,RPA153Ra01】受到科研工作者的认可,荣登优秀国际期刊。

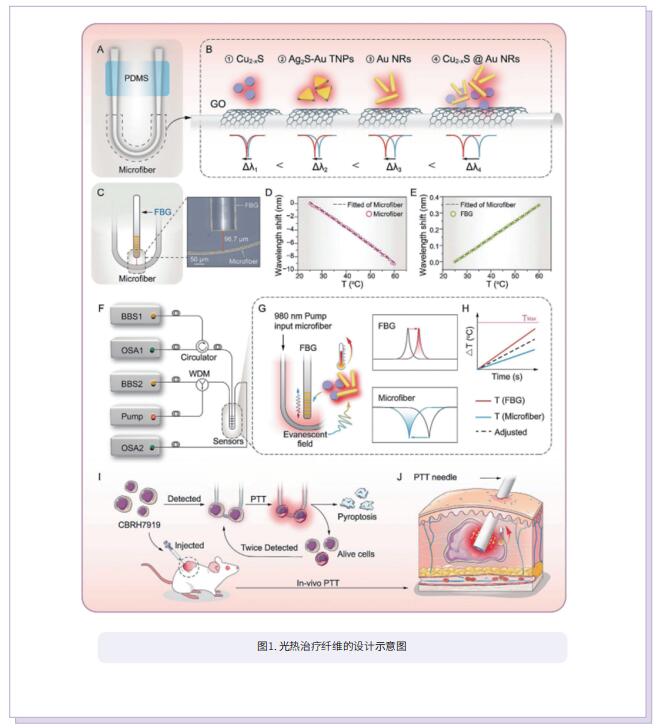
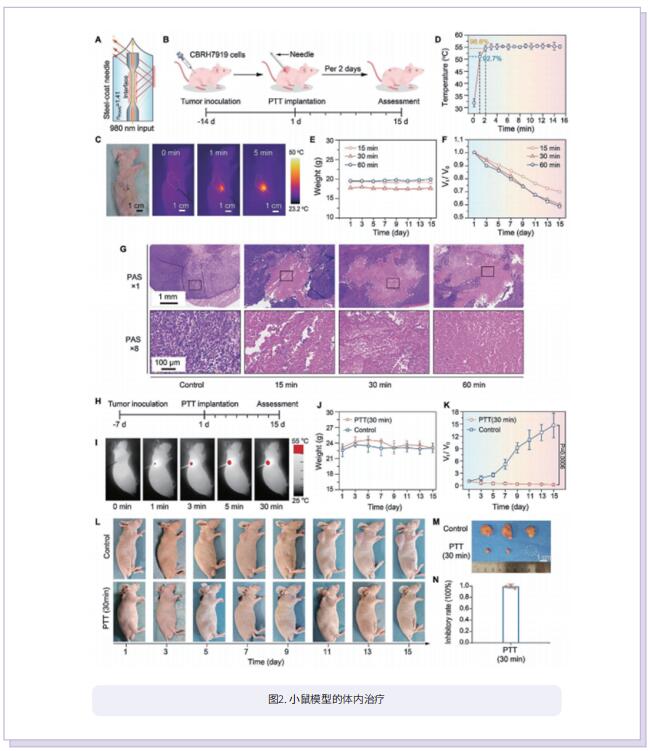
在这项研究中,作者提出了一种通过界面设计将光纤和光热剂的设计概念相结合的技术。使用光学微纤维作为PTT平台,在微纤维界面上组装光热剂以开发PTT纤维。界面材料的光热效应使光纤能够灵活地进行温度调节。此外,光纤的实时温度可以通过侧面的光纤布拉格光栅(FBG)记录。界面的灵活性有助于将制备的纤维的温升调节在0°C和90°C之间。由于光学微纤维的传感器性质,制备的纤维可以量化癌症细胞。因此,该光纤不仅可以在检测到癌症细胞的部位对癌症细胞和肿瘤组织进行PTT,反过来,它能够通过光学微纤维传感器定量癌症细胞来评估PTT效果。该光纤由双等离激元纳米界面和光学微纤维所组成,能够区分癌细胞与正常细胞、量化癌细胞、对癌细胞进行热消融以及评估消融效果。研究发现,基于该光纤的单次治疗的肿瘤细胞消融率能够达到89%。体内外研究结果进一步证明了该光纤能够在NIR-II窗口内实现快速的深部组织光子热疗,以显著消融肿瘤。
综上所述,这项研究开发了一种具有癌症细胞检测和NIR-II PTT功能的纤维。双等离激元纳米界面和光学微纤维的结合有可能克服光穿透深度有限、在正常组织中非特异性积聚和意外损伤等障碍。这项工作为探索在癌症诊断、治疗和术后监测方面同时具有功能的综合治疗平台提供了见解,以供未来的实际应用。